ACUERDO que modifica el Anexo Único del diverso por el que el Consejo de Salubridad General declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, publicado el 14 de diciembre de 2016.
Al margen un sello con el Escudo Nacional, que dice: Estados Unidos Mexicanos.- GOBIERNO DE MÉXICO.- Consejo de Salubridad General.
El Consejo de Salubridad General, con fundamento en los artículos 4o, párrafo cuarto y 73, fracción XVI, Bases 1a. y 3a. de la Constitución Política de los Estados Unidos Mexicanos; 3o., fracciones II y XXVII Bis, 4o., fracción II, 17, fracción VI y 33, fracción IV de la Ley General de Salud, así como 1, 9, fracciones II y VI y 10, fracción VIII del Reglamento Interior del Consejo de Salubridad General, y
CONSIDERANDO
Que el artículo 4o, párrafo cuarto de la Constitución Política de los Estados Unidos Mexicanos, establece que toda persona tiene derecho a la protección de la salud;
Que, en términos de lo dispuesto en los artículos 73, fracción XVI, bases 1a y 3a de la Constitución Política de los Estados Unidos Mexicanos y 4o, fracción II de la Ley General de Salud, el Consejo de Salubridad General tiene el carácter de autoridad sanitaria y sus disposiciones generales serán obedecidas por las autoridades administrativas del país;
Que el Consejo de Salubridad General, con base en las atribuciones que le concede la Constitución Política de los Estados Unidos Mexicanos, la Ley General de Salud, su Reglamento Interior y otros ordenamientos jurídicos, en el ámbito de su competencia, participa en la consolidación y funcionamiento del Sistema Nacional de Salud;
Que el artículo 3o, fracciones II y XXVII Bis de la Ley General de Salud, establece que la atención médica y el tratamiento integral del dolor, son materia de salubridad general;
Que, con fundamento en las disposiciones señaladas, el 14 de diciembre de 2016 el Consejo de Salubridad General publicó en el Diario Oficial de la Federación el Acuerdo por el que se declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, cuyo contenido es necesario actualizar conforme a las mejores prácticas clínicas conocidas en la actualidad, y
Que en virtud de las anteriores consideraciones y a fin de garantizar que las actividades de atención médica paliativas que se brindan a menores de edad sean acordes con las necesidades específicas de dicho segmento de la población, el Consejo de Salubridad General aprobó, en su segunda sesión ordinaria celebrada el 8 de diciembre de 2021, el siguiente
ACUERDO
ÚNICO. Se modifica el Anexo Único del Acuerdo por el que se declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, publicado en el Diario Oficial de la Federación el 14 de diciembre de 2016.
TRANSITORIO
ÚNICO. El presente Acuerdo entrará en vigor al día siguiente de su publicación en el Diario Oficial de la Federación.
Dado en la Ciudad de México, a los treinta y un días del mes de agosto de 2022.- El Presidente del Consejo de Salubridad General y Secretario de Salud, Jorge Carlos Alcocer Varela.- Rúbrica.
ANEXO ÚNICO
Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico
| Coordinación general | |
| Dr. José Ignacio Santos Preciado | Consejo de Salubridad General |
| Dr. Juan García Moreno | Consejo de Salubridad General |
| Dr. Ricardo Plancarte Sánchez | Instituto Nacional de Cancerología |
| Capítulo I | |
| Dra. Kenya Sosa Sánchez | Hospital Infantil de México "Federico Gómez" |
| Dr. Juan Arenas Arrocena | Hospital del Niño Morelense |
| Capítulo II | |
| Dra. Mónica Osio Saldaña | Seminario de Globalidad. Universidad Nacional Autónoma de México |
| Dra. Anaid Dordelly Hernández | Hospital del Niño, Saltillo Coahuila |
| Dra. Iliana Verónica Cortés Ponce | Dirección General de Calidad y Educación en Salud. Secretaría de Salud Federal |
| Lic. Jimena Cabrera Camargo | Consejo de Salubridad General |
| Mtro. Manuel Bandala Ledesma | Consejo de Salubridad General |
| Capítulo III | |
| Dra. Alejandra Laura Nava Martínez | Unidad Médica de Alta Especialidad. Hospital de Pediatría "Dr. Silvestre Frenk Freund", Centro Médico Nacional Siglo XXI |
| Dra. Jessica Haydee Guadarrama Orozco | Hospital Infantil de México "Federico Gómez" |
| Dr. Marcos Homar Córdova Juárez | Hospital de la Niñez Oaxaqueña |
| Capítulo IV | |
| Dr. Sergio Abel Castañeda Ramírez | Instituto Nacional de Pediatría |
| Dra. Irma Alejandra Coronado Zarco | Instituto Nacional de Perinatología "Isidro Espinosa de los Reyes" |
| Dr. Alejandro Escalona Espinosa | Hospital Español |
| Dra. Blanca Olivia Almazán García | Centro Médico Nacional 20 de Noviembre, Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado |
| Dra. Adriana Barrientos Deloya | Instituto Nacional de Pediatría |
| Dra. Celina Castañeda de la Lanza | Secretaría de Salud del Estado de México |
| Capítulo V | |
| Dra. Enjie Fakhr El Din Ismail Paz | Hospital Infantil de México "Federico Gómez" |
| Dra. Georgina Velasco Pérez | Instituto Nacional de Pediatría |
| Dr. Jorge Alberto Ramos Guerrero | Hospital General de Occidente. Secretaría de Salud, Jalisco |
| Dra. Yuriko Nakashima Paniagua | Hospital Civil de Guadalajara "Dr. Juan I. Menchaca" |
| Dra. Edith Adriana Benitez Vázquez | Hospital Civil de Guadalajara "Dr. Juan I. Menchaca" |
| Dra. Angélica Duarte Castro | Instituto Nacional de Pediatría |
| Dr. Jorge Mauricio Cervantes Blanco | Ejercicio privado |
| Capítulo VI | |
| Psic. José Méndez Venegas | Hospital Infantil Teletón de Oncología. Querétaro |
| Mtra. Margarita Dávila Robledo | Docente colaboradora del CSG. Ejercicio privado |
| Psic. Claudia Nidia Lima Carcaño | Voluntariado Oncología CMN SXXI |
| Psic. Mtra. Azareel Maya Del Moral | Hospital de Especialidades del Niño y la Mujer. Querétaro |
| Capítulo VII | |
| Dra. Psic. María Aurora Mortera Gutiérrez | Centro Médico Naval. Secretaría de Marina |
| Mtra. Margarita Dávila Robledo | Docente colaboradora del CSG. Ejercicio privado |
| Psic. Mtra. Martha Gabriela García Durán | Hospital Pediátrico de Sinaloa "Dr. Rigoberto Aguilar Pico" |
| Lic. Enf. Adriana Aidé Galicia Núñez | Hospital Infantil de México "Federico Gómez" |
| Capítulo VIII | |
| Dr. Edén González Roldán | Comisión Nacional de Bioética |
| Dr. Armando Garduño Espinosa | Instituto Nacional de Pediatría |
| Dra. Iris Mabel Narváez Sarmiento | Centro Médico 20 de Noviembre, Instituto de Seguridad y Servicios Sociales de los Trabajadores del Estado. |
| Dr. David Benitez Valladares | Comisión de Bioética Secretaría de Salud de la Ciudad de México |
| Enf. María Cristina Reyes Lucas | Instituto Nacional de Pediatría |
| Capítulo IX | |
| Mtra. María de Lourdes Dávalos Rodríguez. | Consejo de Salubridad General |
| Dr. Jorge Alberto Ramos Guerrero | Hospital General de Occidente. Secretaría de Salud, Jalisco. |
| Dra. Beatriz Elena Dorsey Rivera | Hospital General ISSSTE Tláhuac. Seminario de Globalidad Universidad Nacional Autónoma de México |
| Dr. Gregorio Zúñiga Villanueva | Departamento Pediatría del Tecnológico de Monterrey |
| Dra. Mónica Osio Saldaña | Seminario de Globalidad. Universidad Nacional Autónoma de México |
| Dra. Norma Esthela Llamas Peregrina | Hospital Civil de Guadalajara, "Dr. Juan I. Menchaca" |
INDICE
Presentación
Prólogo
Capítulo I. Panorama actual de los cuidados paliativos pediátricos a nivel mundial, Latinoamérica y en México.
1.1 Introducción.
1.2 Panorama Internacional.
1.3 Latinoamérica.
1.4 Panorama Nacional.
Bibliografía.
Capítulo II. Marco jurídico de los cuidados paliativos pediátricos.
Bibliografía.
Capítulo III. La atención paliativa pediátrica.
3.1 Definición de cuidados paliativos pediátricos.
3.2 Historia de los cuidados paliativos pediátricos.
3.3 Definiciones de importancia para el tema.
3.4 Categorías de enfermedades limitantes para la vida y amenazantes para la vida.
3.5 Generalidades de la atención paliativa pediátrica.
3.6 Organización y atención de la atención paliativa.
3.7 Atención domiciliaria.
Bibliografía.
Capítulo IV. Modelos de provisión de la atención paliativa pediátrica.
4.1 Introducción.
4.2 Modelo de provisión de la atención paliativa perinatal.
4.3 Modelo de provisión para atención paliativa en el paciente no oncológico.
4.4 Modelo de provisión de la atención paliativa pediátrica en el paciente oncológico.
4.5 Modelo de provisión de la atención paliativa pediátrica con transición a la vida adulta.
Bibliografía.
Capítulo V. Control de signos y síntomas en cuidados paliativos pediátricos.
5.1 Dolor y su abordaje multimodal.
5.2 Síntomas sistémicos.
5.3 Síntomas respiratorios.
5.4 Síntomas gastrointestinales.
5.5 Síntomas neuro-psiquiátricos.
5.6 Síntomas dermatológicos.
5.7 Urgencias paliativas.
5.8 Manejo de síntomas refractarios (Sedación paliativa).
Bibliografía.
Capítulo VI. Atención psicosocial, espiritual y duelo en los cuidados paliativos pediátricos.
6.1 Atención psicosocial.
6.2 Espiritualidad en cuidados paliativos pediátricos.
6.3 Duelo.
Bibliografía.
Capítulo VII. Comunicación en los cuidados paliativos pediátricos.
7.1 Definición de comunicación.
7.2 Objetivos de la comunicación.
7.3 Elementos de la comunicación.
7.4 Cuatro ejes que guían el alcance de la comunicación dentro de los cuidados paliativos para pacientes pediátricos.
7.5 Comunicación colaborativa.
7.6 Un enfoque de equipo interdisciplinario para la comunicación.
7.7 Manejo de conflictos.
7.8 Conciencia pronóstica.
7.9 Comunicación con las familias al final de la vida y durante el duelo.
7.10 Comunicación con el paciente.
7.11 Comunicación con los hermanos y familia extendida.
7.12 Conceptos de muerte y enfermedad en el niño/adolescente.
7.13 Comunicar las malas noticias.
7.14 Conspiración del silencio.
Bibliografía.
Capítulo VIII. Consideraciones bioéticas en los cuidados paliativos pediátricos.
8.1 Introducción
8.2 Marcos teóricos
8.3 Marcos metodológicos en apoyo a la toma de decisiones
8.4 Aspectos para considerar desde la perspectiva bioética
8.5 Participación de los Comités Hospitalarios de Bioética
8.6 Investigación en población pediátrica que recibe cuidados paliativos.
8.7 Participación de los Comités de Ética en Investigación.
Bibliografía
Capítulo IX. Competencias para la provisión de cuidados paliativos pediátricos.
9.1 ¿Qué se necesita saber para la provisión de cuidados paliativos pediátricos (CPP)?
9.2 Propósitos.
9.3 Dirigido a:
Profesionales de la salud.
Otras personas involucradas en el CPP.
Organizaciones.
9.4 Escenarios posibles para la atención paliativa.
9.5 Nivel de Complejidad.
9.6 Competencias.
9.7 Formador de formadores.
9.8 Metas.
9.9 Estrategias.
9.10 Formas de intervención: Intervención educativa sinérgica.
Bibliografía
Glosario
Anexo: Enfoque de competencias
PRESENTACIÓN
Las disposiciones y Acuerdos del Consejo de Salubridad General tienen carácter ejecutivo y su cobertura abarca a todo el Sistema Nacional de Salud, gracias a que es la única instancia en el país que, por su estructura, tiene la posibilidad de unificar o alinear a todas las políticas con la de salud y en favor de la salud.
En la actual administración, han existido importantes logros, al vincular sus acciones al Plan Nacional de Desarrollo 2019-2024 y al Programa Sectorial de Salud 2020-2024, mediante 24 funciones, estando dentro de ellas la de "Aprobar los acuerdos necesarios y demás disposiciones generales de observancia obligatoria en el país, en materia de salubridad general, dentro del ámbito de su competencia".
Su visión se actualiza con el devenir de la ciencia, teniendo la innovación como referente y la calidad como sustrato. Asimismo, su filosofía mantiene un enfoque humanista, al considerar a la salud como un derecho humano y a la persona con un valor inapreciable, por lo que sus decisiones fortalecen la atención de la población con mayor grado de vulnerabilidad.
En este contexto, se ha realizado la actualización de la presente "Guía de Cuidados Paliativos Pediátricos", anexa al Acuerdo por el que se declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos en el paciente pediátrico, publicado en el Diario Oficial de la Federación el 14 de diciembre de 2016.
El trabajo fue realizado por 40 profesionales de 23 instituciones de salud y académicas, convergiendo el trabajo de médicos especialistas en: Pediatría, Anestesiología Pediátrica, Algología Pediátrica, Reumatología Pediátrica, Cuidados Paliativos Perinatales, Neonatología, Neurología Pediátrica y Oncología Pediátrica, todos ellos con formación y experiencia en el ejercicio de la Medicina Paliativa.
De igual manera, se contó con la colaboración de maestros y doctores en Psicología, Tanatología, Psico-Oncología, Educación, Sociología, Derecho, Bioética y Enfermería, cuyo desempeño profesional está relacionado con los aspectos normativos, o bien operativos del control del dolor y la aplicación permanente de la Medicina Paliativa.
Cabe destacar que la presente Guía fue elaborada mediante reuniones virtuales, en las cuales se organizaron nueve grupos, acorde al número de capítulos determinados, con la participación de profesionales de diferentes instituciones, turnos y lugares de adscripción en el país. Debido a ello, hubo necesidad de que, cada grupo citara la bibliografía correspondiente al final de su capítulo, numerándola conforme apareciera en el contenido. Lo cual explica por qué una misma cita puede aparecer en más de un capítulo, y evidentemente, al hacer referencia a un concepto o idea determinados, tiene un lugar específico en la numeración correspondiente según el capítulo que la contiene.
El trabajo de los profesionales participantes, plasmado en la presente Guía de Cuidados Paliativos Pediátricos, por demás excelso, seguramente se verá recompensado en cada paciente que de alguna manera sea beneficiado con las decisiones del personal de salud que lo atienda, por lo cual el Consejo de Salubridad General les manifiesta un merecido reconocimiento y les agradece su incondicional y valiosa colaboración.
Dr. José Ignacio Santos Preciado
PRÓLOGO
Los cuidados paliativos pediátricos, desde la perspectiva de la Organización Mundial de la Salud (OMS), constituyen "un enfoque que mejora la calidad de vida de los pacientes y familias que afrontan una enfermedad que amenaza la vida de un niño, a través de la prevención y alivio del sufrimiento".
Con la presente Guía de Cuidados Paliativos Pediátricos, se tiene el propósito de orientar y fortalecer acciones en la prestación de servicios en todas las instituciones de salud y académicas de las entidades federativas de México, acorde y con apego a los diferentes Modelos de Atención con que operan las diversas
instituciones.
Contar con esta Guía, representa también, sin duda, la posibilidad de que el personal para la atención de la salud esté mejor informado, coadyuvando con ello al logro de una visión integral de la atención de y con calidad, que favorezca su desempeño, su desarrollo profesional y le aporte información actualizada para disipar dudas, y a la vez, se propicie la calidad de vida de los pacientes que necesitan los cuidados paliativos, o, en dado caso, reciban un acompañamiento verdaderamente profesional para comprender y aceptar sus condiciones y pronóstico de salud, sin omitir la atención que necesariamente requieren sus familias.
En la determinación de su contenido, se tuvo especial cuidado en tener consenso, participando profesionales de instituciones del ámbito público y privado, todos con formación y experiencia en cuidados paliativos enfocados a la población pediátrica, lo cual permite sustentar que la presente guía, tiene un elevado valor desde el punto de vista científico y como particular relevancia, un material enfocado a las necesidades y características de la población mexicana.
La sólida formación, experiencia y trayectoria profesional de los autores, representan una garantía para la obtención de la guía como fuente de consulta confiable, ya que incorpora información actualizada sobre aspectos conceptuales, regulatorios, atención paliativa pediátrica, modelos de atención, atención psicosocial, espiritual y en duelo en los cuidados paliativos pediátricos, comunicación, aspectos bioéticos y competencias para la provisión de cuidados paliativos pediátricos.
Vale la pena destacar que, en el desarrollo de cada uno de sus capítulos, está considerado el marco conceptual generador de las premisas que determinan la postura del Consejo de Salubridad General sobre los cuidados paliativos pediátricos:
1. Considerar las directrices del contexto internacional;
2. Propiciar que las políticas relacionadas con el "Control del Dolor Crónico y la Aplicación Permanente de la Medicina Paliativa", estén en concordancia con los aspectos legislativos y normativos correspondientes;
3. Disponer de medicamentos para el tratamiento del dolor y otros síntomas en los tres niveles de atención;
4. Incrementar la infraestructura y fomentar la formación y capacitación del personal de salud; y
5. Fortalecer a las instituciones públicas de salud, para lograr modelos de atención eficaces.
Así mismo, valorar a los cuidados paliativos pediátricos, no sólo como acciones a realizar por el personal de salud, sino como la necesidad de reconocerla como una nueva especialidad e impulsar la formación de especialistas en Medicina Paliativa Pediátrica.
Dr. Ricardo Plancarte Sánchez
CAPITULO I
PANORAMA ACTUAL DE LOS CUIDADOS PALIATIVOS PEDIÁTRICOS A NIVEL MUNDIAL, LATINOAMÉRICA Y EN MÉXICO
1.1 INTRODUCCIÓN
El acceso a los cuidados paliativos es un desafío emergente y una prioridad de salud pública, crucial para la salud mundial. Los pacientes con enfermedades graves experimentan una carga considerable de sufrimiento.
La necesidad de cuidados paliativos nunca ha sido mayor y está aumentando a un ritmo rápido debido al envejecimiento de la población mundial, y a los adelantos de la ciencia para la sobrevida de recién nacidos prematuros y con enfermedades amenazantes para la vida, el aumento del cáncer y otras enfermedades no transmisibles y la reciente aparición de COVID-19. Para 2060, se espera que la necesidad de cuidados paliativos al final de la vida se duplique. (1)
Los cuidados paliativos deben proporcionarse de acuerdo con los principios de la cobertura sanitaria universal. Todas las personas, independientemente de sus ingresos, tipo de enfermedad o edad, deberían tener acceso a un conjunto de servicios básicos de salud determinados a nivel nacional, incluidos los cuidados paliativos. Los sistemas financieros y de protección social deben tener en cuenta el derecho humano a los cuidados paliativos para los grupos de población pobres y marginados. (2)
Existen múltiples acuerdos, pactos, artículos, organizaciones y organismos internacionales en el mundo, entre ellas la OMS que se han pronunciado a favor de los cuidados paliativos como un derecho humano, esto incluye el derecho a la salud y el derecho a no ser sometido a tratos crueles, inhumanos y degradantes. Esto implica implementar el acceso a los cuidados paliativos en todos los niveles de atención, lo que obliga a las naciones a desarrollar políticas públicas, leyes, reglamentos y guías de práctica clínica, así mismo asegurar el acceso a medicamentos esenciales para el control de síntomas, e impulsar la educación formal en cuidados paliativos, todo esto con el objetivo de formar una estrategia humanitaria para favorecer los cuidados al final de la vida y permitir una muerte digna. (2)
1.2 PANORAMA INTERNACIONAL
En todo el mundo se estima que más de 56.8 millones de personas requieren cuidados paliativos cada año. Incluidos 31.1 millones antes del final de la vida y 25.7 millones cerca del final de la vida. La mayoría, el 67.1% son adultos mayores de 50 años y al menos el 7% son niños.
La gran mayoría (> 97%) de los niños de 0 a 19 años que necesitan cuidados paliativos viven en países de bajos ingresos.
El número total mundial estimado de niños que necesitan cuidados paliativos en 2017 fue de casi 4 millones. Hay una proporción ligeramente mayor de hombres (53,8%) que de mujeres.
La mayoría de los niños que necesitan cuidados paliativos se encuentran en África y en el Regiones de Asia Sudoriental (51,8% y 19,5% respectivamente), seguidas por las regiones del Mediterráneo Oriental (12%), Pacífico Occidental (7,7%) y Región de las Américas (6,2%). En contraste, la región europea tiene solo el 2.8% del total.
Las regiones de África, el Mediterráneo oriental y el sudeste asiático tienen las tasas más altas por cada 100.000 niños (369, 156, 103 respectivamente).
La condición de Enfermedad que genera mayor necesidad de cuidados paliativos entre los niños es el VIH / SIDA (29,6%), seguida del parto prematuro y traumatismo del nacimiento (17,7%), anomalías congénitas (16,2%) y lesiones (16%). Los cánceres solo representan el 4,1%.
Las enfermedades progresivas no malignas, excluido el VIH / SIDA, generan la mayor necesidad de cuidados paliativos entre los niños de todas las regiones de la OMS, excepto África. El cáncer genera una pequeña proporción de la necesidad en todas las regiones. (3)
1.3 LATINOAMÉRICA
Según el atlas de Cuidados Paliativos de Latinoamérica 2020, se identificaron un total de 123 equipos que corresponden a 0,8 equipos/millón de habitantes menores de 15 años. Esto varía de países con mayor desarrollo como Uruguay con 19,3 equipos / millón de habitantes menores de 15 años a países sin ningún equipo identificado, como Paraguay y Venezuela. Los equipos presentados varían de unidades de cuidados paliativos pediátricos a equipos móviles de interconsulta.
Cinco países tienen una ley específica de cuidados paliativos y de éstos Costa Rica y México tienen un plan nacional. En Chile la ley es específica para pacientes con patología oncológica. Argentina, Brasil, Ecuador, El Salvador, Panamá, Uruguay y Venezuela cuentan con un programa nacional de cuidados paliativos. En México 610,319 personas necesitan atención Paliativa, y solo el 3% de esa población la recibe. (4)
1.4 PANORAMA NACIONAL
México pertenece al grupo de países donde los servicios de cuidados paliativos y hospicio se encuentran en una etapa de integración avanzada en la prestación de servicios generales, un país de esta categoría se caracteriza por el desarrollo de una masa crítica de activismo en cuidados paliativos en una amplia gama de lugares; prestación integral de todo tipo de cuidados paliativos por parte de múltiples proveedores de servicios; una amplia conciencia de los cuidados paliativos por parte de los profesionales de la salud, las comunidades locales y la sociedad en general; una estrategia de cuidados paliativos que se ha implementado y se actualiza periódicamente; disponibilidad irrestricta de morfina y de la mayoría de los analgésicos potentes; impacto sustancial de los cuidados paliativos en la política; la existencia de guías de cuidados paliativos; la existencia de Centros educativos reconocidos y vínculos académicos con universidades con evidencia de integración de los cuidados paliativos en los planes de estudio relevantes; y la existencia de una asociación nacional de cuidados paliativos que ha logrado un impacto significativo.(3)
En materia de política en nuestro país los Derechos Humanos de niñas, niños y adolescentes están previstos en la Constitución Política de los Estados Unidos Mexicanos, en los tratados internacionales y en las demás leyes aplicables, esencialmente en la Convención sobre los Derechos del Niño (CDN) y en la Ley General de los Derechos de Niñas, Niños y Adolescentes, ordenamientos en los que se les reconoce como titulares de derechos.
Es imprescindible que el equipo terapéutico de cuidados paliativos en pediatría esté capacitado para identificar las necesidades a cubrir y resolver las múltiples situaciones que se presenten, mediante intervenciones de probada eficacia, protocolos estandarizados de manejo y criterios uniformes de actuación; de manera que el paciente reciba atención adecuada y de calidad.
El eje rector de la toma de decisiones en pediatría se centra en el mayor bienestar del menor. En esta situación, la integración de un diagnóstico clínico y de un pronóstico son indispensables, sin embargo, el reto para el personal de salud es poder ofrecer al paciente pediátrico y su familia, equilibrio entre las diferentes opciones terapéuticas posibles a lo largo de la evolución de la enfermedad, el impacto en calidad de vida del paciente y las preferencias del menor y su familia. (5)
En materia de formación de profesionales, para efecto de realizar el aval educativo en materia de cuidados paliativos pediátricos, en los términos previstos en el Acuerdo por el que el Consejo de Salubridad General declara la Obligatoriedad de los Esquemas de Manejo Integral de Cuidados Paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos, publicado en el Diario Oficial de la Federación el 26 de diciembre de 2014, se consideraron distintas instituciones, entre las que destacan las universidades nacionales, instituciones y hospitales nacionales del sector salud facultados en la atención
pediátrica, academias y consejos nacionales relacionados con la atención pediátrica, asociaciones y sociedades médicas como la Asociación Mexicana para Estudio y Tratamiento del Dolor (AMETD), Asociación Mexicana de Cuidados Paliativos (AMECUP), Asociación Mexicana de Cuidados Paliativos y Algiólogos A.C. (AMECPA), Colegio Mexicano de Cuidados Paliativos A.C. otros organismos avalados por la Secretaría de Salud, la Secretaría de Educación Pública y la Universidad Nacional Autónoma de México. (5)
Sólo dieciséis de las 102 facultades de medicina en México ofertan cursos sobre cuidados paliativos para estudiantes de medicina de pregrado y estos cursos son obligatorios en sólo dos de ellas, se cuenta también con cursos de alta especialidad y Subespecialidad en Medicina Paliativa, con reconocimiento universitario. (6)
Así mismo desde la publicación de estos acuerdos, (5) se han sumado más universidades y hospitales en las distintas entidades federativas de nuestro país, así como grupos de cada vez mayor crecimiento en la formación profesional para la atención pediátrica, siendo en los últimos dos años el registro de más unidades con atención paliativa pediátrica.
Estas mismas organizaciones en sincronía con el gobierno federal son las encargadas de realizar distintas guías de manejo adecuadas para su aplicación a nivel de toda la República Mexicana, en el afán de ser incluyente con la población pediátrica.
En materia de acceso a medicamentos se creó una modificación en el 2020 al Compendio Nacional de Insumos para la Salud, en los que cada vez se incluyen más medicamentos de presentación pediátrica para el manejo y control de síntomas, y se incluyen nueve opioides en distintas presentaciones para el uso en el control de dolor como síntoma principal en el paciente terminal pediátrico. (7)
Actualmente poco más del 70% de las entidades federativas de la República Mexicana cuentan con al menos una unidad de atención paliativa que atiende pacientes pediátricos, estas unidades iniciaron su formación a partir del 2005 con el Instituto Nacional de Pediatría como pioneros con el Dr. Armando Garduño Espinoza como su principal líder (8), de la misma manera las unidades del Hospital Civil Dr. Juan I Menchaca con la Dra. Yuriko Nakashima Paniagua, se ha convertido en el principal grupo en el occidente de la República; y a partir de esas fechas se ha contado con un crecimiento notable de unidades que brindan atención paliativa a los niños y niñas en el país. Muchas de estas unidades iniciaron operaciones dirigidas en ocasiones por personal para adultos, pero cada vez se vuelven específicas para el paciente pediátrico integrando a sus filas a cada vez más especialistas en la rama pediátrica. (6)(8)
A pesar de la promoción intensa que se realiza día con día de los cuidados paliativos en México, el alcance de sus beneficios a la población está muy lejos de compararse con los países desarrollados. Aunque se conocen las múltiples necesidades de los pacientes pediátricos que requieren el soporte de cuidados paliativos, para poder satisfacerlas, se requiere un enfoque de equipo multidisciplinario e interdisciplinar, lo cual se logra con capacitación constante en el área al personal de salud.
La necesidad de los cuidados paliativos en el país apremia, y dado que todos los seres humanos somos susceptibles de tener sufrimiento durante o al final de nuestras vidas, se requiere urgentemente que se dispongan los recursos necesarios para llevarlos a cabo, no basta el cúmulo de conocimientos, se necesita desarrollar una medicina con enfoque compasivo, que proporcione alivio del sufrimiento para los niños y sus familias.
Los cuidados paliativos son la oportunidad perfecta para entrelazar otras disciplinas como la bioética, el desarrollo humano, trabajo social, que permitan dignificar el estado de salud de las personas que lo necesiten.
BIBLIOGRAFIA
1. Sleeman K, de Brito M, Etkind S. et al. The escalating global burden of serius health-related suffering: projections to 2060 by world regions, age groups, and health conditions. Lancet Global Health [internet]. 2019 [citado 10 enero 2021], 7: 83-92. Disponible en: http://dx.doi.org/10.1016/ S2214-109X(19)30172-X
2. Organización Mundial de la Salud, Ginebra 2018 http://www.who.int/mediacentre/factsheets/fs402/en/
3. Connors Stephen, ed. By Global Atlas of Paliative Care 2ª ed. London UK, 2020 www.thewhpca.org
4. Pastrana T, De Lima L, Sánchez-Cárdenas M, Van Steijn D, Garralda E, Pons JJ, Centeno C (2021). Atlas de Cuidados Paliativos en Latinoamérica 2020. Houston: IAHPC Press.
5. Acuerdo por el que se declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, publicado en el Diario Oficial de la Federación el 14 de diciembre de 2016.
6. Cuidar cuando no es posible curar, Human Rights Watch. Octubre de 2014.
7. Consejo de Salubridad General. Grupo Terapéutico de los Cuidados Paliativos del Libro de Medicamentos del Compendio Nacional de Insumos para la Salud. Ciudad de México, 29 de septiembre de 2020.
8. González C., Méndez J., Romero I., Bustamante J., Castro R., et al., "Cuidados Paliativos en México". Revista Médica del Hospital General de México, Vol. 75, Núm. 3, julio 2012; páginas 173-179.
CAPÍTULO II
MARCO JURÍDICO DE LOS CUIDADOS PALIATIVOS PEDIÁTRICOS
El derecho a recibir atención paliativa está reconocido de manera implícita en el texto constitucional, conjuntamente, encuentra su fundamento en principios y derechos contemplados en el marco normativo nacional e internacional.
La atención paliativa es un derecho humano que sostiene su existencia principalmente en la dignidad humana; en el derecho a la protección de la salud y a la integridad personal y en la protección contra tratos degradantes e inhumanos.
La OMS y el Fondo Internacional de Emergencia de las Naciones Unidas para la Infancia (UNICEF), definen los cuidados paliativos pediátricos como el cuidado activo y total del cuerpo, mente y espíritu del niño con enfermedad que amenaza y/o limita su vida; estos cuidados deben:
· Comenzar desde el momento del diagnóstico junto con el tratamiento curativo, si éste existe;
· Incluir todos los cuidados de confort hacia el paciente;
· Valorar y realizar el tratamiento escalonado del dolor y otros síntomas molestos;
· Incluir un contacto temprano con el niño y la familia;
· Brindarse independientemente del pronóstico a corto plazo;
· Realizarse de preferencia mediante un equipo multidisciplinario;
· Incluir al niño y la familia en la toma de decisiones;
· Usar los recursos disponibles en la comunidad, y
· Ofrecerse en todos los escenarios de atención: hospitalario, ambulatorio, domiciliario, y seguimiento en el duelo.
Por la naturaleza de la población de niños, niñas y adolescentes se hace necesario proponer una Guía específica que la atienda promoviendo el principio del interés superior del menor. En este contexto, los esquemas de manejo integral de cuidados paliativos en el paciente pediátrico, así como los procesos señalados en el presente documento, son obligatorios para los integrantes del Sistema Nacional de Salud.
Dentro de las disposiciones jurídicas que sustentan la atención paliativa en nuestro orden jurídico nacional, se encuentran:
· Las fracciones II y XXVII Bis del artículo 3o. de la Ley General de Salud, conforme las cuales, la atención médica y el tratamiento integral del dolor son consideradas materia de salubridad general;
· La fracción IV del artículo 33 de la Ley General de Salud determina que las actividades de atención médica paliativas incluyen el cuidado integral para preservar la calidad de vida del paciente, a través de la prevención, tratamiento y control del dolor, y otros síntomas físicos y emocionales por parte de un equipo profesional multidisciplinario;
· Título Octavo Bis, De los Cuidados Paliativos a los Enfermos en Situación Terminal, de la Ley General de Salud;
· Capítulo VIII Bis Disposiciones para la Prestación de Servicios de Cuidados Paliativos, del Reglamento de la Ley General de Salud en Materia de Prestación de Servicios de Atención Médica;
· Norma Oficial Mexicana NOM-011-SSA3-2014, Criterios para la atención de enfermos en situación terminal a través de cuidados paliativos;
· El Acuerdo por el que el Consejo de Salubridad General declara la Obligatoriedad de los Esquemas de Manejo Integral de Cuidados Paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos, publicada en el Diario Oficial de la Federación el 26 de diciembre de 2014;
· El Acuerdo por el que se declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, publicado el 14 de diciembre de 2016 en el Diario Oficial de la Federación, y
· Capítulo Noveno Del Derecho a la Protección de la Salud y a la Seguridad Social, del Título Segundo De los Derechos de Niñas, Niños y Adolescentes, de la Ley General de los Derechos de Niñas, Niños y Adolescentes.
Cabe destacar que, desde 2011 se incorporó el principio del interés superior de la niñez en el artículo 4o. de la Constitución Política de los Estados Unidos Mexicanos, al especificar que: en todas las decisiones y actuaciones del Estado se velará y cumplirá con el principio del interés superior de la niñez, garantizando de manera plena sus derechos. Los niños y las niñas tienen derecho a la satisfacción de sus necesidades de alimentación, salud, educación y sano esparcimiento para su desarrollo integral. Este principio deberá guiar el diseño, ejecución, seguimiento y evaluación de las políticas públicas dirigidas a la niñez.
La Ley General de los Derechos de Niñas, Niños y Adolescentes, reconoce principalmente su carácter de titulares de derechos, prevé que el interés superior de la niñez deberá ser considerado de manera primordial, que tienen derecho a ser informados sobre sus derechos e insta a considerar la opinión y preferencia de las niñas, niños y adolescentes para la toma de decisiones que les concierne de manera directa conforme a su edad, desarrollo evolutivo, cognoscitivo y madurez.
Estos cuidados permiten que durante el avance de la enfermedad se mitigue el dolor, el sufrimiento y se atiendan aspectos psicológicos, sociales y espirituales para preservar en todo momento la dignidad del paciente y su calidad de vida, esto en virtud de que "la medicina no solo debe estar dirigida a salvar la vida de los pacientes, sino que también busca mejorar la calidad de vida de los mismos" (7) entendiendo además que, la medicina paliativa no excluye la atención curativa.
En 2014, en la que fue la primera resolución de ámbito mundial sobre cuidados paliativos (resolución 67.19 de la Asamblea Mundial de la Salud) se instó a la OMS y a sus Estados miembros a mejorar el acceso a los cuidados paliativos como componente central de los sistemas de salud, haciendo hincapié en la atención primaria y la atención comunitaria y domiciliaria. (7)
El tratamiento de dolor como un derecho humano, fue aprobado en la Asamblea Mundial de la Salud 2005 WHA 58-22 y establecido en 2010, también valorándose así en la Carta de Montreal. De tal manera que, al ser parte del cuidado paliativo, éste ha sido reconocido y ratificado como derecho humano por la OMS, Carta de Praga, 2014. (WHA 67-19).
Los tratados internacionales en relación con el acceso a cuidados paliativos que México ha suscrito y tienen carácter vinculante incluyen:
· Artículo 25 de la Declaración Universal de los Derechos Humanos;
· Principios II y IV de la Declaración de los Derechos del Niño;
· Artículo 12 del Pacto Internacional de Derechos Económicos, Sociales y Culturales;
· Artículo 26 de la Convención Americana sobre Derechos Humanos;
· Artículo 10 del Protocolo Adicional a la Convención Americana sobre Derechos Humanos en Materia de Derechos Económicos, Sociales y Culturales, "Protocolo de San Salvador";
· Artículo 24 de la Convención sobre los Derechos del Niño, y
· Artículo 12 de la Convención sobre la Eliminación de todas las Formas de Discriminación contra la Mujer.
Bajo este panorama, la implementación de los cuidados paliativos en pediatría es la estrategia adecuada para atender el sufrimiento con un enfoque centrado en el paciente y su familia, promoviendo la calidad de vida y considerando la muerte como un proceso natural.
El respeto a la autonomía del paciente pediátrico implica comprensión de su situación, la intención de las intervenciones y la implicación de la toma de decisiones en su calidad de vida; así como asegurar su capacidad para expresar sus ideas y preferencias.
El menor tiene derecho a elegir en función del desarrollo de sus capacidades, por lo que se reconoce un proceso de adquisición de autonomía progresiva vinculada con su desarrollo.
Ante la incapacidad legal de los niños y las niñas, las decisiones deberán ser consensuadas y autorizadas por los padres o tutor legal, a falta de ellos, se podrá solicitar a un juez, de acuerdo con las disposiciones civiles aplicables, atendiendo siempre al interés superior del menor. El adolescente deberá ser considerado para la toma de decisiones y dar consentimiento en función de su madurez y competencia.
En todos los casos existe la obligación de los padres, tutores y personal de salud de informar y explicar al paciente en términos claros acorde a su desarrollo la información respecto del tratamiento que recibirá y a considerar su asentimiento, opinión y preferencia sobre los procedimientos diagnósticos y/o terapéuticos, tomando en cuenta su edad, desarrollo evolutivo, cognoscitivo y madurez.
El reto para el personal de salud es poder ofrecer al paciente pediátrico y su familia, equilibrio entre las diferentes opciones terapéuticas posibles a lo largo de la evolución de la enfermedad, el impacto en calidad de vida del paciente y las preferencias del menor y su familia. De igual manera, valorar de forma progresiva durante la trayectoria de la enfermedad las circunstancias y escenarios de atención para facilitar la toma de decisiones informadas y consensuadas, así como vigilar la seguridad en su atención, evitando situaciones de riesgo que incurran en abandono, futilidad u obstinación terapéutica.
Todas las acciones realizadas en el contexto de atención paliativa deberán ser plasmadas por escrito en el expediente clínico conforme a la Norma Oficial Mexicana NOM-004-SSA3-2012, del Expediente Clínico.
BIBLIOGRAFÍA
1. Ley General de Salud. Última reforma publicada en el Diario Oficial de la Federación. Febrero 7 de 2022. https://www.diputados.gob.mx/LeyesBiblio/pdf/LGS.pdf
2. Reglamento de la Ley General de Salud en Materia de Prestación de Servicios de Servicios de Atención Médica. Última reforma publicada en el Diario Oficial de la Federación el 17 de julio de 2018. https://www.diputados.gob.mx/LeyesBiblio/regley/Reg_LGS_MPSAM_170718.pdf
3. Norma Oficial Mexicana NOM-011-SSA3-2014, Criterios para la atención de enfermos en situación terminal a través de cuidados paliativos. http://www.dof.gob.mx/nota_detalle.php?codigo=5375019&fecha=09/12/2014
4. Acuerdo por el que el Consejo de Salubridad General; declara la Obligatoriedad de los Esquemas de Manejo Integral de Cuidados Paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos, publicado en el Diario Oficial de la Federación el 26 de diciembre de 2014, http://www.dof.gob.mx/nota_detalle.php?codigo=5377407&fecha=26/12/2014
5. Acuerdo por el que se declara la obligatoriedad de los esquemas manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, publicado en el Diario Oficial de la Federación el 14 de diciembre de 2016. http://www.csg.gob.mx/descargas/pdf/index/slider/Acuerdo_manejo_cuidados_paliativos_pediatricos.pdf
6. Ley General de los Derechos de Niños, Niñas y Adolescentes, consultada el 05-08-2021, pp. 38-43.
https://www.cndh.org.mx/sites/default/files/documentos/2021-01/Ley_GDNNA.pdf
7. Resolución 67.19 Asamblea Mundial de Salud. Fortalecimiento de los Cuidados Paliativos Como Parte del Tratamiento Integral a lo Largo de la Vida, novena sesión plenaria, 24 de mayo de 2014, comisión B, tercer informe. Internet. Consultado el 05-08-2021. https://apps.who.int/gb/ebwha/pdf_files/WHA67-REC1/A67_2014_REC1-sp.pdf
CAPÍTULO III
LA ATENCIÓN PALIATIVA PEDIÁTRICA
3.1 DEFINICIÓN DE CUIDADOS PALIATIVOS PEDIÁTRICOS
Cuidados paliativos pediátricos son aquellos que previenen, identifican y tratan el sufrimiento en los niños con enfermedades crónicas, progresivas y avanzadas, en sus familias y en los equipos que los atienden. Son adecuados en cualquier etapa de la enfermedad y ofrecen más beneficios cuando se proporcionan tempranamente junto con otros tratamientos dirigidos a curar o controlar la enfermedad de base.
No deben limitarse exclusivamente a los últimos días de vida sino aplicarse progresivamente a medida que avanza la enfermedad y en función de las necesidades de pacientes y familia con un mayor enfoque en aquellas enfermedades que no responden a tratamiento curativo, en cuyo caso es ideal su instrumentación desde el diagnóstico de la enfermedad.
La definición de cuidados paliativos de la OMS, adaptada para pediatría, dice que éstos constituyen "un enfoque que mejora la calidad de vida de los pacientes y familias que afrontan una enfermedad que amenaza la vida de un niño, a través de la prevención y alivio del sufrimiento". Para ello se requiere de "la identificación temprana, la evaluación precisa, y el tratamiento adecuado del dolor y otros problemas físicos, psicosociales, y espirituales". (1)
En la actualidad, los avances en el desarrollo de nuevos tratamientos y los abordajes técnicos hacen posible que algunos niños con enfermedades graves desde la etapa neonatal y pediátrica vivan más tiempo, lo que demuestra que mejora la tasa de supervivencia. Disminuyendo de manera importante la mortalidad, con excepción de aquellas enfermedades que son incurables desde su diagnóstico, teniendo un pronóstico extremadamente malo para la vida; pero que pueden sobre vivir por tiempo prolongado con tratamientos que controlan las exacerbaciones, manteniendo una buena calidad de vida y permitiendo la participación en actividades de la vida diaria.
Es difícil identificar el punto en donde el tratamiento se hace exclusivamente paliativo y el principal reto para los médicos y el equipo multidisciplinario que debe de proporcionar este tipo de tratamiento.
Es importante destacar que el grupo de lactantes menores de 1 año representa un tercio de los pacientes con enfermedades limitantes para la vida, donde se concentran patologías como: cardiopatías, daño pulmonar y daño neurológico. (2)
En este grupo es donde la toma de decisiones resulta más difícil porque la evolución de la enfermedad puede presentar una amplia variabilidad. (3)
3.2 HISTORIA DE LOS CUIDADOS PALIATIVOS PEDIÁTRICOS
La OMS definió en 1990 los Cuidados Paliativos (CP) como: el "cuidado integral" de los pacientes cuya enfermedad no responde al tratamiento curativo. Su meta era lograr la mejor calidad de vida posible en los pacientes y en sus familias. En ese entonces, se consideró hacer una distinción entre intervenciones curativas y paliativas, reservando la paliación a un estado de terminalidad.
Lo anterior derivó en dificultad para la toma de decisiones respecto a la transición, dada la exclusión entre los dos tipos de intervenciones terapéuticas. Como alternativa en 1993 el Children 's Hospice International introdujo un nuevo concepto en los CP: Administrar tratamiento curativo y paliativo simultáneamente ajustando el grado de intervención a la respuesta médica que el paciente iba presentando, facilitando junto al tratamiento con finalidad curativa, la terapia de apoyo necesaria para poder sobre enfrentar lo mejor posible la evolución y desenlace en caso de ser letal. Los cuidados paliativos no serían por tanto excluyentes como en un principio se percibió.
En 1998 la OMS siguió insistiendo en que la meta principal de los Cuidados Paliativos Pediátricos (CPP), era lograr la máxima calidad de vida en el paciente y en su familia, independiente de la fase de la enfermedad. Consideró imprescindible el control del dolor y de los síntomas acompañantes, ocasionados no sólo por la enfermedad en sí misma, sino también por los problemas psicológicos o sociales presentes. Desde entonces, recomienda administrar tratamiento curativo y terapias complementarias necesarias para un tratamiento holístico del niño y de su familia. Enfatizando que los CPP deberían comenzar desde que se diagnostica una enfermedad grave con alto riesgo de muerte y que se debería proseguir con ellos, independientemente de que el niño reciba o no, tratamiento dirigido a la curación.
De forma similar, la Academia Americana de Pediatría, en el año 2000, propuso un modelo integral de CPP, que se iniciarían en el momento del diagnóstico y continuarían a lo largo de la enfermedad, con independencia del resultado.
Tradicionalmente el paciente que se incluía en los programas de CP era el paciente en fase terminal definido como aquel que presentaba estas características:
· Presencia de una enfermedad avanzada, progresiva e incurable.
· Falta de posibilidades razonables de respuesta al tratamiento específico.
· Presencia de numerosos problemas o síntomas intensos, múltiples, multifactoriales y cambiantes. Gran impacto emocional en paciente, familia y equipo terapéutico, muy relacionado con la presencia, explícita o no, de la muerte.
· Pronóstico de vida inferior a 6 meses.
Sin embargo, esta definición dejaba fuera a muchos pacientes que pueden beneficiarse de recibir un manejo integral dentro de un programa de CPP, por ello la insistencia en la actualidad de incluir los pacientes desde el diagnóstico de una enfermedad ya sea amenazante o limitante para la vida.
3.3 DEFINICIONES DE IMPORTANCIA PARA EL TEMA
Enfermedades amenazantes para la vida (EAV): Definidas como aquellas en las cuales existe el riesgo de morir. Si bien es un término corriente, se debe reconocer que el sólo hecho de padecer una EAV no define la necesidad de cuidados paliativos. Para cada niño ésta dependerá del desarrollo particular de la EAV y del contexto familiar y social. Por tanto, esta categorización resulta de poca ayuda a la hora de planificar acciones sanitarias, a pesar de que la Organización Mundial de la Salud recomiende el abordaje multidisciplinar desde el diagnóstico de la enfermedad.
Enfermedad crónica compleja: incluye a niños médicamente complejos o niños con patología crónica compleja. Los cuales tienen alguna condición médica que puede esperarse razonablemente que dure al menos 12 meses (a menos que se produzca el fallecimiento) e involucre a diferentes sistemas o a un solo sistema, pero lo suficientemente grave como para requerir atención pediátrica especializada y probablemente, un cierto periodo de hospitalización en un centro de atención terciaria.
Hace referencia, al paciente portador de una enfermedad de larga evolución (años) que finalmente puede ser letal. En su evolución puede sufrir varios episodios agudos, que no tratados conducen a la muerte, pero que en el mejor de los casos una vez superados pueden dejar al paciente cada vez más cerca del final de su vida. Estos episodios son potencialmente terminales. (2,4)
Enfermedad Limitante para la Vida en etapa inicial: se trata de una patología que, no tiene posibilidades razonables de curación, es progresiva y se prevé que ocasionará una muerte prematura, sin embargo, a pesar del pronóstico sombrío de la enfermedad a mediano y largo plazo, el paciente aún se encuentra en buenas condiciones médicas generales, con participación en actividades de la vida diaria y adecuada funcionalidad (3,4).
Enfermedad Limitante para la Vida en etapa Avanzada: Enfermedad incurable, progresiva, con un pronóstico vital limitado, que se encuentra con gran deterioro físico, funcional, emocional del paciente y los cuidadores, ocasionando incapacidad para realizar actividades de la vida diaria con empeoramiento franco de la calidad de vida e incremento en la dependencia de sus cuidadores.
· "No tiene posibilidad razonable de cura": posibilidad menor a 50% de curarse; y
· Muerte prematura: morir antes de los 30 años cumplidos. (5)
Enfermedad Terminal: Se refiere a una enfermedad letal. Este término debería aplicarse solo a aquellos enfermos en quienes la experiencia indica que podrían morir en un plazo relativamente corto de tiempo, medido en días, semanas o meses. Cumpliendo criterios específicos según la enfermedad.
Etapa Preagónica: Etapa previa a la agonía que puede considerarse según la escala de Nova (consta de cinco ítems, los criterios utilizados en la escala son: estado mental, incontinencia, movilidad, nutrición y actividad) a menor puntuación, mayor riesgo de muerte.
Etapa Agónica: Implica la presencia probable de la muerte. Dicha etapa abarca desde las últimas siete a cero horas de vida antes de la muerte.
Ciertas condiciones clínicas indican deterioro severo de los órganos por lo que la muerte podría esperarse en el transcurso de horas. Según la escala de Mentem (incluye criterios objetivos para realizar el diagnóstico de agonía) con más de 4 puntos el paciente entra en etapa agónica.
3.4 CATEGORÍAS DE ENFERMEDADES LIMITANTES PARA LA VIDA Y AMENAZANTES PARA LA VIDA
A continuación, se enumera las cuatro categorías en las que pueden agruparse las patologías susceptibles de recibir cuidados paliativos. El diagnóstico es solo parte del proceso, el espectro de las enfermedades, la severidad de la enfermedad, las complicaciones subsecuentes y las necesidades del paciente y su familia deben de considerarse siempre.
Grupo 1.- Enfermedades amenazantes para la vida, para las cuales el tratamiento curativo es posible, pero puede fracasar. Ejemplo: el cáncer, algunas insuficiencias orgánicas susceptibles del trasplante. Grupo 2.- Enfermedades donde la muerte prematura es inevitable, los tratamientos intensivos pueden prolongar la calidad de vida y permitir participar en actividades de la vida diaria. Ejemplo: fibrosis quística, distrofia muscular.
Grupo 3.- Enfermedades progresivas sin opciones de tratamiento curativo, donde el tratamiento es exclusivamente paliativo y puede proporcionarse durante varios años. Ejemplo: Mucopolisacaridosis.
Grupo 4.- Enfermedades irreversibles, pero no progresivas, que causa severas discapacidades haciendo al paciente más susceptible a complicaciones médicas y provocando la muerte prematura. Ejemplo: parálisis cerebral infantil. (6,7)
3.5 GENERALIDADES DE LA ATENCIÓN PALIATIVA PEDIÁTRICA
El éxito de un equipo de cuidados paliativos pediátricos (CPP) radica en su capacidad para detectar lo bastante oportuno los síntomas y situaciones emocionales y sociales que rodean al paciente que cursa con una enfermedad amenazante o una enfermedad limitante para la vida, principalmente en el final de esta, esto se logra a través de una evaluación integral, sistemática y dinámica del menor y su entorno.
Permanecer asintomático o con los menores síntomas posibles, vivir en el domicilio, mantener la escolarización y las relaciones con los seres queridos, son tan solo algunos de los objetivos que suelen ir dirigidos a respetar el interés superior del menor, o lo que es lo mismo: tratar al niño como persona y priorizar sus intereses a los de los profesionales o la familia.
Para lograr el objetivo anterior, es menester poseer diversas habilidades y capacidades como: escuchar, reconocer, analizar, comunicación eficiente y habilidad para ofrecer recursos de apoyo. El tener una evaluación impecable, resulta un abordaje integral por parte del equipo interdisciplinar tanto del enfermo, de la familia y cuidadores principales.
Los principales objetivos en la Atención Paliativa Pediátrica son:
1. Comunicación y relación entre el personal de la salud, el niño y su familia;
2. Historia Clínica Pediátrica para recabar toda la información con respecto a la evolución de la enfermedad, los tratamientos previamente recibidos, la sintomatología que presenta el paciente con una semiología estricta y en caso de que el niño no tenga la capacidad de comunicación por su edad, o por su limitación secundaria a discapacidad neurológica, interrogar de manera exhaustiva a los padres o cuidadores principales;
3. Clasificar y estadificar la enfermedad;
· Enfermedad amenazante para la vida;
· Enfermedad limitante para la vida. (Antes llamada condición clínica compleja);
· Enfermedad limitante para la vida en etapa incurable inicial;
· Enfermedad limitante para la vida en etapa incurable avanzada; y
· Enfermedad terminal en etapa preagónica o agónica.
4. Detectar necesidades: Físicas, psíquicas, funcionales, familiares, sociales y espirituales;
5. Tener prioridad en los problemas que presenta el paciente;
6. Tener un plan de acción y fijar metas terapéuticas;
7. Seguimiento por la consulta externa, la visita domiciliaria, telemedicina y centro de atención telefónica para la monitorización constante; y
8. Evaluar los resultados, para continuar con el control de la sintomatología o realizar ajustes al tratamiento.
Los Cuidados Paliativos Pediátricos consisten en la atención activa de las necesidades físicas, psicológicas, sociales y espirituales del niño, niña o adolescente con enfermedad incurable y apoyo a su familia y/o cuidador primario. Se inician en el momento del diagnóstico de una enfermedad amenazante para la vida, continúan durante toda la enfermedad del niño, niña o adolescente, independientemente de que reciba tratamiento específico para su enfermedad, y se mantienen durante el proceso de duelo, apoyo a la familia. Tienen como objetivo velar por el mejor interés del niño, niña o adolescente y proteger sus derechos.(8) Los cuidados paliativos pediátricos generan las condiciones necesarias para permitir la creación de una atmósfera de integridad con la finalidad de curación o de bienestar hasta el fin, traducido este último en calidad de vida en el trayecto de cualquiera de estos dos caminos y donde se incluye a la familia.
La atención paliativa se basa en la administración de tratamientos farmacológicos, planificación de estrategias terapéuticas incluyendo rehabilitación física, cuidados de enfermería, la atención psicológica, espiritual y otras terapias. Incluye la atención de las necesidades sociales, educativas y espirituales de forma adaptada a las necesidades de cada paciente en cada momento de su vida. (9)
Los cuidados paliativos comienzan en el diagnóstico de la enfermedad amenazante o limitante para la vida mediante el enfoque paliativo. Con el enfoque paliativo, el pediatra debe aceptar la irreversibilidad del proceso del paciente y la posibilidad de fallecimiento como acontecimiento natural, sin privar al paciente de lo que necesita para estar bien.(10) El enfoque paliativo debe ser ofrecido por todos los médicos pediatras y sub especialistas involucrados en la atención del niño, niña y adolescente. Algunos especialistas pediátricos atienden a un mayor número de pacientes al final de su vida, al ejercer su trabajo en especialidades como la Neonatología, Cuidados Intensivos, Oncología o Neurología. En estas situaciones, los cuidados paliativos generales permiten optimizar el control de síntomas, atender a la familia para mejorar la toma de decisiones y facilitar su adaptación al duelo.
Los cuidados paliativos específicos son los ofrecidos por unidades con formación específica y dedicación exclusiva a los cuidados paliativos. Consisten, además de lo anterior, en el control de síntomas difíciles, en la colaboración en la toma de decisiones complejas teniendo en cuenta el interés superior del niño, sus necesidades y problemas, y en el acompañamiento a la familia durante la vida y tras la muerte del niño, niña o adolescente. (11)
3.6 ORGANIZACIÓN DE LA ATENCIÓN PALIATIVA
El establecimiento y desarrollo de servicios de cuidados paliativos pediátricos es indispensable con base en lo dispuesto por la ley y dada la necesidad de hacer valer un derecho moral y humano para la atención de los pacientes pediátricos con una enfermedad limitante para la vida y para su familia.
La implementación de estos servicios deberá estar conformada por personal capacitado e interesado en esta área, en un espacio físico adecuado y con los recursos materiales suficientes.
Implementar un plan de CPP adecuado requiere la confluencia de múltiples factores. Debe realizarse con base en un plan de metas establecido en conjunto con el paciente (si su edad lo permite), la familia y el equipo médico encargado, tanto para fines curativos como paliativos. Una intervención exitosa requiere de un equipo interdisciplinario, puesto que un solo profesional únicamente abarcará un área de atención y no bastará para cubrir las necesidades del niño y su familia.(12)
Además, se requiere que el equipo médico tenga una relación de confianza con el niño y la familia, para así abrir canales de comunicación efectivos, sin lo cual una intervención exitosa no es posible. Este es quizás uno de los pilares más importantes del CPP, puesto que aspectos culturales y sociales, sumados a un desconocimiento de esta temática, sus alcances y sus métodos, en ocasiones lleva a que los padres de pacientes con enfermedades susceptibles de CPP se nieguen a recibir dicho manejo (13,14)
El deseo del paciente, la edad del niño y el estado de salud general son puntos fundamentales para considerar con respecto al tratamiento, las pruebas diagnósticas y otros procedimientos terapéuticos que pudieran realizarse. La información debe ser clara y suficiente para el niño, niña o adolescente y su familia, respetando las creencias e ideologías que puedan interferir con la implementación del manejo paliativo.
Si los deseos de la familia y el niño, niña o adolescente son acordes a la implementación de CPP, el equipo médico debe dar apoyo a la familia incluso después del deceso del niño niña o adolescente, para asegurar que esta realice un duelo adecuado. Este manejo integral, el cual incluye aspectos físicos, sociales y espirituales, explica la necesidad de tener un equipo estructurado e interdisciplinario que debe incluir profesionales que satisfagan cada una de las necesidades que el paciente y su familia puedan presentar en cada campo. (15)
Respecto a los criterios de inclusión de un paciente a la atención paliativa pediátrica, como se mencionó previamente, deben ser atendidos todos aquellos que se encuentren con enfermedades limitantes para la vida y aquellos con enfermedades amenazantes para la vida cuya severidad, progresión o falta de respuesta al tratamiento los hace susceptibles de recibir atención paliativa.
Este tipo de servicio deberá estar implementado en los tres niveles de atención médica, priorizando el primer nivel, favoreciendo la atención a domicilio, mediante un sistema eficiente de referencia y contra referencia. (25, 26)
Nivel primario de cuidados paliativos pediátricos. Está dirigido a niños con enfermedades relativamente frecuentes y menos graves, donde los principios de los cuidados paliativos pediátricos son llevados a cabo por todos los profesionales sanitarios.
Segundo nivel de cuidados paliativos pediátricos. Dirigido a casos más complejos, que requieren la intervención de personal de atención primaria y hospitalario, que, aunque no se dedica exclusivamente a los servicios de cuidados paliativos pediátricos, posee habilidades específicas determinadas por estándares reconocidos.
Tercer nivel o nivel especializado de cuidados paliativos pediátricos. Dirigido a enfermedades y situaciones muy complejas que requieren cuidados continuados por profesionales que trabajan de manera exclusiva en el sector de los cuidados paliativos pediátricos; miembros de un equipo interdisciplinario especializado.
Para la organización de servicios específicos de cuidados paliativos pediátricos deben considerarse dos entornos potenciales de cuidados: el domicilio y el medio hospitalario.
3.7 ATENCIÓN DOMICILIARIA
Los cuidados centrados en la familia, proporcionados en el domicilio, son el objetivo de los cuidados paliativos pediátricos; es lo que la mayoría de las familias quieren y tienen un impacto positivo en la calidad de vida del niño, niña o adolescente. (16) Las ventajas de la atención domiciliaria son muchas. La atención a domicilio disminuye enormemente la sensación de miedo, aislamiento y desamparo. Permite al niño, niña o adolescente, participar en las actividades de la familia y le ofrece importantes oportunidades de comunicación y socialización. También permite a otros miembros de la familia compartir las responsabilidades de los cuidados. Sin embargo, hay que considerar que, para algunos niños o familias, la atención a domicilio puede que no sea la mejor opción.
La atención domiciliaria requiere la implicación de un equipo multidisciplinar que apoye a la familia. Tiene que haber accesibilidad a un experto en cuidados paliativos pediátricos 24 horas al día, a programas de atención hospitalaria inmediata si fuera necesario. Es esencial que exista un "profesional clave" para coordinar los cuidados del niño con la familia, con el personal de atención primaria, con el hospital de segundo nivel y con los centros especializados.(17,18)
Existen dos principales modelos asistenciales que proporcionan cuidados en el domicilio son:
Cuidados dependientes de un hospital. Cuando un equipo perteneciente a un centro terciario pediátrico continúa atendiendo al niño tras el alta hospitalaria. El equipo con frecuencia está compuesto por enfermeras especializadas, un médico especialista, un médico residente, un psicólogo, un especialista en bioética clínica y personal administrativo. Todos ellos trabajan estrechamente con otros equipos del hospital, incluyendo la unidad de dolor crónico, equipos de enfermedades específicas, la unidad de cuidados intensivos (UCIN/UCIP) (la mayoría de los niños mueren durante el primer año de vida), otros hospitales, hospices, médicos de familia, servicios sanitarios locales de atención primaria y colegios. (19)
Cuidados dependientes de la atención primaria. Cuando un equipo de atención primaria cuida del paciente y la familia. Esta opción permite al niño llevar una vida familiar y social normal; ofrece la posibilidad de una amplia cobertura geográfica y la prestación de servicios multidisciplinares. Sin embargo, esta opción puede sufrir las consecuencias de la discontinuidad del tratamiento hospitalario, unos recursos insuficientes y unas habilidades inadecuadas. El éxito de este modelo de cuidados depende de la comunicación y la interactuación entre los servicios hospitalarios y los comunitarios, de la formación en cuidados paliativos pediátricos del personal de atención primaria, del entrenamiento de la familia para acudir a los servicios de la comunidad y de la disponibilidad de suministros y equipos médicos. Los equipos de atención primaria deben poder llamar a un equipo de cuidados paliativos pediátricos especializado y experimentado cuando lo necesiten. (20)
Los cuidados a domicilio no siempre son posibles; en casos especialmente complejos, por motivos de agotamiento, estrés emocional o razones logísticas o de organización, son necesarias soluciones transitorias. Estas soluciones para niños con enfermedades que limitan o amenazan su vida pueden prestarse principalmente en tres entornos de cuidados; unidades hospitalarias de segundo y tercer nivel de atención, unidades de urgencias y cuidados intensivos y, más recientemente, en unidades de hospitalización de cuidados paliativos pediátricos. (21)
Unidades Hospitalarias de segundo y tercer nivel: estos tienen la ventaja de que se dedican al manejo de casos raros y complejos en un entorno adecuado a las necesidades del niño y la familia. Al cubrir amplias áreas geográficas, tienen el suficiente número de pacientes para desarrollar la experiencia y los recursos específicos de manera que sean económicamente viables. Tienen la desventaja de separar al niño de su hogar.
Salas de urgencias o unidad de cuidados intensivos en hospitales: por su naturaleza, misión y organización éste no es el lugar ideal para proporcionar cuidados paliativos a niños sin embargo en la actualidad estas áreas no deben representar un límite para la administración de cuidados paliativos
pediátricos ya que se ha demostrado que los niños con enfermedades crónicas que mueren en estas áreas tienen más probabilidades de haber recibido ventilación mecánica y hospitalización durante períodos más prolongados antes de su muerte. (22)
Unidades de hospitalización de cuidados paliativos pediátricos: estos "hospices" dentro de un hospital ofrecen cuidados paliativos especializados desde el diagnóstico, a lo largo de los diferentes periodos de la enfermedad que avanza e incluyendo las últimas fases de la enfermedad.
Debido a que cada uno de los modelos organizativos mencionados anteriormente tiene limitaciones, la mayoría de los actuales programas de cuidados paliativos pediátricos adoptan una combinación de las soluciones descritas. Son módulos dentro de una red única, en la que varias organizaciones de salud pública trabajan con otras para prestar cuidados continuos, de forma flexible, a lo largo del curso de la enfermedad. Las familias pueden acceder a los diferentes entornos de cuidados dentro de la red de acuerdo a las necesidades del niño y la familia. Pueden facilitarse distintas opciones de cuidados limitadas en el tiempo, dependiendo de la enfermedad del niño y de la situación clínica en un momento dado. El equipo específico de cuidados paliativos pediátricos actúa como referente para todos los profesionales dentro de la red; este modelo de atención sanitaria ofrece un alto nivel de competencia y un gran apoyo para la familia. Varios estudios internacionales reconocen que las redes específicas de cuidados paliativos pediátricos que cubren amplias áreas y que combinan tanto la atención domiciliaria como la hospitalaria ofrecen el modelo de atención sanitaria más efectivo, eficiente y sostenible para los niños con enfermedades incurables y sus familias. (23,24)
BIBLIOGRAFÍA
1. Hui D, De La Cruz M, Mori M, Parsons HA, Kwon JH, Torres-Vigil I, et al. Concepts and definitions for "supportive care," "best supportive care," "palliative care," and "hospice care" in the published literature, dictionaries, and textbooks. Support Care Cancer. marzo de 2013;21(3):659-85.
2. Burke RT, Alverson B. Impact of Children With Medically Complex Conditions. PEDIATRICS. 1 de octubre de 2010;126(4):789-90.
3. Goldhagen J, Fafard M, Komatz K, Eason T, Livingood WC. Community-based pediatric palliative care for health related quality of life, hospital utilization and costs lessons learned from a pilot study. BMC Palliat Care. diciembre de 2016;15(1):73.
4. Hain R, Devins M, Hastings R, Noyes J. Paediatric palliative care: development and pilot study of a Directory' of life-limiting conditions. BMC Palliat Care. diciembre de 2013;12(1):43.
5. Lenton S, Stallard P, Lewis M, Mastroyannopoulou K. Prevalence and morbidity associated with non-malignant, life-threatening conditions in childhood: Lenton et al. Child: Care, Health and Development. septiembre de 2001;27(5):389-98.
6. RUBIO JV, GARCÍA MA. Cuidados paliativos pediátricos. Bol Pediatr. 2012; 52:131-45.
7. Berry JG, Agrawal R, Kuo DZ, Cohen E, Risko W, Hall M, et al. Characteristics of Hospitalizations for Patients Who Use a Structured Clinical Care Program for Children with Medical Complexity. The Journal of Pediatrics. agosto de 2011;159(2):284-90.
8. Jerrell JM, Shuler CO, Tripathi A, Black GB, Park Y-MM. Long-Term Neurodevelopmental Outcomes in Children and Adolescents With Congenital Heart Disease. Prim Care Companion CNS Disord [Internet]. 22 de octubre de 2015 [citado 12 de septiembre de 2021]; Disponible en: http://www.psychiatrist.com/PCC/article/Pages/2015/v17n05/15m01842.aspx
9. ACT (Organization), Royal College of Paediatrics and Child Health. A guide to the development of children's palliative care services: update of a report. Bristol: ACT; 2003.
10. Watson MS. Manual Oxford de cuidados paliativos. Madrid: Aula Médica; 2008.
11. Graham F, Clark D. WHO definition of palliative care. Medicine. Medicine. febrero de 2008;36(2):64-6.
12. Pinto MJV. Ley Orgánica 8/2015, de 22 de julio, de modificación del sistema de protección a la infancia ya la adolescencia [BOE n. o 175, de 23-VII-2015] y Ley 26/2015, de 28 de julio, de modificación del sistema de protección a la infancia ya la adolescencia [BOE. AIS: Ars Iuris Salmanticensis. 2016;4(1):242-5.
13. Caruso Brown AE, Howard SC, Baker JN, Ribeiro RC, Lam CG. Reported Availability and Gaps of Pediatric Palliative Care in Low- and Middle-Income Countries: A Systematic Review of Published Data. Journal of Palliative Medicine. diciembre de 2014;17(12):1369-83.
14. Williams-Reade J, Lamson AL, Knight SM, White MB, Ballard SM, Desai PPP. Paediatric palliative care: a review of needs, obstacles and the future. J Nurs Manag. enero de 2015;23(1):4-14.
15. Johnson L-M, Snaman JM, Cupit MC, Baker JN. End-of-Life Care for Hospitalized Children. Pediatric Clinics of North America. agosto de 2014;61(4):835-54.
16. Unidas N. Convención sobre los Derechos del Niño. 1989;
17. Río JA del. La Ley 41/2002, de 14 de noviembre, básica reguladora de la autonomia del paciente y de los derechos y obligaciones en materia de información y documentación clínica (II). Josefina Alventosa del Río La Ley 41/2002, de 14 de noviembre, básica reguladora de la autonomia del paciente y de los derechos y obligaciones en materia de información y documentación clínica (II) En: Revista Española de Drogodependencias, 2003, Vol 28, no 4. 2003;
18. Bradford N, Herbert A, Mott C, Armfield N, Young J, Smith A. Components and Principles of a Pediatric Palliative Care Consultation: Results of a Delphi Study. Journal of Palliative Medicine. noviembre de 2014;17(11):1206-13.
19. Gade G, Venohr I, Conner D, McGrady K, Beane J, Richardson RH, et al. Impact of an Inpatient Palliative Care Team: A Randomized Controlled Trial. Journal of Palliative Medicine. marzo de 2008;11(2):180-90.
20. Health ID of, Children. A palliative care needs assessment for children. Department of Health and Children; 2005.
21. Hynson JL, Gillis J, Collins JJ, Irving H, Trethewie SJ. The dying child: how is care different? Medical Journal of Australia [Internet]. septiembre de 2003 [citado 12 de septiembre de 2021];179(S6). Disponible en: https://onlinelibrary.wiley.com/doi/abs/10.5694/j.1326-5377.2003.tb05571.x
22. Consortium YHE, others. Independent Review of Palliative Care Services for Children and Young People: Economic Study. Final Report York: York Health Economics Consortium. 2007;
23. Eaton N. Children's community nursing services: models of care delivery. A review of the United Kingdom literature. J Adv Nurs. 2000; 32(1):49-56.
24. Ramnarayan P, Craig F, Petros A, Pierce C. Characteristics of deaths occurring in hospitalised children: changing trends. Journal of Medical Ethics. 2007;33(5):255-60.
25. Secretaría de Salud. Norma Oficial Mexicana. NOM-011-SSA3-2014. Criterios para la atención de enfermos en situación terminal a través de cuidados paliativos. Publicada en el Diario Oficial de la Federación el 9 de diciembre de 2014. http://www.dof.gob.mx. fecha=09/12/2014
26. Julio V, Vacarezza M, Sosa A. Niveles de atención, de prevención y atención primaria de la Salud. Arch. Med Int. 2011;33(1):7-11. http://www.scielo.edu.uy/pdf/ami/v33n1/v33n1a03.
CAPÍTULO IV
MODELOS DE PROVISIÓN DE LA ATENCIÓN PALIATIVA PEDIÁTRICA
4.1 INTRODUCCIÓN
De acuerdo con el Reglamento de la Ley General de Salud, en Materia de Prestación de Servicios de Atención Médica, el objetivo del plan de atención del paciente en cuidados paliativos es el de organizar la prestación de la atención médica para el paciente con enfermedad avanzada, cuando los tratamientos con fines curativos no pueden aportar beneficios en términos de supervivencia ni calidad de vida.
Se pretende mejorar la calidad de vida de los pacientes y de su familia, cuando afrontan los problemas relacionados con una enfermedad potencialmente mortal que deterioran la función y el desempeño; atendiendo los aspectos físicos, emocionales, sociales y espirituales propios y de su entorno, con medidas de promoción, prevención, rehabilitación y cuidado para el control de síntomas, garantizando la continuidad durante el proceso de la enfermedad.
Se fundamenta en los estándares de cobertura, equidad, calidad y humanismo.
Los objetivos generales incluyen proporcionar las mejores condiciones de vida de los enfermos en situación terminal y/o paliativa a sus familias, de manera racional, planificada y eficiente, garantizando los cuidados paliativos según los principios rectores del Sistema Nacional de Salud.
1. Proporcionar atención integral de calidad favoreciendo la integración de la consejería familiar y asesoría telefónica;
2. Facilitar un modelo de trabajo que permita el abordaje interdisciplinar de las necesidades del paciente, así como la coordinación con otros sectores implicados;
3. Fomentar redes integradas de atención en cuidados paliativos basados en la atención por niveles de complejidad adaptada a las necesidades clínicas y preferencias del paciente;
4. Favorecer la toma de decisiones consensuada con el paciente y la familia que afectan el estado de salud en el momento actual y en situaciones futuras;
5. Fomentar la incorporación organizada de la familia, cuidadores y voluntarios en la atención y cuidado de la persona en situación avanzada y terminal;
6. Impulsar la formación continua de recurso humano en cuidados paliativos, apoyar el desarrollo de la investigación en el campo y su divulgación;
7. Asegurar el desarrollo e implementación de estándares para la atención adecuada en cuidados paliativos, que permitan la generación de indicadores de monitoreo y evaluación del plan; y
8. Desarrollo de indicadores de procesos, calidad y resultado en cuidados paliativos con fines de evaluación.
La implementación del plan de atención del paciente en cuidados paliativos se contempla en los tres niveles de atención considerando:
· Educación, capacitación y difusión. Esto a través de programas permanentes a profesionales de la salud y disciplinas afines, así como la elaboración, actualización e implementación de las normas, acuerdos, guías y algoritmos de cuidados paliativos;
· Fomentar la creación de recursos humanos para la atención de cuidados paliativos, necesaria para proporcionar calidad, efectividad y eficiencia; y
· Desarrollar la infraestructura necesaria para la atención de los pacientes en cuidados paliativos.
Asimismo, las funciones fundamentales de los equipos de apoyo en cuidados paliativos son:
· Atención directa de enfermos y familias, apoyo y consulta a otros equipos, formación y coordinación de recursos;
· Evaluación y tratamiento de los síntomas físicos, psicológicos, sociales y espirituales;
· Definir e implementar con los pacientes y familiares los objetivos del plan de cuidados paliativos, y
· Establecer un sistema de referencia y contrarreferencia eficiente.
La aplicación del plan de atención del paciente en cuidados paliativos en los servicios de salud deberá ser escalonada.
Todos los pacientes con enfermedades limitantes para la vida son susceptibles de ser atendidos con criterios de cuidados paliativos. La atención reside en las redes coordinadas de atención médica. Sin embargo, determinadas situaciones, por su complejidad, requerirán de servicios específicos de cuidados paliativos, en el domicilio u hospitalarios.
La intervención de los equipos específicos debe basarse en principios de efectividad y eficiencia, y debe reservarse para la atención de enfermos y situaciones de alta complejidad, promoviendo la capacidad de resolución de los recursos convencionales (mediante la formación, la interconsulta y la atención compartida).
Los pacientes con necesidades de atención paliativa, son personas con una enfermedad limitante para la vida y sus familias, en los que predominan las necesidades relacionadas con la calidad de vida (síntomas físicos, emocionales, impacto social, espiritual), con pronóstico de vida limitado.
A continuación, se citan algunas características que se sugiere considerar para la atención de los pacientes, según nivel de atención.
Atención en primer nivel
· Pacientes con una enfermedad limitante para la vida en estadía avanzada que elija permanecer en su domicilio con familia capaz de brindar atención;
· Recursos específicos: equipos básicos (médico tratante, enfermera) o completos si se dispone de otros profesionales de la salud (psicólogos, odontólogos, nutriólogos fisioterapeutas, trabajadores sociales u otros); e
· Infraestructura: centro de salud (personal adscrito) y dependiendo de la cobertura un centro de atención telefónica disponible las 24 horas.
Actividades:
· Favorecer la atención domiciliaria;
· Mejorar el acceso para la continuidad de la atención;
· Atención al duelo familiar en donde se cuente con personal calificado;
· Contar con un equipo consultor de apoyo con formación en cuidados paliativos, en el segundo nivel de atención y Coordinación entre niveles asistenciales; y
· Referencia y contrarreferencia: un paciente en enfermedad terminal puede pasar de una modalidad a otra y de un nivel de atención primaria al nivel terciario, dependiendo de las necesidades que presente.
Los pacientes pueden ser:
· Captados por equipos de salud;
· Captados por demanda espontánea de los mismos o sus familiares cumpliendo con las condiciones señaladas previamente, para ser atendidos por los equipos de cuidados paliativos existentes; y
· Referidos por unidades de cuidados paliativos hospitalarios o por otro médico.
Las personas con enfermedad avanzada en fase terminal podrán pasar de una modalidad a otra dependiendo de su evolución clínica y los cambios que se den en su entorno.
El mecanismo de referencia y contrarreferencia se empleará para dar seguimiento y continuidad al proceso.
Atención en segundo nivel
· Contar con criterios de intervención de los equipos específicos;
· Factores en relación con el paciente: dificultad en el control sintomático (por ejemplo: disnea, hemoptisis, estado confusional, dolor neuropático o mixto de mal pronóstico, obstrucción intestinal, etc.);
· Escasa respuesta a terapéutica convencional (por ejemplo, a la morfina oral, antieméticos orales) y que requiere tratamiento más complejo (por ejemplo, rotación de opioides u otros);
· Tratamientos especializados (tecnología o complejidad psicosocial). Dificultades de adaptación emocional;
· Factores relacionados a las familias: emocionales, de cuidados o de adaptación a la situación. Riesgo de duelo patológico. Claudicación del cuidador; e
· Implementación de equipos multidisciplinarios, Integrados por personal del área médica, trabajo social, psicología, enfermería entre otros; que funciona como un equipo de consulta dentro del hospital.
Consulta externa.
Se recomienda que la atención domiciliaria se realice en primer y segundo nivel de atención.
La consulta ambulatoria es un recurso óptimo para mejorar la accesibilidad y cobertura del programa, especialmente por las intervenciones tempranas compartidas con otras especialidades. Puede estar a cargo de un equipo hospitalario con interacción con un equipo de apoyo domiciliario.
Atención en tercer nivel
Unidades especializadas en atención de pacientes paliativos de alta complejidad. Se recomienda que la estructura física de la unidad favorezca la privacidad y el bienestar de los pacientes, facilitando el acceso a los familiares. Que la unidad cuente con camas para hospitalización y largas estancias. La función del tercer nivel de atención en cuidados paliativos está dirigida a la investigación clínica, docencia y asistencia.
Actividades:
· Hospitalización de día. Para control de síntomas que ameriten la permanencia del paciente por algunas horas dentro de la unidad hospitalaria;
· Hospitalización para control de síntomas difíciles, urgencias y/o sedación paliativa;
· Favorecer la referencia y contrarreferencia al primer y segundo nivel de atención según amerite el paciente;
· Hospitalización, consejería familiar, consulta externa;
· Cuidado Global: Es considerar al enfermo de manera integral en el plano biopsicosocial (intelectual, social, financiero y espiritual).
Los objetivos fundamentales de la atención paliativa consisten en el alivio del padecimiento evitable y en la adaptación al padecimiento inevitable, con el fin de mejorar la experiencia de la enfermedad progresiva mediante la promoción de la calidad de vida y el bienestar de enfermos y familias. Para lograrlos, es necesario tener presente y considerar:
· Los fundamentos para el cuidado paliativo perinatal;
· La identificación de los candidatos a cuidado paliativo perinatal;
· Las etapas del cuidado paliativo perinatal;
· Los aspectos clínicos del cuidado paliativo perinatal;
· El manejo del dolor en periodo perinatal;
· El manejo de la disnea en el periodo perinatal; y
· El abordaje de la familia en el periodo perinatal.
4.2 MODELO DE PROVISIÓN PARA ATENCIÓN PALIATIVA PERINATAL
"La dignidad personal es el reconocimiento de que somos merecedores de lo mejor." (Walter Riso).
Fundamentos para el cuidado paliativo perinatal. Socialmente la percepción de la nueva vida no comienza al momento del nacimiento sino desde el momento de la percepción de un embarazo. Se generan expectativas y procesos de inclusión social aún antes del nacimiento, de manera que las pérdidas de vidas tempranas son significativas independientemente de la edad gestacional del producto o de los días de vida posterior al nacimiento. También desde el punto de vista legal, la Constitución Política de los Estados Unidos Mexicanos en su artículo 4°, párrafo cuarto establece que toda persona tiene derecho a la protección de la salud. Por lo que se protege la vida desde el momento mismo de la concepción y con ello tenemos la obligación de respetar los derechos humanos y la dignidad de este grupo. (1)
Actualmente, dentro de la mortalidad por debajo de los cinco años de edad, el grupo más afectado es la población neonatal. En 2019 se registraron por parte del INEGI 23,868 defunciones fetales con una tasa de 1.89 por 10,000 habitantes. En el mismo año se registró un total de 14, 246 muertes neonatales, 69% de las cuales ocurrieron en la primera semana de vida, especialmente dentro del día del nacimiento. La mayor parte de la muerte neonatal se considera prevenible y por tanto existe un gran pendiente por parte de la sociedad para lograr la reducción de dichas muertes. Sin embargo, existe un número significativo de muertes fetales y neonatales que presentan patologías incompatibles con la vida a corto y largo plazo o bien, que, tras los esfuerzos terapéuticos iniciales, presentan una evolución desfavorable para la vida. En estos pacientes neonatales y todos aquellos con condiciones amenazantes para la vida, la incorporación del cuidado paliativo oportuno genera el potencial de brindar calidad de vida y sentido de dignidad independientemente del desenlace.
La protección de la vida humana como elemento fundamental ético implica un trato digno. El feto y el neonato tienen capacidad fisiológica para sentir plenamente el dolor ya que además las rutas inhibitorias están inmaduras, por lo que ante la presencia de por lo menos uno de los síntomas fundamentales en el cuidado paliativo este abordaje es indispensable. (2,3) En función del concepto de dolor que se maneja en otras etapas de la vida, en fetos y neonatos se habla de "actividad nociceptiva" con implicaciones importantes para estos seres humanos en todas las esferas de su vida. Las terminaciones nerviosas nociceptivas existen en la piel del neonato en mayor densidad que en la piel adulta y son detectables en el área peri oral desde la semana 7 de gestación; se desarrollan en todo el cuerpo hacia las 20 semanas de gestación. La inmadurez del sistema nervioso, contrario a lo que se pensaba, no atenúa la percepción nociceptiva, la incrementa. El feto y el neonato tienen estructuras anatómicas y funcionales para la percepción de estímulos dolorosos. (4)
Dignidad fetal y neonatal. Desde la perspectiva ontológica, los miembros de la especie humana son dignos independientemente de su condición, méritos o deméritos. La dignidad surge como consecuencia misma de la existencia del ser humano independientemente de la etapa de la vida en que se encuentre, así como de su identidad. (5) El feto y el neonato son integrantes activos de la familia a pesar de su inmadurez y cuando la vida es breve deja huella permanente en su entorno social.
Desde la perspectiva ética la construcción del trato digno requiere que los tomadores de decisiones primarios sean los padres y deben ser integrados en todo el proceso con comunicación asertiva y apoyo integral.
La generación de sufrimiento es multifactorial y con distinto peso específico para cada variable involucrada, por lo que, en el concepto de trato digno, cada caso debe ser analizado cuidadosamente e individualizado.
El vacío legal para el cuidado paliativo perinatal. La legislación emitida hasta el momento en México (Ver Capítulo II de esta Guía) para el cuidado paliativo no hace alusión específica a la población fetal y neonatal, sin embargo, dentro de la generalidad de dichas leyes y normas existe el espacio para el desarrollo del cuidado paliativo perinatal independientemente de que existe esa deuda por parte el Estado mexicano con estos pacientes en el sentido de ser mencionados como tales en el discurso legal y normativo. La recomendación legal más importante para las instituciones que se encuentran ante el reto de desarrollar procesos para el cuidado paliativo perinatal es la elaboración de consentimientos informados apegados a la ley e inclusivos de las circunstancias y características de esta población, así como de la afectación de su calidad de vida.
Equipo integrante del cuidado paliativo perinatal. La parte fundamental en la implementación de un proceso de cuidado paliativo perinatal es asumir la complejidad. Dicha complejidad parte de la base de que normalmente el análisis incluye la circunstancia de dos personas (binomio) con o sin estructura social de apoyo. La toma de decisiones en relación con una de las personas involucradas implica la salud y el bienestar de la otra. El nacimiento es un fenómeno cultural por lo que todos los factores biológicos, médicos, científicos, éticos, sociales, económicos son determinantes de la calidad de vida de madre, feto o persona recién nacida.
Otro elemento importante es el conjunto de variables que construyen la complejidad de cada evento perinatal y por tanto la toma de decisiones se realiza en un espacio significativo de incertidumbre que no es cubierto plenamente por solo la evidencia científica (Tabla 1). Una forma de poder controlar la incertidumbre es plantearse la organización de un cuidado paliativo perinatal en los distintos escenarios posibles.
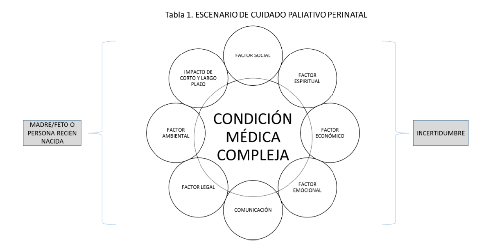
Por esta razón al igual que en otras etapas de la vida, la recomendación es que los procesos de implementación de cuidado paliativo perinatal se integren con un equipo multidisciplinario que genere una auténtica estructura de apoyo en la atención con calidad de vida para paciente y familia. En la Tabla No.2 se realiza una propuesta de estructuración de equipo para atención en cuidado paliativo perinatal.

Construcción de calidad de vida en el periodo perinatal. El objetivo del cuidado paliativo perinatal, al igual que en otras etapas, es la calidad de vida ante una condición amenazante para la vida. Es por ello fundamental definir calidad de vida en esta etapa, sin embargo, no es una tarea fácil al estar hablando de personas que aún no tienen la madurez suficiente para poder expresar su opinión o necesidades. La perspectiva de lo que es calidad de vida entre familiares y personal de salud puede distanciarse enormemente. Discapacidad no equivale a mala calidad de vida en la percepción de muchas familias, pero si para el personal de salud. Mientras que la invasividad y el aislamiento son muy relevantes en la perspectiva de las familias y en menor proporción para el personal de salud. (6) Un referente importante para incluir a la familia de forma adecuada en el proceso de cuidado paliativo es la atención centrada en la familia que hoy se ha vuelto el estándar de calidad de atención neonatal. Sin embargo, este concepto también varía en la literatura médica (7). En esencia es buscar una adecuada interacción de los miembros de la familia del paciente neonatal con el personal involucrado en la atención.
El proceso de atención en cuidado paliativo es un acto médico fundamental que incorpora de forma integral todos aquellos factores o circunstancias que determinan la calidad de vida de la persona recién nacida y su familia a través de un equipo multidisciplinario. Ante la limitación para la comunicación recurrir a escalas de medición puede mejorar la identificación de las necesidades de la persona recién nacida en cuidado paliativo.
En la Tabla 3 se incorporan elementos a evaluar en la construcción de la calidad de vida con algunas sugerencias de escalas de medición que podrían contribuir a una evaluación más objetiva. (8-14)
Tabla 3.
| Dolor | Neonatal Infant Pain Scale, Neonatal Pain Agitation and Sedation Scale, CRIES |
| Patrón neuroconductual | Neonatal Behavioral Assessment Scale, Neonatal Care Unit Network Neurobehavioral Scale, NIDCAP |
| Integridad de la piel | Neonatal Skin Condition Score |
| Calidad del sueño | Peds QL Infant Scale |
| Tolerancia alimentaria | LATCH |
| Disnea | Silverman |
| Estrés ambiental | Medición de ruido |
| Invasividad | N° de procedimientos invasivos |
| Contacto Familiar (piel a piel<9 | Tiempo |
Proceso de atención en cuidado paliativo perinatal
Identificación de candidatos a cuidado paliativo perinatal. En el periodo perinatal la complejidad y la incertidumbre se vuelven parte del reto en la implementación del cuidado paliativo.
La elaboración de protocolos de atención paliativa perinatal permite un mayor cumplimiento de objetivos. Se han elaborado a lo largo del tiempo diversos esquemas con propuestas de pacientes en el periodo perinatal susceptibles de requerir cuidado paliativo, sin embargo, dependiendo de la circunstancia, un mismo paciente puede encontrarse en una categoría en una etapa de la vida y en otra posteriormente.
Es por ello que el listado que se incorpora en la Tabla 4 debe ser entendido como un proceso dinámico en el que la recategorización debe ser contemplada.
La propuesta elaborada por "Together for Short Lives" permite esta flexibilidad muchas veces necesaria derivado de la dinámica de la etapa perinatal.

Inicio del cuidado paliativo perinatal. Este comienza a partir de la identificación de una condición amenazante para la integridad física y la vida. Es fundamental que en el inicio de este tipo de abordajes se tenga siempre presente el impacto que podrán tener las decisiones de forma integral para la madre, feto o recién nacido y el grupo familiar.
El fomentar la conciencia social sobre la importancia de control prenatal adecuado abre las puertas para la identificación oportuna de problemas. En la mayoría de las ocasiones los procesos de atención paliativa perinatal tienen ventanas de oportunidad muy cortas, pero de gran impacto para las personas involucradas. Es así que la aceptación y detección oportuna son pasos fundamentales en el proceso.
En la Tabla 5 se muestra cómo la identificación oportuna genera el espacio de oportunidad para intervenciones adecuadas. La participación de un equipo multidisciplinario fortalece la calidad de atención.
En todo momento será prioritario un enfoque ético y humanista en el que, de ser necesario, debe ser involucrado el Comité Hospitalario de Bioética. El equipo de salud involucrado deberá ser vigilante del apoyo centrado en la familia generando siempre los espacios para la privacidad, intimidad y respeto.
Es idóneo que los miembros del equipo de salud desarrollen habilidades de comunicación y contención como parte del trato digno.
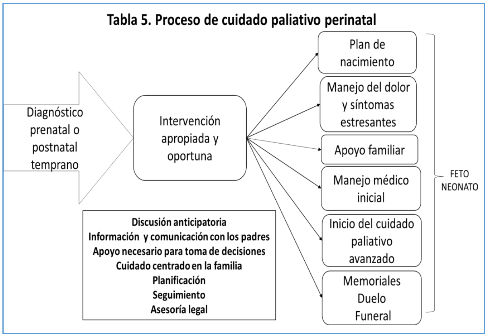
El apoyo psicológico y la información adecuada serán los pilares de las mejores decisiones por parte de la familia. Los sitios destinados para el nacimiento y el fallecimiento deben ser establecidos de acuerdo a las necesidades familiares generando el espacio adecuado para la elaboración de duelo y rituales. En aquellos casos que las condiciones familiares y del paciente lo permitan podrá ser favorecido el fallecimiento en casa, siempre con el enfoque de procurar la calidad de vida durante el cuidado paliativo y en el proceso final. En caso de existir medicación las instrucciones deben ser claras, precisas, y la familia debe conocer el objetivo de los medicamentos que se incorporen al manejo. La asesoría sobre registros de nacimiento, certificados de defunción, servicios funerarios y apoyo psicológico posterior al fallecimiento son indispensables.
Derivado de que los síntomas preponderantes al final de la vida son dolor y disnea, es imprescindible romper las barreras de prejuicio y contemplar de forma óptima los opiáceos. También es necesario que en aquellos casos que el paciente lo requiera y la familia lo solicite, la pre medicación adecuada ante el retiro de manejo de soporte incluida la extubación compasiva debe ser perfectamente analizados y planeados. Independientemente del espacio definido para la defunción, la familia debe ser y sentirse apoyada por el equipo médico. La evaluación del paciente debe ser continua para la identificación de nuevos eventos generadores de estrés que pudieran requerir manejo específico. Dependiendo de las patologías involucradas, dentro de los planes al nacimiento puede estar contemplada una interrupción del embarazo o una intervención curativa o de prolongación de vida, que eventualmente de acuerdo con la evolución puede redirigirse a intervenciones paliativas avanzadas. La muerte digna es un derecho universal incluso al comienzo de la vida, y la aceptación es el primer gran paso para apoyar a esta población vulnerable entre vulnerables. Ante el reto de desarrollar el cuidado paliativo perinatal es importante recordar la frase de Carl Gustav Jung "Lo que niegas te somete, lo que aceptas te transforma".
4.3 MODELO DE PROVISIÓN PARA ATENCIÓN PALIATIVA EN EL PACIENTE NO ONCOLÓGICO
Los objetivos fundamentales de la atención paliativa consisten en el alivio del padecimiento evitable y en la adaptación al padecimiento inevitable, con el fin de mejorar la experiencia de la enfermedad progresiva mediante la promoción de la calidad de vida y el bienestar de enfermos y familias. (16)
Los padecimientos oncológicos encabezan a los pacientes que requieren esta modalidad de atención. Sin embargo, una gran diversidad de enfermedades crónicas se beneficia de estas intervenciones, por debajo del cáncer se encuentran los trastornos neurológicos 30%, malformaciones congénitas y síndromes genéticos 7% y las cardiopatías en un 5%, entre otros grupos, de acuerdo a la casuística en el Instituto Nacional de Pediatría. (17) A diferencia del niño con cáncer, estos pacientes se enfrentan a enfermedades incurables en la mayoría de los casos, con deterioro progresivo y un pronóstico difícil de establecer, pudiendo ser la esperanza de vida muy corta o prolongarse años. Por lo que es fundamental intervenciones tempranas por parte del equipo de soporte para una correcta identificación y valoración inicial.
El objetivo de estas intervenciones tempranas de acuerdo a lo que dicta la OMS ¨reduce las hospitalizaciones innecesarias y el uso de los servicios de salud¨(18) El manejo de los síntomas complejos no es solo el objetivo principal en estos niños, sino vigilar la historia natural de la enfermedad, la complementación del tratamiento farmacológico y no farmacológico de los servicios tratantes, el fortalecimiento emocional y empoderamiento a los cuidadores primarios respecto al manejo en domicilio e identificación de datos de alarma. Y sin duda el gran reto en estos pacientes es evitar la discriminación por el personal de salud o incluso por sus familiares (sobre todo en los pacientes con grave daño neurológico) y la realización de intervenciones fútiles, procurando el trato digno y favoreciendo el interés superior del menor.
4.4 MODELO DE PROVISIÓN DE LA ATENCIÓN PALIATIVA PEDIÁTRICA EN EL PACIENTE ONCOLÓGICO
El cáncer infantil en México es un problema de salud pública por ser la principal causa de muerte por enfermedad entre los cinco y 14 años, se estima que cada año se diagnostican alrededor de 5,000 casos nuevos de cáncer en personas menores de 18 años, con más de 2,000 muertes anuales y una sobrevida global a 5 años de 56%. (19)
El cáncer es curable si se detecta a tiempo; desafortunadamente el 75% de los casos de cáncer en menores de 18 años en México se diagnostican en etapas avanzadas de la enfermedad.
Contar con un modelo de provisión en atención paliativa pediátrica tiene como objetivo mejorar la atención integral de las niñas, niños y adolescentes con condición de vida amenazante, limitante y/o en etapa terminal que reciban tratamiento oncológico en México, brindando a la población pediátrica, así como a su familia, una atención eficiente, oportuna y de calidad conformando equipos interdisciplinarios, comprometidos y de vanguardia que proporcionen atención paliativa para el menor y su familia.
Con este modelo se promueve el acceso oportuno, diagnóstico multidimensional y tratamiento centrado en las necesidades de cada binomio paciente-familia con equidad y respeto a su dignidad y autonomía. Se proporciona a través de una planificación anticipada de cuidados que incluya la percepción de la familia e involucre los recursos comunitarios disponibles; la atención paliativa es asequible aun con recursos limitados y continúa a lo largo de la evolución de la enfermedad independientemente del desenlace; se pueden otorgar en unidades especializadas, hospitales, centros de atención comunitaria y también en el domicilio de los niños. No se limitan a un solo escenario. (20)
La propuesta de atención paliativa de la OMS recomienda: (21-22)
· Comenzar desde el momento del diagnóstico, junto con el tratamiento curativo, si este existe;
· Incluir todos los cuidados de confort hacia el paciente;
· Valorar y realizar el tratamiento escalonado del dolor y otros síntomas;
· Incluir contacto temprano con el niño y la familia;
· Otorgar la atención independientemente del pronóstico;
· Promover el tratamiento de preferencia mediante equipo multidisciplinario;
· Incluir al niño y la familia en la toma de decisiones;
· Usar los recursos disponibles en la comunidad; y
· Ofrecerse en todos los escenarios de atención: hospitalario, ambulatorio y domiciliario.
Todas las unidades médicas que proporcionen atención pediátrica a pacientes con enfermedades limitantes o amenazantes para la vida deben contar con equipos multidisciplinarios capacitados en cuidados paliativos pediátricos. En todos los niveles de atención se deben proporcionar intervenciones adecuadas a las circunstancias y medios que correspondan a cada caso, mantener comunicación y coordinación continua mediante un adecuado sistema de referencia y contra referencia con el fin de proporcionar la mejor calidad de vida al menor y su familia, con respeto a su dignidad y autonomía. (23)
Las instituciones del sistema nacional de salud deberán asegurar el acceso efectivo a los servicios de cuidados paliativos, incluyendo infraestructura, recursos humanos capacitados e insumos.
Criterios de atención
· Paciente en tratamiento curativo con síntomas refractarios o alta complejidad asistencial, en el que se proporciona atención para atender su problemática y continúa atención por el servicio tratante;
· Paciente con enfermedad avanzada, progresiva, síntomas complejos, multifactoriales y alta complejidad asistencial;
· Paciente fuera de tratamiento curativo, con síntomas de difícil control o alta complejidad asistencial;
· Paciente en etapa terminal que elija fallecer en medio hospitalario;
· Paciente que elija tratamiento paliativo en domicilio para establecer plan de atención paliativa, contrarreferencia y seguimiento de caso. (24)
Intervención del equipo de cuidados paliativos
· Conformar equipos multidisciplinarios en todas las instituciones de segundo y tercer nivel que presten atención a población pediátrica;
· Realizar valoración multidisciplinaria desde el diagnóstico cuando se identifiquen necesidades no resueltas o durante el proceso terapéutico;
· Elaborar plan de atención y seguimiento incluyendo a los equipos de atención primaria en las comunidades de origen; y
· Atención terapéutica integral que incluya aspectos físicos, psicológicos, sociales y espirituales para los pacientes y sus familias a nivel hospitalario, ambulatorio y/o domiciliario mediante intervenciones de probada eficacia, protocolos estandarizados de manejo y criterios uniformes de actuación, calidad de atención y continuidad de cuidados. (25)
Referencia. El servicio de oncología pediátrica a cargo del paciente solicita la intervención del equipo interdisciplinario de soporte y paliación. El equipo interdisciplinario realiza valoración multidimensional mediante instrumentos validados y consensuados para integrar el diagnóstico multidimensional integral y elaborar el plan inicial de atención. Todas las intervenciones serán consignadas en el expediente clínico institucional.
Se realiza reunión para consensuar con paciente-familia el plan de atención paliativa y las metas de atención: control sintomático, problemática psico-social, familiar, directrices anticipadas, etc.
El diagnóstico, plan de atención y consensos establecidos se integran en el expediente clínico incluyendo la evaluación de metas e indicadores de atención.
Se establece cita de seguimiento, se valora la evolución y pertinencia de continuar la atención en la clínica de soporte y paliación o referencia a su clínica de atención primaria.
Plan de atención paliativa. Para todos los casos se establecerá un plan de atención multidisciplinario consensuado con paciente y familia con el fin de coordinar las metas de atención durante el proceso evolutivo de la enfermedad.
En el caso de pacientes que elijan atención paliativa en domicilio se establecerá el plan de atención paliativa multidimensional con apoyo psico-educativo para los cuidadores que realizaran los cuidados en el domicilio y referencia al equipo de atención primaria correspondiente.
Niveles de intervención. (26) Primer nivel de atención: los cuidados paliativos pediátricos son llevados a cabo por todos los profesionales de la salud con conocimientos básicos de atención paliativa en seguimiento del plan de atención consensuado con el equipo tratante. Es recomendable contar con pediatras de atención primaria para seguimiento de casos a domicilio.
Segundo nivel de atención: dirigido a casos más complejos que requieren intervención especializada ambulatoria, hospitalaria o de urgencia. Todos los médicos de unidades de segundo nivel deberán tener una formación intermedia en cuidados paliativos y asesoría por cuidados paliativos especializados para dar continuidad al plan de atención.
Tercer nivel de atención: dirigido a situaciones de alta complejidad asistencial que requieren atención por profesionales miembros de un equipo interdisciplinario especializado en cuidados paliativos pediátricos. Estos equipos elaboran guías y planes de atención, capacitan, asesoran mediante telemedicina y dan seguimiento a los equipos que brindan atención de menor complejidad.
La atención domiciliaria se proporciona principalmente en casos con baja complejidad asistencial: pacientes con plan de atención establecido, adecuado control de síntomas, con red de apoyo familiar, cuidadores capacitados y que elijan permanecer en su domicilio en la etapa final de la vida.
Para garantizar la continuidad en la atención del paciente pediátrico y la comunicación entre los diferentes equipos con el binomio paciente-familia, las instituciones de salud deberán facilitar la referencia y contra referencia oportuna, expediente clínico y plan de atención compartido, además de soporte, a través de líneas telefónicas y/o telemedicina.
En caso necesario por complejidad asistencial o síntomas refractarios, se solicitará apoyo de la unidad de cuidados paliativos de segundo o tercer nivel de atención, la cual determinará si el paciente es candidato a hospitalización, manejo en otras unidades especializadas, atención de urgencia o manejo ambulatorio.
Es esencial la organización de redes específicas de acción rápida donde trabajen equipos interdisciplinares pediátricos expertos en estrecha colaboración con las redes locales de atención primaria y hospitales de referencia.
4.5 MODELO DE PROVISIÓN DE LA ATENCIÓN PALIATIVA PEDIÁTRICA CON TRANSICIÓN A LA VIDA ADULTA
El paciente pediátrico se considera hasta los 16-18 años de vida en México, edad que puede variar en diferentes países.
En el contexto legislativo de nuestro país, los adolescentes de 16 años ya son responsables de sus actos delictivos, pero en medicina nos tenemos que preguntar si tenemos que usar las mismas directrices de autonomía y dignidad para con las decisiones terapéuticas que rijan al enfermo.
A pesar de que no existe una estadística confiable para conocer la frecuencia de uso de los servicios médicos en adolescentes, se estima que es aproximadamente 7% de la totalidad de la consulta de primer nivel y la población se encuentra entre 10 y 19 años. (27-28)
Dentro de las primeras causas de mortalidad en la adolescencia e inicios de la adultez se encuentran las leucemias, problemas congénitos y parálisis cerebral infantil, las cuales son enfermedades crónicas que necesitan una atención primaria de cuidados paliativos.
En pacientes con alguna enfermedad crónica o terminal que se encuentre o requiera cuidados paliativos y esté cerca de los 16 años, será muy importante encaminar el tratamiento paliativo a instancias para adultos que puedan y tengan la capacidad para atenderles y así realizar una transición menos agresiva.
La sugerencia es que esta preparación sea aproximadamente de tres meses previos al cambio de instancia. (29,30)
En cuanto a los recursos públicos, normalmente son insuficientes para permitir a todas las familias cuidar de los pacientes en su domicilio, por lo tanto, el equipo debe adaptarse en medida de lo posible a la dinámica de cada familia para procurar mantener su normalidad familiar y social.
BIBLIOGRAFÍA
1. Constitución Política de los Estados Unidos Mexicanos.
2. Bellieni CV, Vannuccini S, Petraglia F. Is fetal analgesia necessary during prenatal surgery? J Matern Fetal Neonatal Med. 2018 May; 31:1241-1245.
3. Glover V, Fisk NM. Fetal pain: implications for research and practice. British Journal of Obstetrics and Gynaecology 1999;106:881-6
4. Anand KJS, Hickey PR. Pain and its effects in the human neonate and fetus. New Engl J Med 1987;317:1321-1329
5. León A. Ensayo sobre ética y profesión médica. Impresora Edive, 1985. pp.303-309
6. Adams, SY, Tucker, R., Clark, MA y col. "Quality of life: parent and neonatologist perspective. J Perinatol 2020; 40:1809-1820.
7. Ramezani T, Hadian Shirazi Z, Sabet Sarvestani R, Moattari M. Family-centered care in neonatal intensive care unit: a concept analysis. Int J Community Based Nurs Midwifery. 2014; 2:268-278.
8. Bass RD, et al. Health-related quality of life for infants in the neonatal intensive care unit. J Perinatol 2012;32:901-6
9. Lowman LB, Stone LL, Cole JG. Using developmental assessments in the NICU to empower families. Neonatal Netw 2006;25:177-86
10. Lund CH, Osborne JW. Validity and reliability of the neonatal skin condition score. J Obstet Gynecol Neonatal Nurs. 2004; 33:320-7.
11. Varni JW, Limbers CA, Neighbors K, Schulz K, Lieu JE, Heffer RW, Tuzinkiewicz K, Mangione-Smith R, Zimmerman JJ, Alonso EM. The PedsQL Infant Scales: feasibility, internal consistency reliability, and validity in healthy and ill infants. Qual Life Res. 2011 Feb; 20:45-55.
12. Jensen D, Wallace S, Kelsay P. LATCH: a breastfeeding charting system and documentation tool. J Obstet Gynecol Neonatal Nurs. 1994 Jan;23:27-32
13. Hedstrom AB, Gove NE, Mayock DE, Batra M. Performance of the Silverman Andersen Respiratory Severity Score in predicting PCO2 and respiratory support in newborns: a prospective cohort study. J Perinatol. 2018;38:505-511
14. Olsson E, Ahl H, Bengtsson K, et al. The use and reporting of neonatal pain scales: a systematic review of randomized trials. Pain. 2021; 162:353-360.
15. Dickson G. A perinatal pathway for babies with palliative care needs. 2a Edition. Editors: Lizzie Chambers, Myra Johnson, Helen Curry. Together For Short Lives 2017. England Wales pp. 14
16. Cassell EJ, editor. The Nature of Suffering and the Goals of Medicine, New York: Oxford Univ. Pr.; 1991.
17. Armando Garduño Espinosa, Cuidados paliativos en pediatría, 2da ed. México: Trillas 2018.
18. Cuidados paliativos (who.int). Agosto 2020. https://www.who.int/es/news-room/fact-sheets/detail/palliative-care
19. Cáncer en la Infancia y la Adolescencia (2013-2018) Programa de acción especifico SS http://www.censia.salud.gob.mx/contenidos/descargas/transparencia/especiales/PAE_Cancer.pdf
20. Manual de atención integral de personas con enfermedades crónicas avanzadas http://calidad.salud.gob.mx/site/calidad/ctcp/art-ctcp_15.pdf
21. Cámara de Diputados. Dictamen de la Comisión de Salud por el que se reforma y adiciona diversas disposiciones de la Ley General de Salud en materia de cuidados paliativos. Gaceta Parlamentaria. 2021. 1-27
http://sil.gobernacion.gob.mx/Archivos/Documentos/2021/04/asun_4174463_20210421_1619018818.pdf
22. World Health Organization. World Health Organization WHO definition of Palliative Care [curso en línea]. Redbioética Unesco, 2007. htpp://www.who.int/cancer/palliative/en/print.htlm
23. Bernarda Cuidados paliativos pediátricos Arch Pediatr Urug 2012; 83(3): 204-211 http://www.scielo.edu.uy/pdf/adp/v83n3/v83n3a08.pdf
24. Acuerdo por el que se declara la obligatoriedad de los esquemas de manejo integral de cuidados paliativos, así como los procesos señalados en la Guía del Manejo Integral de Cuidados Paliativos en el Paciente Pediátrico, publicado en el Diario Oficial de la federación el 14 de diciembre de 2016. https://www.dof.gob.mx/nota_detalle.php?codigo=5465444&fecha=14/12/2016#::text=ACUERDO%20por%20el%20que%20se,Paliativos%20en%20el%20Paciente%20Pedi%C3%A1trico.
25. Modelo de salud para el Bienestar basado en APS https://www.gob.mx/cms/uploads/attachment/file/631068/2021_Modelo_SABI_FINAL_17_feb_21.pdf
26. Cacciavillano, Walter Soporte clínico oncológico y cuidados paliativos en el paciente pediátrico - 1ª ed. - Buenos Aires: Instituto Nacional del Cáncer, 2013. http://www.icpcn.org/wp-content/uploads/2015/04/Soporte-y-cuidados-paliativos-en-el-paciente-pediatrico.pdf
27. Carmen Varela Petito, (2008). Jóvenes en transición hacia una vida adulta. En Demografía de una sociedad en transición, (pp. 69-73). Uruguay: Trilce.
28. J.A. Villegas Rubio y M.J. Antuña García, (2012). Cuidados Paliativos Pediátricos. Boletín de Pediatría, LII, (pp. 131-145).
29. Santos-Preciado JI, Villa-Barragán JP, García-Avilés MA, León-Álvarez GL, Quezada-Bolaños S. y Tapia-Conyer R, (2003). La transición epidemiológica de las y los adolescentes en México. Salud Pública de México, (pp. 45, 140-152).
30. Grupo de trabajo en el seno del Comité de Seguimiento y Evaluación de la Estrategia en Cuidados Paliativos del Sistema Nacional de Salud, (2014). Cuidados Paliativos Pediátricos en el Sistema Nacional de Salud: Criterios de Atención. Madrid, España: Ministerio de Sanidad, Servicios Sociales e Igualdad.
CAPÍTULO V
CONTROL DE SIGNOS Y SÍNTOMAS EN CUIDADOS PALIATIVOS PEDIÁTRICOS
La piedra angular en los Cuidados Paliativos hace referencia al control del dolor y otros síntomas físicos. Las bases para el manejo de síntomas en la población pediátrica, es muy similar a la de los adultos, sin embargo, guarda algunas particularidades con respecto al adulto, como son el estado de maduración y desarrollo del niño, las diferencias de absorción y metabolismo de los medicamentos, sobre todo en los primeros seis meses de vida. Otra de las particularidades de este grupo etario, es la dificultad para poder deglutir las formas sólidas de los fármacos y las pocas presentaciones pediátricas disponibles en el país de los medicamentos necesarios para el control de síntomas. (1,2)
Para favorecer la calidad de vida tanto del niño como de su familia, es imprescindible llevar a cabo un impecable manejo de síntomas, siempre teniendo en cuenta el estado del paciente, la progresión de la enfermedad y los recursos disponibles en cada familia. (1,2)
5.1 DOLOR Y SU ABORDAJE MULTIMODAL
Tanto en niños como adultos en Cuidados Paliativos, uno de los principales síntomas que se evidencian en estos pacientes es el dolor, de ahí la importancia de reconocerlo y manejarlo de forma precoz y eficaz.
Independientemente de la condición del niño; el dolor y el miedo son las principales causas de sufrimiento del niño que cursa con alguna enfermedad limitante o amenazante para la vida. (1, 2).
El dolor se define según la Asociación Internacional para el Estudio del Dolor (IASP por sus siglas en inglés) como una experiencia sensorial y emocional desagradable asociada a una lesión tisular real o potencial, o descrita en términos de dicho daño. También se considera a la percepción del dolor como una cualidad del ser humano que actúa como un sistema de señales en respuesta a un daño tisular, que incluye respuestas fisiológicas como conductuales, por lo que se puede medir mediante indicadores conductuales y/o fisiológicos. Además, el dolor es la consecuencia de una interacción compleja entre factores biológicos, psicológicos, individuales, sociales y ambientales, en el cual se vinculan emociones como la ansiedad, depresión y el comportamiento. (3,4)
Evaluación del dolor en pediatría. La adecuada evaluación y anamnesis del dolor facilitará el manejo oportuno y eficaz dependiendo de la patología y evolución de cada niño.
El primer paso para llevar a cabo ante la presencia de un niño con dolor es realizar una adecuada semiología, existen algunas nemotecnias que ayudarán a evaluar cada aspecto de dolor, una muy útil es la siguiente:
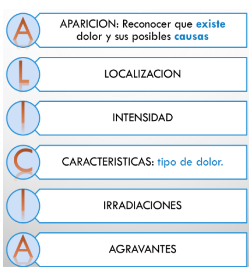
Semiología del dolor. Los métodos de medición utilizados en pediatría son de tres tipos:
· Métodos fisiológicos. La reacción fisiológica del cuerpo del niño al dolor. Se evalúan signos como la frecuencia cardíaca, la tensión arterial, la frecuencia respiratoria;
· Métodos conductuales: Lo que al niño le hace al sentir el dolor. Se fundamentan en la observación de la conducta del niño en situación de dolor; y
· Métodos de autorreporte: Lo que el niño dice respecto a su dolor. A partir de los tres a cuatro años la mayoría de los niños tiene capacidad para comprender el concepto de dolor, percibir su intensidad e informarlo. (5)
Asimismo, una escala ideal debe ser aquella que brinde una adecuada sensibilidad, libre de sesgos, lo más exacta posible, fiable, reproducible, barata y segura, que permita cuantificar el dolor, instaurar un tratamiento adecuado basado en la intensidad de este, valorar la respuesta terapéutica y comparar la efectividad de los tratamientos. (6,7)
Escalas empleadas de acuerdo con el grupo etario. En niños menores de cuatro años se usan las mediciones conductuales, tomando en cuenta como parte fundamental de la evaluación el reporte de los padres, familiares y/o del equipo de enfermería. El siguiente paso es revisar los signos vitales, desde el día anterior hasta la nueva visita y así verificar el comportamiento en las horas anteriores. Esta manera de evaluación también se utiliza en pacientes que no se pueden comunicar por alguna alteración o por el estado de su enfermedad. Una de las escalas más empleadas en la escala de FLACC. (6,7)
| Puntuación | 0 | 1 | 2 |
| Expresión facial. | Expresión habitual; cara relajada. | Arruga la nariz; frunce el entrecejo; muecas esporádicas. | Temblor del mentón mandíbula tensa. |
| Posibilidad de consuelo. | Está a gusto de modo espontáneo. | Se le puede consolar. | Es difícil consolarle. |
| Llanto. | No hay llanto. | Gimotea, se queja. | Llanto intenso. |
| Actividad. | Esta acostado y tranquilo. | Se dobla sobre su abdomen; encoje las piernas. | Está rígido. |
| Movimientos de piernas. | Piernas relajadas. | Piernas inquietas. | Pataleo intenso. |
Nota: 0= no dolor; 1-2= dolor leve; 3-5= dolor moderado; 6-8= dolor intenso; 9-10= máxima dolor imaginable
Escala de FLACC indicada en los pacientes menores de 4 años y no colaboradores. Entre los 4 y los 6 años: la evaluación del dolor puede ser difícil y se debe elegir el elemento que complazca al niño, si es posible la autoevaluación. En este grupo etario, la escala de elección es la Manual Analógica (MA) adecuándose el vocabulario del paciente para mayor entendimiento; se realiza mostrando con la mano si el dolor es "chiquito", "mediano" o "grandote" y se le pregunta al paciente; (7)
| Escala Manual Análoga |  |
Para mayores de seis años, el autorreporte es lo mejor, lo que el niño nos dice respecto de su dolor y cómo lo define.
· Escalas numéricas: preguntar cuánto es el dolor de 0 a 10 (0 indica que no duele nada y 10 es el máximo dolor imaginable).
· Escala visual análoga: variante de la anterior. Sobre una línea de 10 cm, explicar lo mismo y permitir que el paciente señale cuál es su dolor. Esta escala es más sensible.6,7
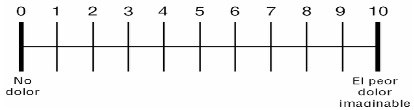
· Escala de las caras revisada (FPS-R, Figura 2): se trata de una escala gráfica con seis caras que van desde una imagen sin dolor a una con mucho dolor. Comparada con otras escalas de caras, es más específica para medir intensidad del dolor. (6,7)

Dichas escalas nos permitirán evaluar la intensidad del dolor: (1,2)
· Leve (0 a 3);
· Moderado (4 a 6); y
· Severo (más de 7)
Clasificación del dolor. El dolor se clasifica según su fisiopatología, temporalidad e intensidad, de acuerdo con la tabla siguiente. (2,3)
| Fisiopatología | Temporalidad | Intensidad | |||||
| · Nociceptivo | Somático | · Agudo | · Leve | ||||
| Visceral | · Irruptivo | · Moderado | |||||
| · Neuropático | · Crónico | · Severo | |||||
| · Dolor mixto | | | | | | | |
| · Psicogénico | | | | | | | |
Escalera analgésica. En 1986 se publicó el artículo Cancer Pain Relief y su publicación derivó en lo que hoy se conoce como la escalera analgésica de la OMS.
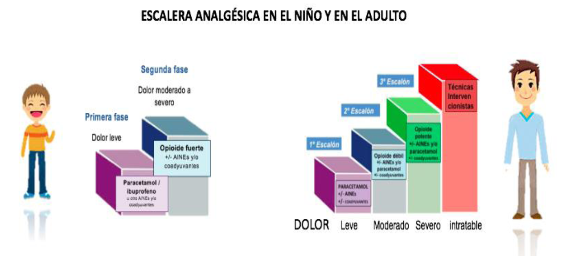
Dicha escalera, ha sido motivo de constantes debates, sobre todo en lo que respecta a la población pediátrica, ya que, en el 2012, se establecieron las directrices del manejo del dolor en pediatría con un documento denominado: "Cancer Pain Relief and Palliative Care in Children", en donde se propone el uso de una escalera de dos peldaños, sin embargo en los últimos años la tendencia ha sido usar la escalera de tres peldaños (usada también en adultos), en la que se recomienda el uso de tramadol para el tratamiento del dolor moderado, ya que este ha cobrado mejor evidencia en la población pediátrica en los últimos años, sobre todo en algunos lugares en donde no es asequible algún opioide fuerte, este fármaco puede ser una opción eficaz para el manejo de dolor moderado. (8)
Estrategias farmacológicas. El manejo farmacológico en el área pediátrica es complejo debido a las variantes en cuanto a la farmacodinamia y farmacocinética en todos los grupos etarios, además de la evidencia clínica limitada que guíe el uso correcto de muchos fármacos. La mayoría de los medicamentos y de las directrices sobre su uso, es basada en información extrapolada de adultos a la práctica en pacientes pediátricos. Por lo que es importante considerar las características farmacológicas, los mecanismos de acción, los efectos adversos y las indicaciones específicas de cada fármaco para incrementar la seguridad en la elección del tratamiento. (8,9)
AINES. Dosis recomendadas de Paracetamol en pediatría para manejo del dolor (9)
| | Dosis inicial única al inicio de tratamiento (mg/kg) | Dosis de continuación (mg / kg) | Intervalo de dosis (h) | dosis diaria máxima (mg / kg / día) |
| Oral prematuros 28-30 SDG | 20 | 15 | 12 | 35 |
| Infantes prematuros 31 -38 SDG | 20 | 15 | 12 | 45 |
| Recién nacido y bebés hasta a 6 meses | 20 | 20 | 8 | 60 |
| Bebés después del sexto mes | 30 | 10-20 | (4-)6 | 60 |
| Niños pequeños> 1 año | 30 | 15 | (4-)6 | 75 |
| Niños> 6 años | 30 | 15 | (4-)6 | 90 Máx. absoluto . |
| Intravenoso recién nacidos de término y niños con peso <10 kgs | 7.5 | 7.5 | (4-)6 | 30 |
| Niños que pesan: >10 kg y <33 y >33 a <50 kg | 15 | 15 | 6 | 60 Máximo: 2 y 3 g /.día. |
| Es necesario destacar que: La dosis de paracetamol por vía I.V. es controvertida en neonatos y lactantes. El BNF para niños sugiere una dosis de 7.5 mg / kg cada 8 h (máximo 25 mg kg al día) en neonatos prematuros de más de 32 semanas de edad postmenstrual y 10 mg kg cada 4-6 h (máximo 30 mg / kg al día) en neonatos. | ||||
Dosis recomendadas de AINES más comunes en pediatría para manejo del dolor. (9)
| Medicamento | Tiempo de acción | Dosis pediátrica | Dosis Adulto |
| Ibuprofeno | 0.5 h | 6-10 mg/kg cada 6-8 hrs. | 200-400 mg cada 4-6 hrs. |
| Naproxeno | 2-4 h | 5 mg/kg cada 12 hrs. | 250-500 mg cada 6-8 hrs. |
| Ketorolaco | 0.75-1 h | 0,25-0,5 mg/kg IV o IM, cada 6 hrs. | Dosis de carga de 30 mg IV, luego 15-30 mg cada 6 hrs. |
| Metamizol | | 10-15 mg/kg cada 8 hrs. | 1 a 2 gr IV cada 8 hrs. |
Opioides. Existen cuatro prácticas fundamentales de optimización del uso de los opioides en niños.
· Los opioides sólo deben utilizarse para las indicaciones apropiadas y ser prescritos por profesionales capacitados tras evaluar detenidamente los beneficios y los riesgos;
· El uso de opioides por parte de las personas, su impacto en el dolor y sus efectos adversos deben ser continuamente monitoreados y evaluados por profesionales capacitados;
· El profesional que prescriba la receta debe tener un plan claro para la continuación, disminución o interrupción de la administración de opioides en función de la afección del niño. El niño y la familia deben ser informados del plan y de su justificación; y
· Debe prestarse la debida atención a la adquisición, el almacenaje y la eliminación de los opioides no utilizados. (10)
Dosis pediátricas de opioides. (10,11)
| Fármaco | Edad | Dosis |
| Tramadol | > 6 meses | 1-2 mg/kg/6-8 hrs Infusión: máximo 6-7 mg/kg/día. |
| Morfina | Recién Nacidos, lactantes y niños. | IV. SC. Bolos: 0.05-0.1 mg /kg cada 2-4 hrs Oral: 0.15-0.3 mg/kg cada 4 hrs 6 u 8 hrs. Infusión: 0.03 mg/kg /hrs o 0.2-0.5 mg/kg /día |
| Oxicodona | Lactantes 1- 8 años >8 años | Oral: 50 a 125 mcg/kg/4 hrs Oral: 125- 200 mcg/Kg/4 hrs (Máximo de 5 mg/dosis) Liberación inm. Oral 5 mg cada 12 hrs (Liberación prolongada) |
| Hidromorfona | 1-12 años | IV. SC. Bolos: 0. 0.015 mg/kg cada 2-4 hrs Oral: 0.03-0.06 mg/kg cada 3-4 hrs Infusión: 0.006 mg/kg/hrs |
| Buprenorfina | Lactantes y niños. | IV Bolos 0.5 a 2 µg/kg/ dosis cada 6- 8 hrs Infusión 6-18 µg / kg / día |
| Fentanilo | Recién Nacidos, lactantes y niños. | IV Bolos: 0.5-1 µg/kg cada 1-2 hrs Infusión: 0.5-3.0 µg /kg /hrs |
| Metadona | Recién Nacidos, lactantes y niños. | 100-200 mcg/kg/4 hr VO (Máximo 5 mg/dosis) VO y IV. Después de 3 dosis se continua cada 6 - 12 hrs. |
Adyuvantes
Neuromoduladores. Son un grupo de fármacos, que participan en la disminución del proceso fisiopatológico de sensibilización central y periférica, actúan como tratamiento esencial para el control del dolor de tipo neuropático y en algunos cuadros de hiperalgesia visceral. Este conjunto farmacológico es representado por antiepilépticos gabapentinoides y antidepresivos tricíclicos. Actualmente sigue existiendo poca evidencia respecto al uso de estos fármacos. (12,13)
· Gabapentioides: actúan como análogos estructurales del GABA, interactúan de manera selectiva con la subunidad alfa-2-delta de los canales de calcio, modulando el influjo de este ión a la célula, reducen la liberación de glutamato y noradrenalina, disminuyen la liberación de sustancia P y calcitonina e inhiben la hiperexcitabilidad de las neuronas. Particularmente la Gabapentina ha demostrado seguridad y efectividad en su uso en pediatría, requiere una titulación gradual, con ajuste a dosis optimas, con dosis iniciales de 10 a 15 mg/ kg / día hasta 50 mg/kg/día. Su principal efecto adverso es el efecto de somnolencia y efecto sedativo de leve a moderado. (12)
· Dexmedetomidina: agonista adrenérgico a-2. Proporciona analgesia al unir receptores alpha-2 en la vía nociceptiva aferentes en el cuerno dorsal de la médula espinal, alterando así la liberación de la sustancia P. Los efectos adversos más representativos son la hipotensión, bradicardia y sequedad bucal. (12,14)
· Tricíclicos: su mecanismo de acción es el bloqueo de los receptores colinérgicos alfa 1 y alfa 2 adrenérgicos, y H1 y H2, histaminérgicos; bloquean la recaptación de la noradrenalina y de la serotonina, bloqueo de canales de sodio, calcio y activador de canales de potasio, inhibición de NMDA, disminución de PGE2 y de la producción del FNT, incrementa la función del receptor GABA, activa receptores opioides. La dosis pediátrica de la amitriptilina es de es de 0,5 - 1 mg/kg al acostarse, pudiendo elevarse la dosis hasta 5 mg/kg. (12)
· Duloxetina: fármaco antidepresivo, inhibidor de la receptación de serotonina y de noradrenalina. También inhibe débilmente la receptación de dopamina, dentro de sus principales adversos destacan las náuseas, somnolencia, mareos y fatiga. La dosis recomendada en pediatría es de 0,5 a 1 mg/kg c/12 ó 24 horas. (12)
· Ketamina: Antagonista no competitivo de NMDA, efectos opiáceos débiles, antagonista del receptor NMDA, demuestra actividad en los receptores opioides, e inhibe la receptación de la dopamina y la serotonina a dosis sub-anestésica tienen efectos analgésicos y anti hiperalgésico. Sus principales efectos adversos son: la disforia, alucinaciones, somnolencia y mareo. La dosis recomendada es de 0.1 a 0.2 mg / kg/ hr. (15)
· Lidoacaina: Fármaco antiarrítmico 1b clase que inhibe los canales de sodio y de potasio, el receptor de NMDA, y el transportador de glicina I. Su uso debe ser cauto tomando en consideración el riesgo de neurotoxicidad y cardiotoxicidad asociado al uso de anestésicos locales. (12,14)
· Esteroides: En situaciones especiales, el uso de esteroides puede ser de utilidad, como por ejemplo en tumoraciones que condiciones hepatomegalia, infiltración al sistema nervioso central o periférico, la hipertensión intracraneana, en el dolor óseo refractario ó secundario a metástasis óseas. El fármaco de elección en este grupo es la dexametasona con una dosis 0.25 mg-0.5 mg/kg/día. (12,14)
Estrategias no farmacológicas para manejo de dolor. Definición: Medidas físicas y psicológicas para disminuir el dolor, empleadas de primera línea y como auxiliar en el tratamiento con enfoque multimodal que incluye el empleo de estrategias no medicamentosas. Se centra en individualizar las necesidades del paciente y ha demostrado la necesidad de dosis más bajas y menos efectos adversos de los medicamentos. La mayoría de las estrategias pueden ser llevadas a cabo por cualquier miembro del equipo de salud. Las intervenciones pueden ser de mucho beneficio cuando se requiere la cooperación del paciente para realización de procedimientos y el empleo de fármacos no es factible. (16)
Los niños menores de 7 años son cognitivamente inmaduros por lo que las medidas de comodidad física y las actividades de distracción son más eficaces que el razonamiento verbal para el control de angustia, y por lo tanto a mejorar el dolor. (17)
Medidas de comodidad física:
· Estimulación oral. Administración de alimentación mediante succión o solución glucosada al 25% durante el periodo neonatal;
· Contacto físico con los padres. Terapia Canguro (piel con piel) durante procedimientos dolorosos; (16)
· Masaje: Superficial, que tiene efecto sobre los sistemas nervioso y muscular porque mejora de circulación local; y profundo, que estimula la circulación, disminuye espasmos y tensión muscular;
· Medicina física:
· Medios físicos (crio o termoterapia);
· Neuroestimulación eléctrica transcutánea (TENS);
· Requiere prescripción médica;
· Estimulación vibratoria. (Requiere prescripción médica); y
· Movilización articular, que puede emplearse en conjunto con terapia asistida con animales. (16)
Actividades de distracción. Pueden ser empleadas en pacientes de distintas edades y nivel de desarrollo:
· Medios electrónicos: juegos de videos, caricaturas, películas, etc.;
· Juego: marionetas, juego de imitación, interactivos, lectura de historias, cuentos imaginativos guiados;
· Terapia asistida con animales;
· Intervenciones conductuales;
· Arte: pintura, dibujo, musicoterapia; y
· Empleo de lenguaje positivo: hablar con sinceridad, tranquilizar, emplear analogías de acuerdo con las preferencias culturales y necesidades del paciente y su familia. (17)
Actividades de relajación
· Aromaterapia con las siguientes recomendaciones de esencias:
Cefalea: menta, lavanda, romero, eucalipto;
Dolor generalizado: pimienta negra, limón, romero, copaiba;
Ansiedad: naranja, manzanilla, lavanda, sándalo, ylang ylang.
Observación: Estas esencias no deben ser ingeridas, nebulizadas o aplicadas directamente en mucosas o heridas abiertas. Su uso es mediante difusores, inhalación del recipiente que las contenga, en caso de no existir alergias pueden aplicarse en la piel de preferencia diluidas en aceites vehiculares como el de coco fraccionado, aguacate, uva, etc. De emplearse en manos pueden ser mediante el terapeuta o paciente y estas deben de lavarse con agua y jabón al concluir la terapia. (18,19)
Técnicas de relajación
· Modificación del ambiente: Buscar un ambiente tranquilo, luces y sonidos tenues, aroma y temperatura agradable;
· Posicionamiento: cambio de posiciones para buscar la comodidad del paciente;
· Mindfulness; y
· Dibujar. (19)
5.2 SÍNTOMAS SISTÉMICOS
Síndrome constitucional. Se integra con la presencia de tres signos y síntomas: astenia, pérdida de peso involuntaria (>5 % del peso corporal total en 6 meses) y anorexia. (1)
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Procinético. En caso de asociarse a náuseas o para mejorar el vaciamiento gástrico. | Cisaprida (VO) Pediatría: 0.1 a 0.2 mg/kg/dosis cada 6 a 8 horas. No exceder 10 mg/dosis. Metoclopramida (VO/IV) Pediatría: 0.1 a 0.15 mg/kg/dosis hasta cada 8 horas. No exceder 0.5 mg/kg/día | Pueden presentarse diarrea, cólicos y alteraciones gastrointestinales, que mejoran con disminución de la dosis. Trastornos Extrapiramidales. |
| Glucocorticoides *Suelen usarse por periodos cortos de tiempo. | Dexametasona (IM/IV/VO) Pediatría: 2.5-10 mg/ m2/día. Repartir en 2 a 4 dosis. Máximo 10 mg cada 6 horas. Prednisona (VO) Pediatría: 1 a 2 mg/kg/día. dividido en 1 a 3 dosis. Dosis máxima 60 mg/día. | Hipertensión arterial, hipokalemia, debilidad muscular. Síndrome Cushing Uso prolongado a dosis altas: supresión adrenal. *En caso de pacientes con obesidad calcular con base a peso ideal. |
Estrategia no farmacológica
· Explicar a la familia que el apetito e ingesta de alimentos suele disminuir al final de la vida;
· Ofrecer alimentos apetecibles en pequeñas cantidades y en un entorno tranquilo con compañía;
· Atención psicosocial;
· Empleo de técnicas de relajación;
· Mindfulness;
· Aromaterapia; y
· Musicoterapia. (2)
Fiebre. Cuando sea posible, se debe determinar si las causas son reversibles, es decir, susceptibles de tratamiento.
Ejemplo de este tipo de circunstancias, sería cuando se obtienen beneficios con el uso de antibióticos, citotóxicos, relajantes musculares, antiinflamatorios, transfusiones sanguíneas, enfermedad injerta contra huésped, desregulación autonómica, estado pro inflamatorio. Sin omitir que, cuando el paciente se encuentra al final de la vida, el tratamiento se limita generalmente al control de síntomas. A continuación, se citan algunos fármacos de utilidad.
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Antipiréticos | Paracetamol (VO/IV) <12 años: 10-15 mg/kg/dosis cada 4 a 6 hrs <12 años: 325 a 650 mg cada 4 a 6 hrs Vía Rectal: 10-20 mg/kg/dosis cada 4 a 6 hrs No sobrepasar 3 gr/día. Metamizol (VO/IV) Pediatría: 10-15 mg/kg/dosis cada 4 a 6 horas | Hepatotoxicidad *Evitar vía intrarrectal en pacientes con neutropenia |
| AINE | Ibuprofeno (VO) Pediatría: 10 mg/kg/dosis cada 6 a 8 horas, no sobrepasar 400 mg cada 6 horas. Dosis máxima 3.2 gr/día *Combinación con paracetamol en caso de que la fiebre no ceda a un solo agente. Naproxeno (VO) 2 a 12 años: 5-7 mg/kg/ dividido en dosis cada 12 horas al día >12 años: 250-500 mg cada 8-12 hrs Dosis máxima: 1,250 mg/día | Con uso prolongado incrementa riesgo de sangrado de tubo digestivo. Cuando es posible administrar con alimentos o leche. Nefrotoxicidad. No emplear en conjunto más de un AINE. |
Estrategia no farmacológica
· Evitar sobre arropamiento;
· Mantener al paciente hidratado;
· Evitar fluctuación de temperatura en la habitación;
· Baño con agua tibia;
· Evitar el uso de alcohol o fomentos con agua fría;
· Promover el cuidado de la boca, manteniendo labios y mucosa hidratados; y
· Explicar a cuidadores que la fiebre puede ser parte del proceso de muerte y no siempre es causada por infección. (2)
Caquexia y anorexia. El tratamiento de la enfermedad de base puede ayudar en el control de la producción excesiva de citosinas y factores pro inflamatoria.
Estos síntomas en general tienen mala respuesta al tratamiento farmacológico. (1)
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Procinético En caso de asociarse a náuseas o para mejorar el vaciamiento gástrico | Cisaprida (VO) Pediatría: 0.1 a 0.2 mg/kg/dosis cada 6 a 8 horas. No exceder 10 mg/dosis. Metoclopramida (VO/IV) Pediatría: 0.1 a 0.15 mg/kg/dosis hasta cada 8 horas. No exceder 0.5 mg/kg/día. | Pueden presentarse diarrea, cólicos y alteraciones gastrointestinales, que mejoran con disminución de dosis. Trastornos extrapiramidales |
| Corticoesteroi-des: *Suelen usarse por periodos cortos de tiempo | Dexametasona (IM / IV / VO) Pediatría: 2.5-10 mg / m2/ día. Repartir en 2 a 4 dosis. Prednisona (VO) Pediatría: 1 a 2 mg / kg / día. dividido en 1 a 3 dosis. Dosis máxima 60 mg / día | Hipertensión arterial, hipokalemia, debilidad muscular. Síndrome Cushing Uso prolongado a dosis altas: supresión adrenal. *En caso de pacientes con obesidad calcular con base a peso ideal. |
| Hormonales | Acetato de megestrol (VO) >8 meses: 7,5 a 10 mg / kg / día dividida en 1 a 4 dosis y ajustar dosis en función de la respuesta. Se recomienda disminuir la dosis si el aumento de peso es excesivo. Dosis máxima diaria: 800 mg/día o 15 mg / kg / día. Duración aproximada del tratamiento: 3-11 meses. | |
| Antihistamínicos | Ciproheptadina (VO) Pediatría: 2 a 4 años: 3 mg/8 horas. 4-10 años: 6 mg / 8 horas. >10 años: 9 mg / 8 horas. | Sedación, mareo |
Estrategia no farmacológica
· Intervención psicosocial;
· Explicar a cuidadores que generalmente disminuye el apetito del paciente al final de la vida. Establecer metas alcanzables;
· Forzar la ingesta de alimento no prolonga la vida y puede causar molestias como: vómito, calambres, constipación y alteraciones en motilidad intestinal;
· Individualizar cada caso y considerar el empleo de tubos de alimentación;
· Sugerir opciones distintas a la nutrición como humedecer los labios y boca (con esponja, gasa o algodón húmedos, pequeños trozos de hielo);
· Hacer partícipe al paciente en la elección de sus alimentos y ofrecer pequeñas porciones. Pueden ofrecerse alimentos líquidos con un alto aporte calórico (licuado, dieta polimérica);
· Ofrecer alimentos fáciles de deglutir; y
· Brindar compañía al paciente mientras come e intentar brindar alimento en una habitación distinta al área de descanso. (2)
Alimentación e hidratación. Cuando se habla sobre la Alimentación y la Hidratación en Cuidados Paliativos, muchas veces se traslada a los dilemas éticos que estos temas presentan sobre todo en la etapa final de la vida. Sin embargo, hay que recordar que este tipo de cuidados no sólo se brinda al final de la vida, si no desde el momento del diagnóstico de enfermedades que limitan o amenazan la vida; y es en este mismo tenor que la alimentación artificial (entendida como aquella que requiera de algún dispositivo como sondas oro/nasogástricas, de gastrostomía o de forma parenteral) puedan ser consideradas para los niños que tienen pronóstico que puede extenderse por meses incluso años. (3)
Hay que recordar que proveer alimento, es una forma muy instintiva de cuidado por parte de los padres, especialmente de la madre, por lo que hacer ajustes para poder cubrir esa necesidad sin que esto implique un disconfort o genere algún tipo de sufrimiento en el niño.
En los más pequeños siempre se favorecerá la alimentación al seno materno de ser posible. En niños mayores que pueden ingerir alimento de forma oral se aconseja que los platillos no sean muy especiados (sobre todo en el paciente que recibe quimioterapia) o picantes, que se presenten en formas atractivas y fraccionar en porciones pequeñas varias veces por día. Hacer del momento de la comida un tiempo agradable.
La Hidratación, se rige por los mismos principios que la alimentación. Al final de la vida no hay que hidratar de manera artificial, se puede administrar pequeñas cantidades con jeringa incluso con un gas o un algodón mojado pasando sobre los labios del paciente. (4)
Siempre hay que tener en cuento en la etapa final de la enfermedad que tanto la nutrición como la hidratación, administradas de forma artificial, constituyen intervenciones que pueden ser retiradas al igual que otras actividades que son parte del soporte vital siempre y cuando haya un consenso de que el continuar con estas medidas no proporciona un beneficio real para el paciente, lo cual afectaría el interés superior del niño. (5,6)
5.3 SÍNTOMAS RESPIRATORIOS
Disnea. Sensación desagradable y consciente de dificultad para respirar. Suele ser uno de los síntomas más temidos y estresantes, frecuentemente acompañada de ansiedad.
Se presenta en el 40 a 65 % de los niños con enfermedades malignas. (1)
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Opioides Mejoran la sensación subjetiva de falta de aire, sin alterar el ritmo respiratorio. | 1. Paciente virgen de opioides: Morfina 30 a 50 % de la dosis inicial para dolor. VO 0,1-0,25 mg / kg / dosis IV 0,05-0,1 mg / kg / dosis cada 2 a 4 hrs Nebulizado: 2,5-5 mg / 3 ml de suero fisiológico en nebulización cada 4 hrs 2. Paciente con opioides: se titula, como para el dolor, con aumentos entre 30 a 50 % de la dosis previa. (2) Es importante proveer alivio anticipatorio con dosis de rescate de opioides (10 % de la dosis diaria total), ante posibles exacerbaciones de la disnea. | Depresión respiratoria. Estreñimiento Retención urinaria. Náuseas y vómito *la morfina en nebulización puede causar bronco-espasmo intenso y empeorar la disnea. Podría ser preferible el fentanilo en nebulización. (2) |
| Benzodiazepinas Se usan en combinación con opioides por sus efectos sedativos y ansiolíticos. Son un grupo de drogas que reducen la ansiedad, proveen sedación y mejoran el sueño. Su utilización está indicada ante la presencia de ansiedad asociada, o no, con crisis de pánico. Su uso específico para alivio de la disnea sin estos síntomas no ha sido demostrado. (3) | Midazolam subcutáneo o intravenoso para sedación ante la presencia de síntomas refractarios y de intensidad insoportable para el paciente (crisis de asfixia, hemoptisis masiva). Dosis inicial de 50 a 100 mcg/kg/hr en infusión continua. Clonazepam (usualmente la presentación en gotas es más sencilla de usar) 0.01 a 0.05 mg/kg/día cada 8 a 12 hrs. (2) | Aumento excesivo de secreciones, broncorrea. Sedación profunda. (2) |
Estrategia no farmacológica
Crear un ambiente confortable con medidas simples, tales como:
· Mantener ventanas abiertas;
· Evitar la presencia de muchas personas en la habitación;
· Eliminar los irritantes ambientales;
· Introducir humidificación;
· Brindar educación y soporte a la familia;
· Enseñar ejercicios respiratorios y de relajación; (3)
· Oxígeno; y
· Su uso en disnea es controvertido, pero se ha observado que a algunos pacientes les puede funcionar. (3)
Broncorrea y estertores. Sensación desagradable y consciente de dificultad para respirar. Suele ser uno de los síntomas más temidos y estresantes, frecuentemente acompañada de ansiedad.
Se presenta en el 40 a 65% de los niños con enfermedades malignas. (4)
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Butilhioscina | 0.3-0.6 mg/kg/día en cuatro dosis, en niños mayores de 12 años 10 mg cada 6 horas. | Los efectos secundarios son los propios del bloqueo muscarínico, siendo xerostomía, taquicardia, retención aguda de orina y glaucoma los más frecuentes. |
| Haloperidol | Dosis: 0,01-0,02 mg/kg/dosis v.o., s.l., v.r. cada 8-12 hrs | Resulta de elección por su acción anticolinérgica que reduce las secreciones respiratorias. |
| Acetilcisteína | Niños entre 2 y 7 años: La posología recomendada es de 300 mg de acetilcisteína al día por vía oral, en 3 tomas de 100 mg cada 8 hrs | No asociar Acetilcisteina con antitusígenos ni anticolinérgicos. |
| Erdosteína | Niños de 7 años o más: 200 mg / 8 horas o 600 mg/24horas. Dosis ponderal: 10 mg/kg/día, cada 12 hrs VO | |
| Atropina | (1% o 10mg/ml) gotas | Escopolamina y atropina ocasionan confusión y disminución del nivel de consciencia con mayor frecuencia ya que atraviesan la barrera hematoencefálica. (5) |
Estrategia no farmacológica
· Posicionamiento del paciente;
· Cambios posturales laterales o en semiprono para facilitar el drenaje postural de secreciones; y
· Succión oral suave para la eliminación de secreciones ubicadas en la cavidad oral. (6)
Tos. Mecanismo de defensa para permeabilizar la vía aérea, reflejo medido por el nervio vago.
Es un síntoma raro en niños de cuidados paliativos pediátricos, la tos suele deberse a una infección (aguda o crónica), aspiración (especialmente en niños con problemas de deglución), reflujo gastrointestinal y, en ocasiones, enfermedad maligna.
Una tos eficaz depende tanto de la tenacidad de la mucosa como de la capacidad de crear una velocidad adecuada de la corriente de aire.
La incapacidad para producir una tos eficaz puede provocar una tos persistente y angustiosa, que puede afectar negativamente al sueño y contribuir a los síntomas de náuseas, dolor y disnea. (7)
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Morfina | Recién Nacidos, lactantes y niños. IV. SC. Bolos: 0.05-0.1 mg/kg cada 2-4 hr Oral: 0.15-0.3 mg/kg cada 4 hr.6 u 8 hrs. Infusión: 0.03 mg/kg/h o 0.2-0.5 mg/kg/día | Es probable que los opioides sean el medicamento más eficaz en el tratamiento paliativo de la tos seca persistente. |
| Oxicodona | Lactantes. Oral: 50 a 125 mcg/kg/4 hrs 1 a 8 años. Oral: 125-200 mcg/Kg/4 hrs (Máximo de 5 mg/dosis) Liberación inm. Mayores de 8 años. Oral 5 mg cada 12 hrs. (Liberación prolongada) También se pueden utilizar Agonistas B2 y Anticolinérgicos en casos especiales. (9) | La práctica aceptada es utilizar entre el 25% y el 50% de la dosis de dolor. (8) |
Estrategia no farmacológica
· Intervenciones dirigidas a una causa específica, por ejemplo: niño con enfermedades neurológicas, debilidad muscular o que han recibido alimentación asistida;
· Reducir los volúmenes de alimento y / o comenzar la alimentación continua puede ser una intervención eficaz, junto con o en lugar de antiácidos y procinéticos;
· Los niños con problemas de deglución, la tos secundaria a la aspiración puede reducirse modificando la técnica de alimentación o cambiando de alimentación oral a nasogástrica (o gastrostomía);
· El tratamiento de la infección y el manejo del broncoespasmo es particularmente importante en niños con enfermedades respiratorias, como fibrosis quística; (9) y
· En general se ha de procurar una ventilación correcta de la habitación, aire fresco, evitar irritantes, humidificación ambiental, hidratación oral suficiente, facilitar expulsión de secreciones. (10)
Hemoptisis. Expectoración de sangre procedente del tracto respiratorio bajo (pulmón o bronquios). Es necesario diferenciarla del sangrado orofaringeo y de la hematemesis (sangrado de origen gastrointestinal). (11) En cuidados paliativos se observa con mayor frecuencia en niños con neoplasias hematológicas, alteración de la coagulación por otras causas como, por ejemplo, en coagulación intravascular diseminada e infección respiratoria. Puede ser extremadamente aterrador para el niño y los padres. Incluso una pequeña cantidad de esputo con manchas de sangre puede generar temores de que pueda seguir una hemorragia grande y más significativa. (8)
Estrategia famacológica. El manejo es a base de: Adrenalina nebulizada (1mg/1ml=1/1.000), 0,3-0,6 mg/kg. Dosis máxima de 6 mg. Disolver en sol. salina hasta 10 ml. Flujo 5 l/min. Estar preparados en caso de ser necesario, para realizar una sedación de emergencia. (11) Ver capítulo de sedación paliativa.
Estrategia no farmacológica
· Disponer en la cabecera del paciente una palangana y toallas de color oscuro para comprimir el punto de hemorragia y absorber y disimular la sangre; y
· Colocar al paciente en decúbito lateral en caso de hematemesis o hemoptisis para prevenir el ahogamiento. (11)
El tratamiento de los episodios debe ser individualizado y depende de diversos factores como la posibilidad de reversión o control de la causa del sangrado, la existencia de episodios previos y su respuesta al tratamiento recibido, la situación clínica, el pronóstico vital del paciente, el tratamiento endoscópico o quirúrgico rara vez está indicado al final de la vida, pero debe considerarse en niños que se prevé que tengan un pronóstico más prolongado. (12)
5.4 SÍNTOMAS GASTROINTESTINALES
Mucositis. La mucositis oral es una condición inflamatoria común que afecta la mucosa de los tejidos del tracto gastrointestinal y es secundaria a muchos tratamientos para oncológicos. (1-5) La morbilidad por mucositis está asociada principalmente al dolor que produce debido a la inflamación y a la ulceración de la mucosa. Afecta negativamente a la alimentación, así como a la administración de medicamentos vía oral, mantenimiento de la higiene bucal y a la calidad de vida. (2,3)
Puede afectar el resto del tracto gastrointestinal como en la esofagitis y proctitis por radiación. Presente en 35-40% de los niños en quimioterapia citotóxica. Niños en trasplante de médula ósea, niños neutropénicos con niveles elevados de creatinina y con poco peso conllevan mayor riesgo (>70%) (2,3,5)
Causas:
· Quimioterapia con alto riesgo para MO: Bleomicina, cetuximab, cytarabina, soxorrubicina, etoposido (altas dosis, erlotinib, severolimus, fluorouracilo, metrotexate (dosis bajas) sorafenib, sunitinib; (3) y
· Radiación, en particular cabeza y cuello y Tracto GI. La siguiente es una escala que permite evaluar el grado de daño.
Escala Toxicidad Oral (OMS): (5)
Grado 1 (dolor y/o eritema);
Grado 2 (eritema, úlceras, disminución de la ingesta);
Grado 3 (úlceras, eritema, imposibilidad de ingesta);
Grado 4 (mucositis extensa, la alimentación no es posible).
Estrategia farmacológica (1-7) De manera general, el tratamiento consiste en control sintomático, cuidado oral y protección de la mucosa que ayude a regeneración tisular.
· Mantener la hidratación y utilizar la vía intravenosa para asegurar volumen;
· Control del dolor: paracetamol en dolor leve u opioides sistémicos para dolor moderado a intenso. La morfina es opioide de elección (Ver Dolor; Morfina). Existe un soporte limitado para el uso de morfina en enjuague oral, aunque se ha utilizado a dosis bajas;
· Uso de enjuagues: Ya sea en monoterapia o combinados, se utilizan agentes protectores como el hidróxido de aluminio y magnesio, carbonato de calcio, analgésicos (morfina), antihistamínicos (difenhidramina) y anestésicos tópicos (lidocaína, benzocaína). Clorhexidina no está indicado para prevención o tratamiento, pero puede ayudar para limpieza oral; e
· Infecciones: La colonización infecciosa de las úlceras por microorganismos puede llevar a infecciones sistémicas y exacerbar la severidad de la mucositis. En pacientes con datos de infección según sea la sospecha diagnóstica deben prescribirse antimicóticos (clotrimazol, nistatina) en caso de candidiasis; antivirales (aciclovir, valaciclovir) en sospecha de Virus del Herpes Simple e inmunocompromiso y/o antibióticos (sospecha de infección bacteriana, amoxicilina/clavulanato).
De acuerdo con el grado en la escala OMS, se propone como manejo. (7)
Grado 1: Enjuagues para alcalinizar el medio, analgésicos;
Grado 2: Enjuagues alcalinizantes; bencidamina en concentración del 0,15%, 15 ml cada 2-3 horas;
Grado 3: Enjuagues alcalinizantes, bencidamina, antimicóticos, analgésicos, valorar hidratación intravenosa; y
Grado 4: Alimentación enteral o parenteral, hidratación y analgésico vía intravenosa, así como antibióticos según sospecha.
Estrategia no farmacológica (3-7)
· Limpieza de cavidad oral frecuente;
En menores de tres años, con solución salina o agua con bicarbonato de sodio. En mayores de tres años, con cepillo suave en dientes, encías, paladar y lengua;
· No utilizar enjuagues con alcohol;
· Dieta suave o líquida según sea tolerada, evitando alimentos salados, secos o ácidos que requieran mucha masticación;
· Alimentos blandos, paletas heladas y los helados de agua pueden ser calmantes para las úlceras; y
· Láser de baja potencia nueva opción terapéutica.
Nausea y vómito. Ocurren en 16-78% de los pacientes, en particular en la última semana de vida. (9,10)
Náusea. Sensación displacentera de necesidad de vomitar acompañada de síntomas autonómicos como palidez, sudoración fría, salivación, taquicardia y diarrea. Náusea Crónica: >1 semana sin una causa bien definida o autolimitada. (1,3,8-10)
Vómito. Proceso complejo de espasmos involuntarios de los músculos diafragmáticos y abdominales que dan por resultado el reflujo del contenido gástrico a través de la boca. (1,3,8-10)
Causas: Ansiedad, disfunción autonómica, obstrucción intestinal, constipación, gastroéstasis, infecciones, incremento de la presión intracraneal, dolor, medicamentos (antibióticos, AINE, quimioterapéuticos, opioides, abstinencia o intoxicaciones); desórdenes metabólicos (hipercalcemia, daño renal), radiación, reflujo.
Fisiopatología: De acuerdo al área o áreas involucradas, se consideran:
· Corteza Cerebral, induce vómito por ansiedad, aromas y sabores, incremento de presión intracraneal, se usan esteroides para disminuir PIC y ansiolíticos para ansiedad anticipatoria y sobre estimulación olfativa;
· Vestibular, activada por movimiento, zona sensibilizada por opioides; mediada por histamina y acetilcolina; se utilizan antihistamínicos y anticolinérgicos;
· Estimulación del tracto Gastrointestinal, vías vagal y simpática, mediadas por D2, acetilcolina y 5-TH. Se utiliza metoclopramida y anticolinérgicos; y
· Fallo autonómico, genera gastroparesia y por tanto náusea, constipación, anorexia y saciedad temprana; se presenta en IRC, desórdenes neurológicos, caquexia, VI).
Evaluación: (3,9) Considerar el grupo etario del paciente, el inicio (abrupto o insidioso), el patrón del vómito, tiempo posterior a la ingesta en el que se presenta, material del vómito, síntomas asociados y la evaluación física para llegar a una sospecha clínica diagnóstica y actuar en consecuencia.
Puede utilizarse en la evaluación de mayores de 7 años la Escala BARF (Baxter Retching Faces) validada en español:
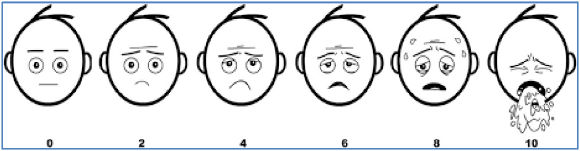
Escala BARF (Baxter Retching Faces)
Estrategia farmacológica. Prevención. Se recomienda la administración profiláctica de acuerdo al potencial de la quimioterapia para inducir nausea y vómito, el cual, en ausencia de profilaxis y de acuerdo a prevalencia se considera:
· Alto (>90%);
· Moderado (30-90%); y
· Bajos (10-30%). (10)
Abordaje: Es necesario evaluar y atender las consecuencias de vómito prolongado como la deshidratación y los desequilibrios hidroelectrolíticos; de ser posible es necesario tratar las causas potencialmente reversibles de la náusea o el vómito.
De acuerdo con la fisiopatología de la náusea y el vómito, elegir el(los) fármaco(s) (8,10)
Primera Línea:
· Antagonista de receptor 5HT3 (ondansetrón) y/o;
· Antagonista de receptor D2 (metoclopramida) y/o;
· Antagonistas de histamina y acetilcolina (difenhidramina).
Segunda Línea:
· Considerar añadir un corticosteroide (dexametasona) en un pulso corto;
· Añadir dosis baja de benzodiacepinas; y
· Sustituir fármacos de primera línea por otro de su misma clase (ejem. granisetrón, haloperidol, difenhidramina)
Tercera Línea:
· Considerar aprepitant;
· Considerar cannabinoides de acuerdo con aprobación (dronabinol); y
· Considerar dosis bajas de propofol.
·
| Fármaco | Dosis | Consideraciones | |
| Antagonista Receptor de Serotonina 5HT3 | Ondasetrón > 1 mes | 0.1-0.15 mg/kg c/6-8 h; VO, SL, IV; Max. 4-8 mg dosis. Dosis alta: 0.45mg /kg 30 minutos previo a la quimioterapia emetogénica, Max:16 mg dosis Adultos 4-8 mg; VO, SL, IV | Puede inducir náusea a dosis altas. Efectos adversos: cefalea, constipación |
| Granisetrón | 0.01-0.05 mg / kg c/8 h; VO, IV; Max. 3 mg/dosis. | ||
| Antagonista Receptor de Dopamina D2 | Metoclopramida | 0.1-0.2 mg/kg c/8 hrs. VO, IM, IV Adultos: 10 mg c/ 6-8 hrs VO/IM/IV 1mg/kg para D2 antagonismo o nausea inducida por quimioterapia. | De elección en nausea por estasis gástrica. 5HT4 agonista (a altas dosis). Procinético, uso si se presenta gastroparesia. Extrapiramidalismo a menor edad, difenhidramina puede utilizarse para prevenir, sin disminuir la eficacia antiemética. Altas dosis pueden generar discinesia tardía irreversible. Contraindicada en obstrucción intestinal completa. Efectos Adversos: Sedación, confusión. |
| Haloperidol > 3 años | 0.01 - 0.1 mg/kg; c/8 h. (Titular lentamente, Max. 1-2mg/kg, 100mg/dosis Adulto: 0.5-1 mg q/12 h o c 4-6h PRN VO, SL, IM, SC, Inyección > 18 años. | Acción en la Zona quimiorreceptora activadora de la náusea (CTZ). Potente D2 Antagonista; menos sedación. Reservar el uso en menores de 3 años que no responden a otros antieméticos. Efectos adversos: prolongación de intervalo QT, disminución del umbral convulsivo, extrapiramidalismo. | |
| Domperidona | 0.2 - 0.4 mg/kg; c /4-8 h. Max: 10mg | No cruza barrera hematoencefálica y por tanto no produce extrapiramidalismo. | |
| Antagonista receptores Histamina (H1)/ muscarinico acetilcolina (AChm) | Dimenhidrato >2 años | 1.25 mg/ kg c/6-8 h; VO, IM; Max: 2-5 años: 75 mg/día 6-12 años 150 mg/día Adultos 50-100 mg; VO, IM, IV; Max. 400 mg/día | Nausea Vestibular Efectos Adversos: Excitación paradójica, constipación, sedación. Se han reportado eventos adversos serios en < 2 años (convulsiones, depresión respiratoria) *Hidroxicina, actúa en la Zona Cortical de náusea y ansiedad (ansiolítico) |
| Difenhidramina >2 años | 0.5-1 mg/kg c/4-6 h; VO, IM, IV; Max. 50 mg/dosis Adultos 25-50 mg; VO, IM, IV; Max. 300 mg/día | ||
| Hidroxizina * >2 años | 0.5-2 mg/kg por día, en niños hasta de 40 kg. VO Adulto: 1 -25 mg; VO, IM. | ||
| Antagonista receptores muscarínico acetilcolina (AChm) | Butilhioscina Escopolamina (Buscapina) | 0.01 mg/kg c/6h; VO, IV. | *Solo antimuscarínico (no antihistamínico) Efectos adversos anticolinéricos, sedación. |
| Antagonista receptores de Dopamina (D2) e Histamina (H1)/ muscarinico acetilcolina (AChm) | Clorpromazina | 0.5-2mg/kg VO; 0.25-1mg/kg infusión lenta IV. | Fenotiazina, con efectos psicotrópicos. Efectos Adversos: Extrapiramidalismos y anticolinéricos, agranulocitosis. |
| Antagonista receptor Neurokinina 1 | Aprepitant | > 12 años: 40mgs VO dosis única. (Prequirúrgica) 125 mg VO dosis única, seguido de 80 mg una vez al día (Quimioterapia) | De elección en nausea asociada a quimioterapia. Efectos Adversos: Constipación, cefalea, fatiga y taquicardia sinusal. |
| Abreviaturas: AChm (Receptor muscarínico acetilcolina); D2 (Receptor de Dopamina 2); h (hora); H1 (Receptores Histamina 1); IM (Intramuscular); IV (Intravenosa); Max (Máxima dosis); PIC (Presión Intracraneal); SC (Subcutánea); SL (Sublingual); VO (Vía oral); 5HT3 (Receptor de Serotonina 3). | |||
Estrategia no farmacológica (1,3,8-10)
· En caso de deshidratación utilizar el Esquema de Hidratación Oral;
· Ofrecer líquidos claros, ingeridos lentamente y con cuchara; la alimentación debe ser con porciones pequeñas y frecuentes;
· Evitar desencadenantes como aromas y alimentos irritantes;
· Promover el cuidado de la cavidad oral;
· Hipnosis, desensibilización; y
· Acupuntura / Acupresura.
Estreñimiento / constipación. Es la disminución en la frecuencia de la emisión de heces, cualquiera que sea su consistencia o volumen. En ocasiones con dolor y pujo excesivo.
Causas: (1,3,8,9) Generalmente multifactorial, pudiéndose combinar algunos de los siguientes mecanismos: a) Funcional; b) Alteraciones neurológicas (Enf. Hisrchprung, lesiones medulares, parálisis cerebral infantil, neurofibromatosis, neuropatías y miopatías, encefalopatías); c) Patología anal (fisuras, estenosis, malformaciones); d) Trastornos endócrinometabólicos (hipotiroidismo, hipocalemia, hipercalcemia, deshidratación, fibrosis quística); e) Medicamentos: Opioides, antidepresivos tricíclicos, antiepilépticos, fenotiacinas, diuréticos, antihistamínicos, anticolinérgicos, suplementos de hierro).
Evaluación: (3) Se utiliza a los Criterios de Roma III para definir la presencia del síntoma:
· Dos o menos deposiciones a la semana;
· Al menos, un episodio de incontinencia fecal a la semana (en los menores de cuatro años, tras haber alcanzado el control del esfínter anal);
· Antecedente de posturas o actitudes retentivas para evitar la defecación;
· Defecación dolorosa;
· Fecalomas en el recto; y
· Deposiciones muy voluminosas.
Abordaje:
· Evaluación que incluya la presencia de otros síntomas asociados tales como dolor abdominal, distensión, flatulencia, nausea o vómito;
· Una exploración física integral y los paraclínicos aplicables;
· Tratamiento de causas subyacentes.
Estrategia farmacológica. (1,3,8,9) De forma general se inicia con un ablandador de heces y si es necesario añadir un estimulante.
· En caso de exploración con ámpula rectal llena, datos de impactación fecal y ausencia de complicaciones utilizar un enema o supositorio de glicerina para desimpactar; y
· En el caso de constipación inducida por opioides, se ha estudiado en adultos la naloxona, metilnaltrexona, y almivopam sin reportes publicados aún para niños. (3)
| Tipo | Fármaco | Dosis | Consideraciones |
| Enemas3 | Enemas de fosfato Hipertónico. | No indicado en menores de 2 años En >6 años: 3 ml/kg, VR máx.: 35 ml | Se recomienda no usarlos más de cinco días. Efectos adversos: Riesgo de traumatismo mecánico y de hiperfosfatemia hipocalcemia y tetania. |
| Enema de Solución Salina Isotónica. | 5 ml/kg dos veces al día, VR | Se recomienda no usarlo más de cinco días. Efectos adversos: Riesgo de traumatismo mecánico. | |
| Osmóticos | Hidróxido de Magnesio | 1 a 3 ml/kg/día VO | Efectos Adversos: Diarrea intensa, hipermagnese-mia, hipofosfatemia e hipocalcemia. |
| Lactulosa | 3 m a 1 año: 0.8 - 3.5 ml VO (no por kilo) 3 veces día. > 1 año: 10mg - 3.5ml VO (no por kilo) 3 veces día. | Titular para evitar los efectos adversos. Efectos Adversos: Flatulencia, dolor abdominal, nausea, hipernatremia a altas dosis. | |
| Sorbitol | 60 mg/día >8 años: 10 mg/kg c/8 h; Max. 120 mg/día | Efectos Adversos: Flatulencia, dolor abdominal. | |
| Polietilenglicol | 2-12 años: 10-20ml/kg o 1- 2g/kg/día, VO en dos tomas durante 3 a 5 días, dejando transcurrir no más de 6-8 horas entre ambas dosis. >12 años: 4 sobres diarios VO e incrementara razón de 2 sobres/día hasta un máximo de 8 sobres al día. | Iniciar con por 10ml/kg (agua o jugo) e incrementar. Descontinuar en casos con dificultad para tomar. Efectos adversos: náusea, distensión abdominal, vómito, diarrea, irritación perianal. Neumonía por aspiración, edema pulmonar (polietilenglicol con electrolitos) | |
| Estimulantes | Senósidos | 6 meses a 1 año: 3.75 mg (no por kilo) VO al acostarse. 3-10 años: 7.5-15 mg (no por kilo) VO al acostarse >10 años: 15-30 mg (no por kilo) VO al acostarse | Efectos adversos: Dolor abdominal cólico. |
| Bisacodilo | 6 - 11 años: 5 mg (no por kilo) VO al acostarse. >12 años: 5-15mg (no por kilo) VO al acostarse | Efectos adversos: Dolor abdominal, diarrea e hipercalcemia, proctitis, urolitiasis | |
| Picosulfato de sodio | Sólo para desimpactación en niños >5 años: 2 a 6 gotas/día | Efectos adversos: Dolor abdominal, diarrea. Fenómeno de rebote con uso prolongado. | |
| Abreviaturas: VO (Vía oral) VR (Vía rectal). | |||
Estrategia no farmacológica (1,3,8,9) Cuando sea posible:
· Establecer una rutina intestinal diaria;
· Incrementar la actividad física activa o pasiva;
· Incrementar el volumen de líquidos;
· Incrementar cantidad de fibra en la dieta;
· Considerar masaje gentil del abdomen en sentido de las manecillas del reloj;
· Revisar medicamentos que pueden causar estreñimiento y adecuar prescripción; y
· Con demostrada utilidad la auto hipnosis, biofeedback y terapia cognitiva conductual.
Diarrea. Es el aumento en el número de deposiciones y/o una disminución en su consistencia. Se puede acompañar de signos y síntomas como náuseas, vómitos, fiebre o dolor abdominal. Diarrea aguda < 14 días; persistente >14 días; Crónica > 30 días. (1,3) Presente entre el 21-40% de los niños al final de vida. (8-11)
Causas: Pueden presentarse de manera individual o simultanea algunos de los siguientes mecanismos: (1,3,8)
· Incontinencia por rebosamiento en estreñimiento e impactación fecal;
· Intolerancia alimentaria;
· Errores en la alimentación enteral (tiempo, frecuencia, tipo de fórmula);
· Sobreuso de laxantes;
· Daño intestinal inducido por radiación;
· Síndrome de intestino irritable;
· Enfermedad inflamatoria intestinal (Crohn, CUCI);
· Malabsorción y esteatorrea por disminución de función pancreática;
· Infecciones bacterianas;
· Infecciones virales;
· Infecciones parasitarias; y
· Síndromes carcinoides o VIPomas.
Evaluación: Es imprescindible valorar el estado de hidratación generado por el síntoma, evaluar las causas precipitantes y de ser posible remitirlas. Según sea el caso, debe valorarse el equilibrio hidroelectrolítico de manera paraclínica.
| Estrategia Farmacológica (3,8) | ||
| Fármaco | Dosis | Consideraciones |
| Loperamida | 0.03-0.27 mg/kg VO dos veces al día. | Efectos Adversos: distensión, estreñimiento, efectos neurológicos centrales (en infantes), con el uso concomitante de inhibidores de P-Glicoproteina (ketoconazol, omeprazol, quinidina) que permite atravesar la barrera hematoencefálica. |
| Subsalicilato de Bismuto | 15-25 mg/kg, VO, 5-6 veces día | Datos limitados en pediatría. Precaución: Puede inducir Sx. Reye. Heces color negro. |
| Octreotide | 1-2 mg / kg, IV o SC, dos veces al día Titular el efecto a 10 mg/kg/dosis | Uso en diarrea secretora, que incluye síndromes carcinoides, tumores VIP y Diarrea por VIH. Evidencia limitada en pediatría. Efectos Adversos: nausea, empeoramiento de hipertonía arterial preexistente, colelitiasis, hipercontractilidad vesicular. |
| Colestiramina | 0-6 años: 1-2g VO dos veces al día > 6 años: 2-4 g VO dos veces al día | Uso en diarrea crónica. Dosis no ponderal |
| Abreviaturas: IV (Intravenosa; SC (Subcutánea); VO (Vía oral); VSO (Vida Suero Oral) | ||
Estrategia no farmacológica (1,3,8)
· Plan de hidratación oral con VSO, continuar con alimentación e ingesta de fluidos.
· En casos particulares evaluar la ingesta de lácteos o el cambio a deslactosados; y
· Prevenir la rozadura de piel con cuidado frecuente que mantenga la zona seca, aplicar cremas de barrera u pasta de óxido de zinc.
Hipo / singulto. Síntoma derivado de la contracción súbita e involuntaria del diafragma y los músculos intercostales, terminando con un cierre de glotis abrupto que produce el sonido característico. Generalmente auto limitado. El hipo prolongado puede ocasionar interrupción de la alimentación, habla, sueño.
Causas: (3)
· Benigno: (minutos-horas): Distención gástrica, alimentación excesiva, reflujo, areofagia, tabaco, alcohol;
· Persistente (2-3 días); Intratable (>1 mes); frecuencia alta >60 hipos/min:
· Sistema Nervioso Central (EVC, contusión cerebral, hematomas, encefalitis, meningitis, hidrocefalia,
neoplasias, trauma, ansiedad, esclerosis múltiple);
· Medicamentos (Estimulantes del SNC, sulfonamidas, Esteroides IV, benzodiacepina, antibióticos, analgésicos);
· Metabólico (hiponatremia, hipocalcemia, hipocapnia, gota, fiebre, falla renal, infección);
· SN Periférico (tumores de cabeza y cuello, masas pulmonares, bocio); y
· Quirúrgicas (ventilación inadecuada, intubación, hiperextensión de cuello, laparotomía, toracotomía, craneotomía, manipulación).
· Otros: hipnosis, acupuntura, masaje de cuello.
Estrategia farmacológica. El tratamiento debe estar basado en la casusa subyacente cuando esta es identificada. Las medidas farmacológicas se reservan para el hipo persistente o intratable. Se describe carbamacepina, gabapentina y valproato como opciones de tercera línea. En hipo refractario, puede requerirse sedación paliativa (midazolam).
| Fármaco | Dosis | Consideraciones |
| Clorpromacina >6 meses | > 6 meses: 0.5-1 mg/kg/dosis c/4-8 hrs VO, IM, IV. Max: < 5 años o 23 kg: 40mg/día. 5-12 años: 75 mg/día; VO, IM, IV. Adultos: 25-50 mg c/6-8 h; VO, IM, IV | Indicado en hipo de origen central. Precaución en condiciones patológicas cardiovasculares, renales, hepáticas, convulsivas o respiratorias. Efectos Adversos: Disminución del umbral convulsivo, extrapiramidalismo. |
| Metoclopramida | 0.1-0.2 mg/kg c/8 hrs VO, IM, IV Adultos: 10-20 mg c/6-8 hrs VO/IM/IV | Fármaco procinético, promueve el vaciamiento gástrico; antihemético. Útil en Hipo asociado a distención gástrica Contraindicación: Obstrucción intestinal completa. Se requiere ajuste de dosis para ClCr <50 Efectos Adversos: Confusión, extrapiramidalismo, sedación, disminución del umbral convulsivo. |
| Baclofeno | Administración VO, IV < 2 años: 2.5- 5 mg c/8hrs; Max. 40mg/día. < 2-7 años: 5- 10 mg c/8hrs; Max. 60 mg/día. > 8 años: 10 m g/kg c/8 h; Max. 120 mg/día. Adultos: 10-20 mg c/8-12 h; Max. 80 mg/día | Genera relajación muscular Titular dosis cada tres días |
| Omeprazol >1 año | >1 - 5 años: 0.7 mg/kg/día. < 6 años: 1 mg/kg cada 12 - 24 h 5-10 kg: 5 mg/día 10-20 kg: 10 mg/día > 20kg: 20 mg/día > 16 años: 20 mg/día. Max. 40mg/día | Indicado en hipo asociado a reflujo. Pueden requerirse incremento de dosis en niños de 1-6 años por aclaramiento incrementado. Ajustar dosis en daño hepático. Efectos Adversos: edema, Foto sensibilidad, trombocitopenia |
| Pantoprazol >1 año | Niños: 20 mg/día (0.5-1 mg/ kg/día); VO/IV Adultos: 40 mg/día por 8 semanas VO; IV (uso < 10 días) | En hipo asociado a reflujo. Datos de uso en niños, son limitados. |
| Abreviaturas: EVC (Evento Vascular Cerebral); IM (Intramuscular); IV (Intravenosa); SC (Subcutánea); PaCO2 (Presión arterial de dióxido de carbono); SNC (Sistema Nervioso Central); VO (Vía oral). | ||
Estrategia no farmacológica
· Maniobras respiratorias que incrementen PaCO2: Aguantar la respiración, respirar en una bolsa, maniobra de valsalva, estornudar o toser, jadear, presión positiva continua de la vía aérea;
· Estimulación nasofaringea: presión de la nariz, beber agua;
· Alivio de la distención gástrica: ayuno, sonda nasogástrica;
· Maniobras vagales: valsalva, opresión ocular, masaje carotideo;
· Intervencionismo: bloqueo del frénico.
5.5 SÍNTOMAS NEURO-PSIQUIÁTRICOS
Espasticidad. Aumento anormal del tono muscular que característicamente es velocidad dependiente (es decir, a mayor velocidad de estiramiento muscular pasivo, mayor resistencia se encontrará), el cual se asocia generalmente con debilidad muscular y reflejos exaltados. La etiología es una lesión del tracto corticoespinal.
Causas: La parálisis cerebral infantil es la causa más común de la espasticidad en niños; otras causas son: traumáticas, isquemia, tumores, enfermedades neurodegenerativas. (1, 2)
Debe ser tratada por un equipo de profesionales multidisciplinario.
Evaluación: De acuerdo con la extensión de su afectación y para su tratamiento se clasifica en:
· Focal o segmentaria: Afecta a un área del cuerpo aislada (brazo o pie); y
· Generalizada: afecta a múltiples áreas del cuerpo aisladas o no contiguas.
Estrategias farmacológicas. Para el tratamiento se considera el tipo de espasticidad:
· Espasticidad generalizada: Indicados fármacos orales; primera línea baclofeno y benzodiacepinas, segunda línea dantrolene y tizanidina; y
· Espasticidad focal o segmentaria se sugiere la administración de toxina botulínica (por profesionales experimentados en su manejo).
Los objetivos del tratamiento de la espasticidad son:
· Mejorar la función (marcha, uso de la mano, etc.);
· Optimizar el cuidado (ej. administración en músculos de la cadera para mejorar el cambio de pañal); y
· Evitar fracturas, contracturas fijas de las articulaciones y dolor.
Tratamientos intervencionistas: bloqueo nervioso con fenol, rizotomía dorsal o colocación de bomba de baclofeno intratecal.
| Fármaco | Dosis | Consideraciones | |
| Baclofeno | VO 0.5 mg/kg/día en 2 ó 3 dosis al día, con incrementos semanales hasta lograr efecto deseado; Máx. 2 mg/kg/día. En niños mayores o adolescentes, puede iniciarse 5 mg dos o tres veces al día e incrementar hasta 40 - 80 mg/día repartida en 3 dosis. (4) | Efectos adversos frecuentes: sedación, constipación, retención urinaria y nausea; Menos frecuentes: confusión, hipotonía, ataxia y parestesias. Cuidados particulares: no debe suspenderse súbitamente, existe riesgo de abstinencia con crisis convulsivas y alucinaciones, hipertermia | |
| Benzodiadiacepinas3 | Diazepam | Vía oral en dosis -0.3 mg/kg/día dividido en 2 a 4 dosis (máximo 10 mg/dosis), titulación gradual hasta efecto (dosis máxima no bien establecida, se ha considerado 0.8 mg/kg/día) | Efectos adversos: somnolencia, ataxia, alteraciones de memoria, sialorrea y dependencia. Debe procurarse que el tratamiento con benzodiacepinas tenga un curso corto e incluso ser usado como medicamento "de rescate" en casos de espasmos musculares. En caso de necesitar terapia a largo plazo con ellas, es preferible el uso de clonazepam, cuya vida media es más larga. |
| Clonazepam | VO 0.01 - 0.3 mg e incrementos graduales en 0.2 mg/kg/día cada 3 días. (5) | ||
| Agonista alpha-2-adrenérgico central | Tizanidina | Dosis de inicio: De 2 a 10 años: 1 mg/c-24 hrs. por la noche. >de 10 años 2 mg/c-24 hrs por la noche con incrementos semanales hasta dosis máxima de 0.3-0.5 mg/kg/día fraccionado en 2 a 4 dosis en 24 hrs. (4) | Efectos adversos más comunes: hipotensión, mareo, astenia, xerostomía, toxicidad hepática. |
| Clonidina1 | Días 1-3: 0.002 mg/kg (0.1 mg) VO, por la noche. Días 4-6: 0.002 mg/kg, dos veces al día. Días 7-9: 0.002 mg/kg tres veces al día. Incrementar cada 2-4 días 0.002 mg/kg hasta efectividad o efectos adversos. * | Efectos adversos: Gastrointestinales (sequedad de boca, estreñimiento, dolor abdominal, anorexia, náuseas, vómitos); Cardiovasculares (Bradicardia, hipotensión ortostática, palpitaciones, arritmias, bloqueo auriculoventricular, sincope, fenómeno de Raynaud.) SNC (letargia, somnolencia, mareos, cefalea, sedación, depresión, cambios en el comportamiento, alteraciones del sueño, irritabilidad); trastornos generales (cansancio, depresión respiratoria). | |
| Abreviaturas: Dosis Máxima (Máx); Vía Oral (VO) | |||
Estrategia no farmacológica. Es indispensable ofrecer terapia ocupacional y física (pasiva y/o activa).
Crisis convulsivas. Se definen como la aparición transitoria de signos y / o síntomas debido a una actividad neuronal excesiva o sincrónica en el cerebro; (2) son un síntoma común en una mayoría de los niños, niñas y adolescentes con enfermedades avanzadas, ya sea por padecer enfermedades neurológicas o como un signo de lesión agregada secundaria a otra enfermedad (ej. Hipoxia isquemia, secuelas de neuroinfección, efectos adversos de fármacos).
Las manifestaciones pueden ser variadas: alteración del estado de alerta, sensoriales, motoras y autonómicas. Las crisis convulsivas, por sus manifestaciones clínicas se clasifican de la siguiente manera: (6)
a. Inicio focal:
· Con conciencia alterada / Con conciencia preservada;
· Inicio motor / Inicio no motor; y
· Focal a bilateral tónico - clónica (reemplaza el término previo de "secundariamente generalizada").
b. Inicio generalizado:
· Motor: tónico - clónico, otro motor; y
· No motor: ej. ausencia.
c. Inicio desconocido:
· Motor: tónico - clónico, otro motor; y
· No motor.
d. No clasificada.
Las crisis focales pueden ser determinadas clínicamente cuando existe un síntoma delimitado a una topografía cerebral específica (ej. movimientos clónicos de una extremidad o un hemicuerpo, parestesias, percepción de un sonido particular) o solo la alteración de la conciencia generalmente sin pérdida del tono corporal. Esto será el único signo presente durante la crisis o será el inicio de una descarga que se propagaría al hemisferio contralateral ocasionando una crisis generalizada en la cual ya existe una alteración del estado de alerta (generalización secundaria).
El auxiliar para estudiar las crisis convulsivas es el electroencefalograma. En él se puede llegar a observar el sitio donde se originan las descargas. Aun así, la diferenciación de un tipo de crisis u otra puede ser difícil.
Muchos pacientes pediátricos susceptibles de cuidado paliativo han sido diagnosticados con epilepsias refractarias por un neurólogo. Algunos ejemplos son: ej. Síndrome de West, Síndrome de Lennox Gastaut, epilepsias secundarias a disgenesias cerebrales; el manejo farmacológico conlleva importantes aspectos que requieren un adiestramiento específico.
Estrategia farmacológica. Los fármacos más accesibles y que cubren el mayor número de crisis son: fenitoína, ácido valproico y levetiracetam. A manera de recordatorio, la carbamazepina y oxcarbazepina son exclusivos para crisis focales. La lamotrigina y el topiramato son utilizados para crisis focales y algunos tipos generalizados.
El fenobarbital se utiliza exclusivamente en el período neonatal. Sin embargo, aun cuando no hay recomendaciones formales para ello, el fenobarbital puede ser utilizado en el contexto de una enfermedad muy avanzada y/o final de vida ya que tiene alta eficacia antiepiléptica y efecto sedante. Por esto último, además de sus efectos adversos cognitivos es lo que limita su uso en otros contextos.
Neuroirritabilidad (6,7) Se define como estado conductual irritable, difícil de consolar, en un paciente con daño neurológico grave (DNG). Las causas del DNG pueden ser: malformaciones del sistema nervioso central, asfixia perinatal, secuelas de encefalopatía hipóxico-isquémica, enfermedades genéticas (ej. Síndrome de Rett) o metabólicas (enfermedades mitocondriales, leucodistrofia de Krabbe, aciduria glutárica, etc).
La neuroirritabilidad obedece a una alteración de la percepción y modulación de los estímulos dolorosos y de la regulación autonómica. Repercute en la calidad de vida del paciente y de la familia, ocasionando trastornos del sueño, del estado de ánimo, frustración y claudicación del familiar.
Cuadro clínico: llanto generalmente de tono agudo y a veces inconsolable, irritabilidad y agitación psicomotriz asociado o no a posiciones anormales (opistótonos), manifestaciones vegetativas (distermia, piloerección, diaforesis), dolor o incomodidad, permanencia de reflejos primitivos con reactividad excesiva a estímulos sensoriales, alteraciones del sueño, del tono (hipertonía, distonía).
Se sospecha cuando la irritabilidad no se atribuye a ninguna de las causas comunes de dolor o disconfort en niños con DNG. Para ello se debe realizar un abordaje sistematizado para cubrir las causas de dolor en pediatría y las que son más frecuentes en niños con DNG.
· Gastrointestinales: abscesos periodontales, reflujo gastroesofágico, constipación, intolerancia alimentaria secundaria a trastornos de la motilidad gastrointestinal, pancreatitis (pacientes con ácido valproico). Existe un fenómeno llamado hiperalgesia visceral. Se refiere a la hipersensibilidad del tracto gastrointestinal a estímulos normales como el aumento de la presión intraluminal y se manifiesta con irritabilidad y cambios autonómicos (taqui o bradicardia, palidez o rubor, diaforesis) asociada a la alimentación, tránsito intestinal, flatulencias o evacuación; es especialmente frecuente en niños portadores de gastrostomía y/o funduplicatura;
· Osteomusculares: espasticidad, luxación de cadera, escoliosis, fracturas;
· Genitourinarias: infección de vías urinarias, litiasis ureteral (sospechar en pacientes con topiramato);
· Neurológicas: crisis epilépticas, dolor neuropático, espasmos musculares, disfunción autonómica con crisis diencefálicas o tormenta autonómica: son muchas veces ignoradas o confundidas con crisis convulsivas y por lo tanto tratadas incorrectamente, presentes en paciente con daño neurológico severo, incluso estado vegetativo. Consisten en eventos súbitos de diaforesis, posición extensora anormal, midriasis, hipertensión, fiebre y siempre taquicardia que puede durar hasta varios minutos. Pueden ser desencadenadas por estímulos dolorosos.
Abordaje y manejo:
· Descartar causas comunes de dolor o disconfort en pediatría y más frecuentes en niños con DNG;
· Dar tratamiento específico para todas ellas. Siempre considerar el tratamiento del dolor con AINE y/u opioide paralelo al tratamiento de la causa;
· Búsqueda intencionada de infección de vías urinarias y reflujo gastroesofágico. Puede ser útil brindar tratamiento empírico del reflujo con procinéticos, inhibidores de bomba de protones y antiácidos; y
· De no observar mejoría, iniciar manejo empírico con neuromoduladores: gabapentina o amitriptilina.
| Estrategias farmacológicas | ||
| Fármaco | Dosis | Consideraciones |
| Gabapentina | Día 1-3: 2 mg/kg/dosis VO cada 8 h. Día 4-6: 4 mg/kg VO cada 8 h. Incrementar cada 2 a 4 días en 5 - 6 mg/kg por día hasta: · Analgesia efectiva; o · Efectos adversos. Máx: 50 - 72 mg/kg/día (los niños < 5 años pueden requerir llegar a la dosis alta). La dosis nocturna podría ser mayor a las otras si los síntomas ocurrieran predominantemente por la noche o hubiera insomnio asociado. Los incrementos podrían ser diarios si la intensidad de los síntomas lo ameritan. | Efectos adversos: sedación, nistagmus, temblor, edema. No hay interacciones farmacológicas importantes. Se ha utilizado hasta en lactantes de un mes de vida, y actualmente se está evidenciando su uso y seguridad incluso en neonatos. |
| Amitriptilina | Día 1-4: 0.2 mg/kg/día VO por la noche. Incrementos en 0.2 mg/kg/día cada 4 a 5 días hasta lograr el efecto deseado ó presencia de efectos adversos. Dosis óptima 1 mg/kg (50 mg máx). Puede ser necesario llegar hasta 1.5 - 2 mg/kg (máx 100 mg); la incidencia de efectos adversos es mayor incluyendo prolongación de QT. | Efectos adversos: boca seca, constipación, retención urinaria, sedación, agitación / acatisia, prolongación del segmento QT (Recomendable realizar un EKG previo a inicio). No administrar si se utilizan fármacos que pudieran prolongar el intervalo QT. |
| Abreviaturas: Daño Neurológico Grave (DNG); Dosis Máxima (Máx); Segmento QT (QT) Vía Oral (VO) | ||
Estrategias no farmacológicas. Informar a los padres que los síntomas son debidos al daño neurológico grave y los factores que pueden contribuir; ellos se vuelven los mejores monitores de síntomas.
Puede ser útil intentar estrategias complementarias como terapia asistida con mascotas, música, fisioterapia.
Brindar a La familia estrategias de autocuidado; cuidar de un niño con DNG es agotador.
Delirium. Se define como trastorno neuropsiquiátrico global transitorio de la cognición, derivado de una disfunción cerebral que se manifiesta clínicamente con una variedad de síntomas neuropsiquiátricos de inicio abrupto, en particular alteraciones de conciencia, atención, cognición, y percepción que tiende a fluctuar sobre el curso del día y usualmente tiene una etiología de base en factores fisiológicos. (1, 8-9)
Cuadro clínico: Las características esenciales del delirium son:
· Una alteración de la atención o de la conciencia;
· Esta alteración se acompaña de cambios en la cognición que no se pueden explicar mejor por otro trastorno neurocognitivo preexistente (ej: retraso mental, demencia);
· Esta condición se desarrolla en un periodo de tiempo corto, de horas o días, y a menudo fluctúa durante el día, con empeoramiento típicamente nocturno; y
· Hay indicios a partir de la historia del paciente, la exploración o los resultados de laboratorio de que la alteración es probablemente el resultado de una enfermedad médica o de su tratamiento.
El delirium tiene un rango amplio de síntomas y conductas psicomotoras que se subdividen según el componente motor que predomine en:1,10
· Hipoactivo: Forma más común, aunque generalmente esta subdiagnósticado Es caracterizado por la apatía, disminución de la respuesta y retraimiento, los niveles de dopamina son bajos o normales y hay una desregulación colinérgica importante. Menor calidad de vida con mayor riesgo de cursar con infecciones intrahospitalarias y úlceras por presión;
· Hiperactivo: caracterizado por la inquietud psicomotora, agitación, labilidad emocional, mayor riesgo de extubación y de auto-infligirse daño. Se presenta más frecuentemente relacionado a intoxicación por sustancias o síndrome de abstinencia. Existe un alto estado dopaminérgico, que desencadena la agitación y la agresión. Pueden cursar con trastornos del pensamiento, dificultad para hablar con claridad o hablar sin sentido; los delirios, que son pensamientos o creencias falsas sin base en la realidad y alucinaciones. Su prevalencia varía entre 1.6 % a 35 %; y
· Mixto: pudiendo fluctuar entre uno y otro.
En el niño, este padecimiento, además de los síntomas psicomotores, cursa con otros síntomas neuropsiquiátricos como acciones sin sentido, estado inconsolable y signos de la desregulación autonómica. (8-9)
Diagnóstico: Este suele ser clínico, la sospecha siempre se deberá llevar a cabo ante la aparición aguda de una alteración de la cognición, las emociones, la conciencia o la aparición de alteraciones conductuales en un niño críticamente enfermo. Se han utilizado algunas herramientas como:
· Delirium Rating Scale (DRS) y Delirium Rating Scale Revised-98 evalúan detalladamente el estado mental de los pacientes. Estas escalas se pueden aplicar a los niños con enfermedad crítica; y
· pCAM-ICU es un instrumento validado e para el diagnóstico del delirium pediátrico en niños críticamente enfermos. Este algoritmo se aplica a los mayores de cinco años o que tengan esta edad por desarrollo (sensibilidad del 85 %, especificidad del 98 %).
Diagnóstico diferencial: El diagnóstico diferencial de las situaciones que potencialmente pueden conducir a un delirium se recogen en el acrónimo (en inglés:) "I WATCH DEATH" (Infecciones; Withdrawal (abstinencia); Acute metabolic (Trastornos metabólicos agudos); Trauma; Enfermedad del SNC; Hipoxia; Deficiencias (Vitamina B12, hipovitaminosis, niacina, tiamina); Enviromental (Ambiente; hipo/hipertermia, endocrinopatías); Vascular Agudo (Emergencia hipertensiva, hemorragia subaracnoidea); Tóxicos (medicamentos, drogas, pesticidas, etc); Heavy metals (Metales pesados como hierro y mercurio).
El diagnóstico diferencial del delirium hipoactivo merece una particular atención en los siguientes casos:
· Retiro de fármacos sedantes o/y opioides de manera súbita y brusca;
· Cuando hay una intoxicación subyacente por psicotrópicos o un síndrome por neurolépticos por sensibilidad a los antipsicóticos; y
· La posibilidad de estatus epilépticos no convulsivos, trastorno depresivo mayor o inhibición catatónica debe ser excluida.
Estrategias farmacológicas. Delirium hiperactivo: Se puede considerar el uso de medicación para reducir síntomas como ansiedad, agitación, alucinaciones y alteraciones del sueño. Considerar y evaluar los efectos adversos e interacciones medicamentosas.
Se emplean antipsicóticos típicos como el haloperidol y atípicos como la risperidona, quetiapina, olanzapina; se utilizan benzodiacepinas y clonidina en el tratamiento del delirium por abstinencia de benzodiacepinas; para el tratamiento del delirium por abstinencia de opiáceos se usan clonidina y metadona. (14-16)
| Fármaco | Dosis | Consideraciones |
| Haloperidol (1) | VO/SC/IV/IM 3 meses a 3 años: 0.0125-0.025 mg/kg c/6-8 hrs Máx: 0.15 mg/kg/día. > 3 a 12 años: 0.025-0.05 mg/kg c/6-8hrs Máx: 5mg/día. > 12 años: 0.5-1.5 mg c/6-8hrs Máx: 20 mg/día | Dosis IV es dos veces más potente que VO. Efectos adversos: Extrapiramidalismo, distonía, riesgo de prolongar el QT. Uso como antiemético. |
| Risperidona (1) | <20 kg: 1.25 -0.25 mg VO, en una o dos dosis día. Máx.: 1-2 mg/día. 20-60 kg: 0.25-0.5 mg VO, en una o dos dosis día. Máx.: 2-3 mg/día. >60 kg: 0.5-1 mg VO, en una o dos dosis día. Máx.: 4 mg/día | Tratamiento de delirium, agitación y cambios de ánimo inducidos por los esteroides. Causa incremento de peso y de prolactina. |
| Quetiapina (1) | Lactantes: 0.5 mg /kg/día Dosis extra de 0.5mg/kg cada 8 horas (mientras la agitación se controla). Max: 6mg/kg/día (menores 7 kg) 7-20 kg: 6.5-12.5 mg en una o dos dosis al día. Máx.: 200 mg/kg/día. 20-40 kg: 18.75 mg una o dos dosis al día. Máx.: 300 mg/kg/día 40-60 kg: 25 mg una o dos dosis al día. Máx.: 300 mg/kg/día | Efectos adversos: hipertermia maligna, arritmia de puntas torcidas, movimientos extrapiramidales, hipotensión, desregulación de la glucosa y los lípidos, espasmo laríngeo. Efectos anticolinérgicos: constipación, retención urinaria y boca seca. Evitar el uso QT prolongado o arritmia cardiaca. |
| Olanzapina (1) | <30 kg: 1.25 mg VO, en una o dos dosis día. Max: 5mg/día 30-60 kg: 1.25 mg VO, en una o dos dosis día. Max: 10 mg/día. >60 kg: 5 mg VO, en una o dos dosis día. Max: 20 mg/día | Puede administrarse IM. Útil como sedante leve, delirium, ansiedad, insomnio, estabilizado del ánimo. Buen antiemético para nausea y vómito inducido por opioides. Evitar Olanzapina IM con Benzodiacepinas IV |
| Abreviaturas: Intravenoso (IV); Dosis Máxima (Máx); Segmento QT (QT);Vía Oral (VO) | ||
Estrategias no farmacológicas (11-13)
· Prevención: identificar, modificar y, cuando sea posible, corregir las afecciones médicas subyacentes de un paciente que pueden generar delirium;
· Presencia de familiar continuamente;
· Promover la toma de siesta durante el día, con un horario establecido;
· Alentar familia de traer objetos como fotografías, juguetes, almohadas, etc.;
· Retiro oportuno de catéteres, sondas, restricciones;
· Apagar luces a una hora determinada, disminuir en medida de lo posible las interrupciones del sueño; y
· Promover el uso de anteojos, aparatos auditivos en caso de que el paciente los requiera.
Insomnio. La prevalencia de insomnio en niños con enfermedades crónicas es alta y generalmente de origen multifactorial. El insomnio de un niño enfermo impacta considerablemente en su calidad de vida y en la de sus padres, ya que un niño que no duerme bien provoca un padre que tampoco lo haga.
Las causas más frecuentes son: (18)
· Otros síntomas descontrolados (ej. dolor, nausea, vómito);
· Alteración primaria del sistema nervioso central (ej. niños con tumores de sistema nervioso central o niños con daño neurológico grave);
· Tratamientos con toxicidad neurológica (radioterapia craneal, quimioterapia);
· Trastornos del estado de ánimo (depresivo o ansiedad);
· Por intervenciones de enfermería durante hospitalizaciones ó por los cuidadores en casa, ya sea para monitorizar parámetros clínicos o administrar medicamentos;
· Ambiente hospitalario (ej. cuartos de hospital privados de luz natural); y
· Comorbilidad - obesidad, insuficiencia cardíaca, ceguera.
| Estrategias farmacológicas | ||
| Fármaco | Dosis | Consideraciones |
| Difenhidramina | 0.5 a 1 mg/kg VO, 30 minutos antes de ir a dormir. Dosis habitual: 12.5 a 50 mg/dosis. Máx. 50 mg/dosis | Por períodos breves, paralelo a medidas conductuales; sin embargo, en condiciones progresivas, su uso puede extenderse. |
| Melatonina | 1 mg en lactantes, 3 mg en niños y 5 mg en adolescentes, VO o SL (de acuerdo a preparación); 90 minutos antes de hora de ir a dormir. Ajustar de acuerdo a respuesta individual. | Adyuvante para insomnio inicial o alteración del ritmo circadiano (pacientes con tumores de sistema nervioso central -tálamo, hipotálamo; invidentes). Bien aceptado por padres. Efectos adversos: pesadillas. |
| Clonazepam | - 0.002 - 0.01 mg/kg; VO | Trastorno ansiedad, depresión; espasmos musculares, antiepiléptico. Efectos adversos: potencial dependencia física o psicológica. |
| Amitriptilina, Gabapentina | -Ver neuroirritabilidad. | |
| Abreviaturas: Dosis Máxima (Máx); Segmento QT (QT); Vía Oral (VO) | ||
Estrategias no farmacológicas (11-13)
· Revisar factores propios del paciente o externos que estén afectando el inicio o la continuidad del sueño;
· Mejorar la higiene de sueño y corregir los factores externos que sea posible (ej. favorecer exposición a luz natural durante el día, disminuir intervenciones de enfermería);
· Uso de estrategias conductuales (relajación muscular progresiva, respiración profunda, hipnosia).
Ansiedad. La ansiedad se produce como una respuesta a las experiencias desconocidas, traumáticas, dolorosas y a la separación de la familia. Prevalencia entre el 7-40%. Se manifiesta como miedo, evitación, irritabilidad, llanto y dificultad para concentrarse; puede presentarse con síntomas somáticos como malestar gastrointestinal, náuseas, vómitos, cefalea, mareos e insomnio. Puede estar presente en el Síndrome de Estrés Postraumático.
Estrategias farmacológicas. Los pacientes con desorden de ansiedad se benefician con ISRS como primera línea farmacoterapia y es superior cuando se combina con TCC. Los benzodiacepinas son de uso común en el paciente en CPP (para insomnio, como antieméticos, sedantes, o como "puente" ansiolítico al iniciar un ISRS), sin embargo, es necesario considerar:
· La dependencia y abstinencia al utilizarlas por tiempos más prolongados; y
· Monitorizar la desinhibición paradójica o agitación que puede presentarte especialmente en niños neuroatípicos.
Precaución al utilizar junto a opioides por el riesgo de depresión respiratoria
| Fármaco | Dosis | Consideraciones |
| Clonazepam (1) | 0.25 a 0.5 mg por dosis, dos o tres veces al día, VO. Máx: 3 mg día. | Inicio de acción lento. Duración 6-8 h. Usado par ansiedad general, insomnio. |
| Midazolam 1 | 0.025-0.05 mg/kg IV, Intranasal. 0.25-1 mg/kg VO. | Rápido. Indicado para sedación. |
| Lorazepam (1) | 0.25 - 1 mg por dosis, VO, SL, SC, IV. Puede indicarse cada 4 horas. (Incrementar 0.25-0.5 mg, si primera dosis no es efectiva) Máx. 3-6mg/día | Inicio de acción rápida. Duración 4 h. Puede ser usado hasta c/h PRN. Usado para ansiedad general, ataques de pánico, nausea pre-quimioterapia, insomnio. |
| Olanzapina (1) | Ver delirium | |
| Abreviaturas: ISRS (Inhibidores selectivos de la recaptura de serotonina; Segmento QT (QT) Vía Oral (VO) | ||
Estrategias no farmacológicas
· La preparación del ambiente, el niño y los padres pueden disminuir la ansiedad;
· Optimizar la comunicación;
· Favorecer la estancia de los padres o tutores;
· Terapia de exposición gradual y desensibilización ante las situaciones que generan ansiedad;
· Terapia Cognitiva Conductual (TCC); Relajación, imaginería, resolución de problemas y manejo de estrés; e
· Hipnosis, Mindfulness.
Depresión. Trastorno del estado de ánimo, se presenta como una tristeza persistente, pérdida del interés en las actividades cotidianas, fatiga, disminución de la energía, disminución de concentración y cambios en los hábitos de alimentación por más de dos semanas; siempre debe descartarse la ideación suicida. Las tasas de depresión se incrementan en niños con condiciones o enfermedades crónicas.
El DSM-5 no distinguen la depresión pediátrica a la de adultos, sin embargo, los niños pueden tener más irritabilidad y en ocasiones, derivado del proceso de desarrollo, pueden no entender o comunicar los síntomas depresivos; además, no se contemplan criterios de depresión en niños con comorbilidad, en los cuales la presencia de síntomas asociados a su condición de base puede confundir al clínico. La tristeza sostenida, irritabilidad, aislamiento social y/o anhedonia pueden ser más sensibles para indicar depresión en niños enfermos. (1)
Es importante diferenciar depresión mayor del trastorno de adaptación, en los que hay síntomas emocionales, menos intensos y de menor duración que se desarrollan en relación con un estresor específico.
En el abordaje es imprescindible evaluar factores de riesgo tales como historia personal o familiar de premorbilidad afectiva, disfunción familiar, insomnio, caquexia, aislamiento social y educativo por la enfermedad, duelo, presencia de síntomas descontrolados como dolor, entre otros.
Estrategias farmacológicas. (1) Los antidepresivos tricíclicos, paroxetina y los inhibidores de la MAO no se usan en depresión en paciente con comorbilidades. Es importante evaluar la ideación suicida por el incremento de la misma al iniciar terapia antidepresiva. Deben estar monitorizados de manera cercana.
| Fármaco | Dosis | Consideraciones |
| Inhibidores selectivos de la re captación de serotonina (ISRS) | Sertralina: >6 años de edad: iniciar 12.5 mg y titular hasta lograr el efecto. Máx. 200 mg/día. | Uso off label para ansiedad y depresión. Inicio de acción lento (4-6 semanas) |
| Fluoxetina: > 8 años: iniciar 5 a 10 mg/ día. >12 años: iniciar 10 mg/día. Incrementos de 10 mg cada 7-14 días. Máx. 60 mg/día. Escitalopram: >12 años: 10 mg al día y aumentar a 20 mg/día después de 3 semanas. | Uso off label para ansiedad. Vida media larga, puede descontinuarse abruptamente; riesgo de sobredosis por vida media prolongada. Interacción con fármacos que se metabolizan en citocromo P450 | |
| Venlafaxina: 37.5 - 225 mg VO (Máx. en niños); Máx.: 300mg/día (adolescentes) -Incrementos de 18.25-37.5 mg cada 7-14 días | Uso off label para depresión y baja energía del paciente en CPP. Primera línea si el pronóstico es <2-3 semanas; inicio de alivio rápido. Efectos adversos: Insomnio, empeoramiento de la ansiedad, alucinaciones visuales | |
| Abreviaturas: DSM-5 (Diagnostic and Statistical Manual of Mental Disorders, Quinta Edición); Dosis Máxima (Máx); Inhibidor Selectivo de la Recaptura de Serotonina (ISRS); Intravenoso (IV); Por razón necesaria (PRN); Sublingual (SL) Terapia Cognitiva Conductual (TCC); Vía Oral (VO) | ||
Estrategias no farmacológicas (11-13)
· Cambios en el ambiente e intervenciones para modificar el comportamiento del niño;
· Comunicación abierta, efectiva, segura y sin juicios;
· Psicoterapia: Terapia cognitiva conductual; Terapia familiar sistémica;
· Terapia de juego o de arte;
· Meditación; y
· Mindfulness.
5.6 SÍNTOMAS DERMATOLÓGICOS
Prurito. Se define como una sensación desagradable que provoca la necesidad imperiosa de rascarse, ocasiona malestar y a veces lesiones por rascado, puede ser altamente incapacitante y pone en peligro la integridad de la piel como barrera de protección. (1,2)
Fisiopatología tanto el dolor como el prurito comparten algunos mecanismos neurofisiológicos la sensación de prurito se transmite al cerebro por nociceptores, fibras C y fibras A delta, que transmiten la señal a las neuronas de la vía espinotalámica hasta el área singulada anterior de la corteza cerebral (centro cortical del prurito). Actúan de forma indirecta al liberar mediadores como la histamina, serotonina, péptidos vasoactivos, encefalinas, prostaglandinas. (2)
Mecanismos
· Dermatológico, causado por procesos inflamatorios o patológicos (urticaria y eccema);
· Sistémico, relacionado con enfermedades de otros órganos (colestasis);
· Neuropático, relacionado con enfermedades del sistema nervioso central o sistema nervioso periférico (esclerosis múltiple);
· Psicógeno o psiquiátrico, relacionado con trastornos psiquiátricos
· Enfermedad cutánea primaria;
· Enfermedad sistémica; y
· Causada por medicamentos. (1,2,3)
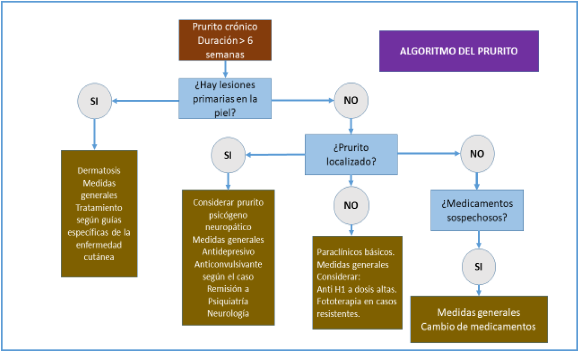
Estrategias farmacológicas
Antihistamínicos:
· Difenhidramina: IM o IV. Menores de 1 año 1mg/kg/ día 3 a 4 tomas.
Mayores de 1 año 1mg/kg/día, c/ 6 u 8 hrs. Máximo 5 mg/kg/día, con dosis máxima de 50 mg;
· Hidroxicina: 2 mg/kg/día, c/ 6-8 hrs. Vía oral o intramuscular;
· Clorpromazina: 0.5 a 1 mg/kg/dosis c/ 6-8 hrs.; (1,4,5)
· Loratadina: 2 a 5 años 5 mg/día. Mayores de 6 años 10 mg/día vía oral;
· Desloratadina: Menores de 6 años 1.25 mg al día, 6 a 12 años 5 mg al día vía oral;
· Cetirizina: Menores de 2 años 0.25/kg/día, 2 a 5 años 2.5 mg/día, mayores 6 años 5 a 10 mg/ día vía oral; y
· Corticoides. Su rol no está bien definido.
Antidepresivos:
· Sertralina 75 - 100 mg/ día.
Otros:
· Rifampicina;
· Propofol; y
· Fototerapia. (1,4,5)
Estrategias no farmacológicas (1,2,3,4,5)
· Cuidados de la piel;
· Mantener piel fría e hidratada;
· Evitar baños calientes;
· Evitar el sobre abrigo;
· Evitar sustancias vasodilatadoras (alcohol);
· Cremas con calaminas y mentol;
· Jabones hidratantes y de Avena; y
· Cremas humectantes.
Xerosis. La xerostomía es la sensación subjetiva de boca seca que es secundaria a una hiposecreción salival, la cual corresponde a una disminución objetiva del flujo salival. (6) La persistencia en el tiempo de tasas bajas de secreción salival conlleva cambios en el medio bucal y condicionan la aparición de lesiones sobre los tejidos duros y blandos de la boca. (7)
Estrategia farmacológica. Pilocarpina en pacientes adolescentes de más de 45 kilos: tabletas de 5 mg y se administra de 5 a 10 mg cada 8 horas V.O. Produce efectos secundarios debido a su acción colinérgica (sudoración, rinitis, molestias urinarias). Contraindicada en pacientes con asma, enfermedad pulmonar obstructiva crónica, insuficiencia cardiaca, epilepsia, hipertiroidismo, glaucoma, úlcera gástrica y enfermedad de Parkinson. Su administración tópica disminuye los efectos adversos. (6)
Estrategia no farmacológica
· La más importante: Cuidado bucal estándar;
· Trate la causa, p. Ej. deshidratación, infección;
· Considere la saliva artificial;
· Proporcione comodidad local: cubitos de hielo, frescos trozos de piña, cubos de hielo en frappe; y
· Parafina suave en los labios. (6)
Es importante conocer si existe en el enfermo con boca seca, parénquima salival funcionante que pueda ser estimulado de forma mecánica, química o gustativa. (8)
5.7 URGENCIAS PALIATIVAS
El manejo deberá personalizarse de acuerdo con el momento y la situación que se encuentre el paciente, ya que no es lo mismo que se presente alguna urgencia como pudiera ser una compresión medular si lo situamos el diagnóstico al inicio del tratamiento que en la fase final de la enfermedad, la agresividad del manejo dependerá de acuerdo a las variables que se presenten en cuanto a estado general del paciente, evolución de la enfermedad y recursos disponibles, entre otros.
Estado epiléptico. Definición: Una crisis epiléptica generalizada que dura cinco o más minutos, o la presencia de dos o más crisis sin recuperación de la consciencia en un periodo de 30 minutos, o una crisis focal que persiste durante más de 10 minutos o con alteración de la consciencia durante 60 minutos o más de duración [2] El manejo inicial del estado epiléptico puede ser brindado por los padres si han sido capacitados para ello; de lo contrario el paciente debe ser trasladado a unidad hospitalaria. (1)
Los pasos iniciales son:
· Vía aérea; acomodar adecuadamente la cabeza. Asegurar intercambio gaseoso y acomodar adecuadamente cabeza (evitar ronquido, obstrucción lingual); si es necesario y se cuenta, administrar oxígeno; y
· Administrar por vía rectal, nasal, i.m. o i.v. benzodiacepina a dosis estándar. Es sumamente útil capacitar a los padres para la administración transrectal de diazepam o intranasal de midazolam y que tengan el material en casa para emergencias. (1)
Administración transrectal:
· Introducir vía transrectal 5 cm de una sonda de alimentación 8 ó 10 FR;
· Tomar el contenido total de una ampolleta de diazepam; y
· Administrar la dosis previamente calculada por el médico.
Una vez en la Unidad de salud deberá tomarse glicemia capilar y signos vitales.
De no remitir el cuadro con primera dosis de benzodiacepina, puede administrarse una segunda. En caso de no remitir con dos dosis de benzodiacepinas, puede iniciarse infusión de fenitoína, levetiracetam o ácido valproico. (1)
El manejo hospitalario e intensivo se continuará de acuerdo a protocolos aceptados en la literatura y de acuerdo a las metas de tratamiento previamente habladas con la familia.
Soporte a la familia. En el contexto de pacientes con enfermedad neurológica avanzada es posible que el estatus epiléptico sea causa del fallecimiento. Es necesario brindar de manera anticipada a los padres las herramientas técnicas y soporte emocional para poder manejar este evento lo mejor posible.
Manejo crónico. En el paciente con daño neurológico severo y/o epilepsia refractaria con calidad de vida limitada los objetivos son:
· Lograr el menor número de crisis convulsivas, con el menor número de fármacos antiepilépticos para evitar los altos costos y efectos adversos que la polifarmacia implica; y
· Reconocer e informar a los familiares que es probable no se logre un control absoluto a pesar de utilizar los mejores tratamientos existentes y así ponderar efectos adversos de dosis altas y combinaciones de fármacos. (ej. somnolencia, bradipsiquia, sialorrea).
| Fármaco | Dosis | Consideraciones |
| Ácido valproico | Estado epiléptico: 20-40 mg/kg i.v. hasta 1.5 g (velocidad de infusión - 15 minutos). Inicio y mantenimiento vía oral: 10 - 15 mg/kg/día en dos o 3 dosis con incrementos semanales de 10 mg/kg/día hasta 20 a 30 mg/kg/día. Los lactantes pueden llegar a requerir dosis tan altas como 60 mg/kg/día. | Efectos secundarios: hepatotoxicidad, trombocitopenia, leucopenia, pancreatitis. Útil para crisis focales y generalizadas. Niveles terapéuticos: 50 - 100 mg/ml. (2,3) |
| Fenitoína | Estado epiléptico: 15-20 mg/kg/dosis IV (velocidad de infusión 1 mg/kg/min al menos en 20 min) Mantenimiento: 5-7 mg/kg/día en 2 o 3 tomas, IV o VO. Impregnación vía oral (descontrol de crisis): 20 mg/kg/día en 2 dosis (día 1) y posteriormente iniciar mantenimiento convencional. | Fármaco de amplio espectro. Interacción con múltiples fármacos. Para evitar los alimentos afecten su absorción, alejar la toma 90 minutos antes o después de la ingesta de comida. Niveles terapéuticos entre 10 - 20 mg/ml. (2,3) |
| Levetiracetam | Dosis inicio: 10 mg/kg/día con incrementos semanales de 10 mg/kg/día hasta una dosis de mantenimiento de 30 a 60 mg/kg/día. Estado epiléptico: 20-60 mg/kg i.v. hasta 2.5 g, 15 min de infusión. | Dosis IV es equivalente a VO. (2) |
| Diazepam | IV: 0.3 mg/kg hasta 5 mg en menores de 5 años y 10 mg en mayores de 5 años. Rectal: 0.5 mg/kg de 1 a 3 años 5 mg, mayores de 3 años 10 mg dosis habitual. | Es sumamente útil capacitar a los padres para la administración transrectal de diazepam. (2,3) |
| Midazolam | Mayores de 40 kg: 0.2 mg/kg hasta 10 mg Menores de 40 kg: 0.2 mg/kg hasta 5 mg Vía: intranasal o mucosa oral. | Puede existir ardor local por el pH ácido. (2,3) |
Taponamiento cardiaco*
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Oxígeno suplementario (4) | Mínimo necesario que requiera el paciente. | |
| Opioides Manejo de disnea *Se recomienda se emplee 25 a 50% de la dosis indicada para manejo de dolor. (4) | Morfina (VO/SC/IV) Pediatría: 0.05-0.1 mg 7kg/dosis hasta cada 4 horas. Oxicodona (VO) Pediatría: 0.05 mg-1 mg/kg dosis hasta cada 4 horas. Dosis máxima 5 mg cada 4 horas. | Depresión respiratoria Estreñimiento |
| Benzodiazepinas Manejo de ansiedad. (4) | Diazepam Pediatría VO: 0.1-0.8 / mg / kg / día dividido en 3 o 4 dosis. Máximo 60 mg / día Pediatría IV / IM: 0.04-0.3 mg / kg / dosis cada 2 a 4 horas Máximo 0.6 mg/kg cada 8 horas. Lorazepam (VO/SC/IV) Pediatría: 0.05 mg/kg hasta cada 4 horas. Máximo 10 mg/día. | En pacientes neonatales su metabolismo es disminuido Los metabolitos se acumulan en pacientes con enfermedad renal. Administrar con alimentos para disminuir efectos adversos gastrointestinales. |
Estrategia no farmacológica
· Individualizar en cada caso el beneficio de realizar pericardiocentesis guiada por ultrasonido;
· Facilitar un ambiente tranquilo y limitar el número de personas en la habitación;
· Favorecer ventilación de la habitación, abrir ventanas, emplear ventiladores de aspas con aire hacia el rostro o aire acondicionado;
· Promover comodidad en la posición del paciente (Semi-sentado); y
· Emplear técnicas de relajación.
Síndrome de vena cava superior* Obstrucción intrínseca o extrínseca de la vena cava superior. Dentro de las principales causas se encuentran: neoplasias, infecciones, accesos venosos y/o trombosis.
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Identificar la causa e individualizar el caso para determinar si es susceptible de tratamiento Ej: quimioterapia, radioterapia, anticoagulantes | ||
| Oxígeno suplementario | Mínimo necesario | |
| Diuréticos *Ayudan a disminución de precarga. (4) | Furosemida (VO / IV) Pediatría: 1-2 mg/kg/dosis hasta cada 6 horas. Dosis máxima 40 mg/día | Desequilibrio hidroelectrolítico Deshidratación. Hipotensión. |
| Esteroides *Útil si sospecha de edema cerebral o edema de vía aérea. (4) | Dexametasona (IM/IV) Pediatría: 2.5-10 mg/ m2/día. Repartir en 2 a 4 dosis. Dosis máxima 10 mg cada 6 horas. | |
Estrategia no farmacológica
· Posición elevada de cabeza y cuello a 45º;
· Vigilar balances hídricos y evitar hiperhidratación;
· Valorar colocación de endoprótesis / stent;
· Facilitar un ambiente tranquilo y limitar el número de personas en la habitación; y
· Favorecer ventilación de la habitación, abrir ventanas, emplear ventiladores de aspas con aire hacia el rostro o aire acondicionado. (5)
Claudicación familiar Agotamiento del cuidador o familiar que ocasiona pérdida de capacidad para cubrir de forma adecuada las necesidades del paciente. Las principales manifestaciones asociadas en los cuidadores son: incertidumbre, preocupación por la insuficiencia para solventar las necesidades del paciente. (6)
Estrategia no farmacológica
· Detectar a los cuidadores o familias que se encuentran en riesgo de claudicación;
· Las acciones del equipo de cuidados paliativos estarán dirigidas a valorar si la familia puede atender adecuadamente a su paciente y a ayudar a identificar a la persona que llevará la responsabilidad de los cuidados (cuidador principal), para fortalecer el cuidado y atención del paciente; (7)
· Establecer redes de apoyo con familiares y personas allegadas al paciente para evitar desgaste del cuidador principal. Ej: compartir responsabilidades en la toma de decisiones, relevo para el cuidador del paciente, apoyo económico y emocionalmente entre otras; (7)
· Brindar a la familia y cuidadores toda la información necesaria para comprender la enfermedad del paciente, pronóstico y planes terapéuticos estableciendo metas realistas. Priorizando la comunicación
efectiva entre los miembros que participen en el cuidado del paciente.
· La situación de la familia y cuidadores debe ser evaluada periódicamente pues a lo largo de la enfermedad del paciente pueden presentarse sucesos que generen claudicación, pues su aparición se asocia a disminución en la calidad de atención del paciente.
· Se recomienda la intervención psicológica de la familia desde el momento del diagnóstico del paciente. (6)
Sangrado masivo. El sangrado puede ocurrir en pacientes con diagnósticos oncológicos, principalmente en estadios avanzados.
La presencia de sangrado, sobre todo al final de la vida, es una de las situaciones más atemorizante tanto para los cuidadores, pacientes e incluso el equipo de salud, por lo que es muy importante anticiparse a dicho evento, hablarlo previamente con la familia para considerar las posibles intervenciones a realizarse y tener disponible los insumos que se requerirán. (8)
Es muy importante averiguar la causa del sangrado, así como la severidad y pronóstico del paciente, ya que el manejo depende de esos tres aspectos.
Identificar riesgos potenciales y anticiparse a los mismos (Patología de base, antecedentes de hemorragias previas, coagulopatías, tipo y sitio del tumor, hepatopatía, etc.)
Respecto de los concentrados plaquetarios y eritrocitarios, será siempre necesario individualizar cada caso, valorando el riesgo y beneficio.
| Estrategia farmacológica | ||
| Fármaco | Dosis | Precauciones |
| Ácido tranexámico (8) | Hemorragia alveolar: 250 mg inhalados cada 6 horas en <25 kg, 500 mg inhalados cada 6 horas en > 25 kg (Hasta completar 3 o 4 dosis) Otro sangrado: Carga de 10-30 mg/kg IV seguida de infusión continua a 5-10 mg/kg/hrs. | Contraindicado en casos de coagulación intravascular diseminada. |
| Omeprazol (8) | 1-2 mg/kg/día (Máximo 40 mg / día). | |
| Ranitidina (8) | Oral: 4-8 mg/kg/día cada 12 horas (Máximo 300 mg/día) IV: 2-4 mg / kg/día cada 6-8 horas (Máximo 50 mg/dosis) | |
| Adrenalina | Humedecer gasas con el medicamento y aplicar en los sitios de sangrado | |
| Midazolam (8) | 0.05-0.15 mg/kg/dosis, cada 4 horas, máximo 10 mg/dosis (IM o IV) 0.5-2 mcg/kg/min (En infusión continua IV) | Dosis altas pueden ocasionar depresión respiratoria. |
Estrategia no farmacológica
· Aplicar presión si es posible;
· Utilizar toallas o paños oscuros para disfrazar el color de la sangre;
· Acompañamiento en el proceso al paciente y la familia (Estar disponibles en cualquier forma desde la presencial, virtual, por llamada telefónica, etc.); y
· Formular el plan terapéutico (Puede ser domiciliario, intrahospitalario, en hospice, albergue, etc.) y comunicarlo a los padres o cuidadores, al equipo médico tratante y al paciente.
Sofocamiento. Sensación angustiante y subjetiva de respiración incómoda o "falta de aire", ser ocasionada por factores físicos (fluidos, tumores, debilidad, etc.), psicosociales (miedo, ansiedad, etc.) y espirituales (miedo a una muerte inminente, miedo a la sofocación). (8)
Causas:
· No reversibles: Obstrucción de vía aérea (Tumores o anomalías congénitas), cardíacas (Falla cardiaca, hipertensión pulmonar), debilidad muscular, falla del parénquima pulmonar (Fibrosis quística, neumonías). (8)
· Reversibles: Ansiedad, trastornos hematológicos (Anemia, acidosis metabólica) broncoespasmo (Asma), tos (Aumento de secreciones, tumores, infecciones), fluidos en tracto respiratorio (Edema, secreciones, inflamación, infecciones, dolor (Fracturas costales, pleuritis), embolismo pulmonar, neumotórax o derrames pleurales. (8)
Estrategia farmacológica. Considerar que los opioides suprimen la conciencia respiratoria, disminuyen la respuesta a la hipoxia e hipercapnia, proveen vasodilatación pulmonar y mejoran el radio de ventilación/perfusión en los pulmones, (8) y que los fármacos benzodiacepinas funcionan como ansiolíticos.
| Fármaco | Dosis | Precauciones |
| Morfina (4) | 0.05-0.1 mg/kg/dosis cada 4 horas (Vía oral, IV, SC) | Puede presentarse íleo por uso de opioides, vigilar características y frecuencia de las evacuaciones. Dosis altas pueden ocasionar depresión respiratoria. |
| Oxicodona (4) | 0.05-0.1 mg/kg/dosis cada 4 horas, máximo 10 mg/dosis (Vía oral, IV, SC) | |
| Diazepam (4) | 0.12-0.8 mg/kg/día cada 6-8 horas, máximo 60 mg / día (Vía oral o sublingual) 0.04-0.3 mg/kg/dosis cada 2-4 horas, máximo 0.6 mg/kg (IM o IV). | Dosis altas pueden ocasionar depresión respiratoria |
| Midazolam (4) | 0.05-0.15 mg/kg/dosis cada 4 horas, máximo 10 mg/dosis (IM, IV, SC). 0.5-2 mcg/kg/min (En infusión continua IV) | |
| Lorazepam (4) | 0.5 mg/kg cada 4 horas, máximo 2 mg / dosis. |
Estrategia no farmacológica
· Iniciar una respiración más lenta y profunda;
· Soplar para hacer burbujas, respirar en una bolsa de papel, usar ventiladores;
· Mantener las ventanas abiertas;
· Posición en sedestación;
· Hipnosis, técnicas de relajación;
· Oxigenoterapia (Poco efectiva en la fase de agonía); y
· Ventilación no invasiva con presión positiva. (Puede beneficiar en casos de fatiga muscular, permitiendo respiraciones más profundas). (8)
Síndrome de lisis tumoral. Conjunto de anormalidades metabólicas caracterizadas por hiperuricemia, hiperfosfatemia, hiperkalemia e hipocalcemia y las alteraciones clínicas que estas generan: (insuficiencia renal aguda, arritmias cardiacas, convulsiones y muerte), desencadenadas por la destrucción espontánea o inducida por el tratamiento de células malignas.
Es más común en pacientes con leucemia linfoblástica aguda, linfoma de Burkitt posterior al inicio de la quimioterapia, pero también en algunos tumores de alta tasa de proliferación su presentación puede ser de forma espontánea. (9)
Estrategia farmacológica. Identificar a los pacientes que tienen riesgo para su presentación.
Uno de los objetivos del tratamiento es:
· Corregir las alteraciones metabólicas secundarias: hiperkalemia, hipocalcemia, hiperuricemia, hiperfosfatemia. (4) Sin añadir potasio, fósforo ni calcio a las soluciones; y
· Líquidos: Asegurar aporte hídrico:
>10 kg: 3 litros / m2
<10 kg: 200 ml / kg / día.
Estrategia no farmacológica
Individualizar el caso. Si es necesario: Monitorización estrecho, control de líquidos cada ocho horas.
| Fármaco | Dosis | Precauciones |
| Furosemida Asegurar uresis: <10 kg: 4-6 ml/kg/ hora >10kg: >100 ml/m2/hrs (4) | (VO/IV) Pediatría: 1-2 mg/kg/ dosis hasta cada 6 horas. Dosis máxima 40 mg/ día. Infusión continua IV: comenzar con 0,05-0,1 mg/kg/hrs. Adecuar dosis en función del efecto aumentando hasta dosis máxima de 1 mg / kg / h. | |
| Alopurinol (4) | VO: 10 mg/kg/día o 300 mg/m2/día cada 8 h por vía oral (dosis máxima de 800 mg/d). | Requiere ajuste de dosis en lesión renal. En pacientes de alto riesgo lo ideal es iniciarlo 12 horas antes del inicio de quimioterapia.9 |
| Rasburicasa (9) | IV: 0,15 o 0,20 mg/kg/día, en una sola dosis. Aforar en 50 ml de solución salina al 0.9%. | Puede provocar hiperfosfatemia, hiperpotasemia e hipocalcemia. |
*Currow D, Clark K. (2006). Tumor Lysis Syndrome. Emergencies in Palliative and Supportive Care, Chap. 7, 202.
Síndrome de compresión medular. El síndrome de compresión medular ocurre en aproximadamente entre el 3 al 5% de los pacientes con cáncer. Se considera una de las emergencias oncológicas más frecuentes.
Evaluación: Se deberá sospechar en todo el paciente pediátrico portador de sarcomas (especialmente Ewing), neuroblastoma, tumores de células germinales, linfomas y tumores primarios del Sistema Nervioso Central, con dolor de espalda, déficit neurológico, motor y sensorial agudo.4
Tratamiento:
De manera inicial, mientras se hace el abordaje, administrar:
· Dexamentasona 1-2mg/kg/ VO/IV; y
· Valorar quimioterapia, radioterapia y cirugía.
5.8 MANEJO DE SÍNTOMAS REFRACTARIOS (SEDACIÓN PALIATIVA)
La sedación paliativa es la disminución deliberada de la conciencia del enfermo, una vez obtenido el oportuno consentimiento mediante la administración de los fármacos indicados y a las dosis proporcionadas, con el objetivo de evitar un sufrimiento insostenible causado por uno o más síntomas refractarios.
La sedación paliativa se utiliza cuando el enfermo se encuentra en sus últimos días u horas de vida para aliviar el sufrimiento intenso. En esta situación, la sedación es continua y tan profunda como sea necesaria. La sedación intermitente es aquélla que se pauta de forma transitoria con el objetivo de ser retirada en un plazo de tiempo determinado para reevaluar la persistencia o no del sufrimiento del paciente.
En este contexto, debemos recordar que los cuidados paliativos se caracterizan por ser la buena práctica al final de la vida. Son aquellos que proporcionan una atención integral a los pacientes cuya enfermedad no responde a tratamiento curativo, siendo primordial el control de síntomas, especialmente del dolor, así como el abordaje de los problemas psicológicos, sociales y espirituales. El enfoque debe ser interdisciplinario que incluye al paciente, la familia y su entorno, en hospital o en casa. La sedación se ha de considerar actualmente como un tratamiento médico indicado para aquellos enfermos con sufrimiento intolerables que no han respondido a los tratamientos adecuados.
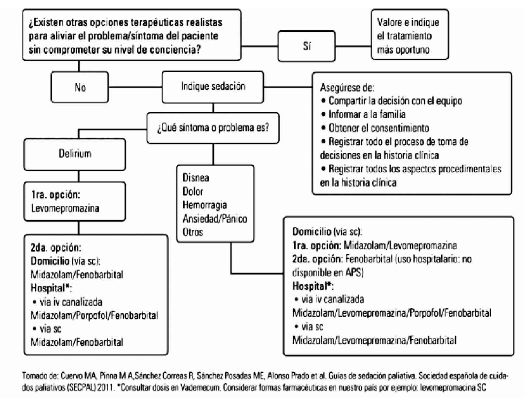
Las causas más frecuentes para la indicación de sedación son: delirium, disnea, dolor, náuseas, vómito, hemorragia masiva, ansiedad o pánico y sufrimiento existencial, siempre y cuando no hayan respondido a tratamientos indicados y aplicados correctamente durante un tiempo razonable. (1)
Proceso de la sedación
· Indicación por sufrimiento intolerable causado por síntomas refractarios;
· Consentimiento del paciente o representante legal que se establece en normativa vigente;
· Prescripción, empleo de fármacos adecuados y dosis de acuerdo a las necesidades del paciente; y
· Evaluación continua y supervisada por el médico responsable. (1,2)
Sedoanalgesia
| Fármaco | Dosis y Vía de administración |
| Benzodizepina Clonazepam solución oral Midazolam solución oral | 0.0.30 a 0.50 mg/kg/día cada/6 a 8 hrs vía oral o sublingual. 0.1 A 0.5 mg/kg/día en infusión IV continua. (2,3,4) |
| Morfina solución oral | Lactantes de 1- 12: meses 80-200 mcg/kg cada 4 hrs Niños de 1-2 años: 200 - 400 mcg/kg cada 4 hrs Niños de 2-12 años: 200 - 500 mcg cada 4 hrs Vía oral. (5) |
| Morfina solución Inyección subcutánea | Recién nacido: 25-50 mcg/kg cada 6 h. Lactante 1 - 6 meses: 100 mcg/kg cada 6 h. Niños de 6 - 2 años: 100 mcg/kg cada 4 h Niños de 2 - 12 años 100-200 mcg/kg cada 4 hrs; la dosis máxima es de 2.5 mg (5,7) |
| Morfina solución intravenosa durante 5 minutos | Recién nacido: 25-50 mcg/kg cada 6 h. Lactantes 1-6 meses 100 mcg cada 6 h. Niños de 6 meses - 12 años 100 mcg/kg cada 4 h. la dosis máxima inicial es de 2.5 mg (5,7) |
| Morfina solución inyectable infusión continua | Recién nacido: 25-50 mcg/kg intravenoso durante un mínimo de 5 minutos, seguidos de 5 - 10 mcg / kg / h en infusión continua. Lactantes 1 - 6 meses: inicialmente 100 mcg/kg intravenosos durante un mínimo de 5 minutos, seguidos de 10 a 30 mcg/kg/h en infusión continua. (5,7) |
| Morfina solución inyectable infusión continua subcutánea. | Lactantes 1 - 3 meses: 10 mcg/kg/hrs Lactantes o niños 3 meses a 12 años: 20 mcg/kg / hrs (5) |
| Fentanilo solución inyectable en infusión continua. | Recién nacido: 0.5 - 1 mcg/kg/hrs Niños 1 mcg/Kg/hrs Menores de 1 año 0.2 - 0.7 mcg/kg/hrs Mayores 1 año 0.5 - 1 mcg / kg /hrs |
| Buprenorfina solución inyectable. | RN a menos de 50 kg: 1-2 mcg/kg/dosis, administración lenta c/8 hrs 3-9 mcg/kg/día dosis tope 18 mcg/kg/ día. (2,5,7) |
| Dexmedetomidina solución inyectable | Niños 0.2 - 1 mcg/kg/hrs Infusión continua. (6) |
| Levomepromazina solución oral en caso de psicosis | Niños 0.5 - 2 mg/kg/día de 2 - 3 tomas diarias. (3,7) |
| Propofol solución inyectable | Mayores de 16 años 1 - 4 mg/kg/hrs infusión continua sólo por 24 horas |
| Fenobarbital solución oral | Neonatos 20 - 30 mg/kg Sublingual Niños 10 - 20 mg/kg Sublingual Dosis máxima de 40 mg/kg |
BIBLIOGRAFÍA
Dolor y su abordaje multimodal
1. Chirino-Barceló Yazmín Amelia, Gamboa-Marrufo José Domingo. Cuidados paliativos en pediatría. Bol. Med. Hosp. Infant. Mex. 2010 Jun; 67 (3): 270-280.
2. Tutelman, Chambers, Stinson. Pain in Children with Cancer: Prevalence, Characteristics, and Parent Management. The Clinical Journal of Pain Publish Ahead of Print (2017)
3. Loeser JD, Treede RD. The Kyoto protocol of IASP basic pain terminology. Pain 137(3), 473-477 (2008).
4. Pérez Fuentes J. Versión actualizada de la definición de dolor de la IASP: Un paso adelante o un paso atrás. Rev. Soc. Esp. Dolor. 2020; 27(4):232-233. https://dx.doi.org/10.20986/resed.2020.3839/2020.
5. Collins JJ. Management of symptoms associated with cancer: pain management. In: Cancer In Children And Adolescents. Carroll WL, Finlay JL (Eds.). Jones & Bartlett, MA, USA, 541-546 (2010).
6. Quiles Mª J, van-der Hofstadt C. J., Quiles Y. Instrumentos de evaluación del dolor en pacientes pediátricos: una revisión (2ª parte). Rev. Soc. Esp. Dolor. 2004 Sep; 11 (6): 52-61.
7. Velasco PG. Acta pediatr. Méx vol.35 número3; Acta Pediátrica de México. 2014; 249 a 255.
8. Drake R, Anderson BJ, Van Den Anker JN, Zernikow B. Managing persisting pain in children with medical illnesses: another frontier unexplored. Peadiatr. Anaesth. 23(5), 381-384 (2013).
9. Marzuillo P, Guarino S, Barbi E. Paracetamol: a focus for the general pediatrician. Eur J Pediatr 2014;173(4);415-25.
10. Martin DP, Bhalla T, Beltran R, Veneziano G, Tobias JD. The safety of prescribing opioids in pediatrics. Expert Opin. Drug Saf. 13(1), 93-101 (2014).
11. Chiaretti A. Et al. Current practice and recent advances in pediatric pain management. European Review for Medical and Pharmacological Sciences, Italy. 2013; 17(Suppl 1): 112-126
12. Howard RF, Wiener S, Walker SM. Neuropathic pain in children, Arch Dis Child 2014;99:84-89
13. Halefom Kahsay Assessment and treatment of pain in pediatric patients. Curr Pediatr Res 2017; 21 (1): 148-157
14. Candido, Kusper, Knezevic, et. al. New Cancer Pain Treatment Options, Curr Pain Headache Rep (2017) 21:12DOI 10.1007/s11916-017-0613-0
15. Jonkman K, Dahan A, van de Donk T, Aarts L, Niesters M, van Velzen M. Ketamine for pain. 2017; 6
16. O´Neill Hunt M., McCrate Protus B., Penfield Winters J., Et al. (2014). Pain. Pediatric paliative care consultant, guidelines for effective management of symptoms. 1ª edición. Alabama. HospiScript; PP 193-215.
17. Korones David. N. 2007. Pediatric Palliative Care. Pediatrics in Review, Vol. 28, 46-56; 193-215.
18. Jody Chrastek and Donna Eull. (2010). Just in time Guide a primer for pediatric palliative care at home. Hospice and palliative nurses association. P: 63.
19. Ezgi Karadag, Sevgin Samancioglu, Dilek Ozden. (2017). Effects of aromatherapy on sleep quality and anxiety of patients. Nurs Crit Care. Mar; 22(2). Pp: 105-112.
Síntomas sistémicos
1. O´Neill Hunt M, McCrate Protus B, Penfield Winters J., Et al. (2014). Anorexia & cachexia. Pediatric paliative care consultant, guidelines for effective management of symptoms. 1ª edición. Alabama. Pp: 48-53.
2. Wolfe Joane., Hinds Pamela., Sourkes Barbara. (2011). Gastrointestinal symptoms. Textbook of Interdisciplinary Pediatric Palliative Care. Saunders. Pp: 311-334.
3. Germ R., Dussel V., Medín G. Cuidar un Niño Enfermo en Casa. Manual de Cuidados Palitaivos para Padres. Ed. Fundación Natali Dafne Flexer. Pág 39-41
4. E. Collazo Chao, E. Girela. (2011). Problemas éticos en relación a la nutrición y a la hidratación: aspectos básicos. Nutrición Hospitalaria, 26(6), 1231-1235.
5. Ragsdale LB, Miller EG. Is My Baby Feeling Hungry?, Pediatric Palliative Care. What Do I Do Now. Oxford University Press Pag. 189-193. 2020.
6. Weise KL, Okun AL, Carter BS, et al. (2017) Guidance on Forgoing Life-Sustaining Medical Treatment. Pediatrics; 140(3)
Síntomas respiratorios
1. Wolfe J, Grier,H.E., Klar,N. et al. Symptoms and suffering at the end of life in children with cancer. N England J Med 2000; 342:326-33.
2. Goldman.A, Hain.R, Liben.S "Repiratory symptoms" en Goldman.A, Hain.R, Liben.S. Oxford Textbook of Palliative Care for Children. Oxford University Press. New York. 2006 p.438-47.
3. A practical guide to Palliative Care in paediatrics , Pain Medicine and Palliative Care The Children's Hospital at Westmead Sydney, Australia, Children's Health Queensland Hospital and Health Service 2014 ISBN: 978 0 9875207 0 8
4. Bennet M et al. Using anti-muscarinic drugs in the management of death rattle: evi- dence-based guidelines for palliative care. J Pall Medicine 2002; 16: 369-74.
5. Bickel K. et al. Death rattle and oral secretions. J Pall Medicine 2008 1040-1041.
6. Vallejo Palma JF, Garduño-Espinosa A. Cuidados paliativos en pediatría. Acta Pediat Mex 2014; 35:428- 435.
7. Villegas R J. Antuña GM. Cuidados Paliativos Pediátricos. Bol Pediatr 2012; 52: 131-145
8. Suárez RE García FT. Cuidados paliativos pediátricos. Desde la perspectiva enfermera. NPunto Vol. III. Número 23. Febrero 2020.
9. Cheng B. Rost M. Palliative care initiation in pediatric oncology patients: A systematic review. Cancer Medicine. 2019; 8:3-12.
10. Zambrano JG. López LJ. Mucositis bucal parte III: Retos en el tratamiento. Acta Odontológica Venezolana. Volumen 57, No. 1, Año 2019.
11. Cordobilla R, Bollo de Miguel E. et al. Diagnóstico y tratamiento de la hemoptisis Arch Bronconeumol. 2016;52(7):368-377
12. Cheng B. Rost M. Palliative care initiation in pediatric oncology patients: A systematic review. Cancer Medicine. 2019; 8:3-12.
Síntomas gastrointestinales
1. Goldman A; Hain R; Liben R; (2021), Oxford Textbook of Palliative Care for Children; Third Edition; Oxford University Press.
2. Berger VD; Zandonade E; (2017); Prevalence of oral manifestations in children and adolescents with cancer submitted to chemotherapy. BMC Oral Healt. 2017; 17:49.
3. Hunt M; Protus B; Parker D; Winters J; (2014); Pediatric Palliative Care Consultant: Guidelines for Effective Management of Symptoms; HospiScript, ISBN: 978098895583;
4. White MC; Hommers C; Parry S; Stoddart PA; (2011); Pain management in 100 episodes of severe mucositis in children. Paediatr Anaesth.;21(4):411-6.
5. Palomo-Colli, M.Á; Soltero-Becerril, D; Juárez, L; Cícero, C; Gaytán-Morales, J; Castorena-Villa, I; Mier-Cabrera, M; (2018); Mucositis oral en niños con cáncer y su relación con limitación de actividades; Gaceta Mexicana de Oncología; Vol. 17; doi: 10.24875/j.gamo.M18000137.
6. Zambrano JG; López LJ; (2019); Mucositis bucal parte III: Retos en el tratamiento. Acta Odontológica Venezolana; Volumen 57, No. 1.
7. De la Teja-Ángeles, E; Niembro-Zermeño, A; 2011, Durán-Gutiérrez A; Mucositis Bucal; Acta Pediatr Mex; 32(4):255-256.
8. Wolfe J; Hinds P; Sourke B; (2011); Textbook of Interdisciplinary Pediatric Palliative Care, 1st Edition; Saunders; ISBN: 9781437702620.w
9. Malec M; Shega JW; (2020); Management of Gastrointestinal Symptoms (Nausea, Anorexia and Cachexia, Constipation) in Advanced Illness. Med Clin North Am. 2020; 104(3):439-454. doi: 10.1016/j.mcna.2019.12.005.
10. Paw Cho Sing E, Robinson PD, Flank J, Holdsworth M, Thackray J, Freedman J, Gibson P, Orsey AD, Patel P, Phillips R, Portwine C, Raybin JL, Cabral S, Sung L, Dupuis LL; (2019) Classification of the acute emetogenicity of chemotherapy in pediatric patients: A clinical practice guideline. Pediatr Blood Cancer. doi: 10.1002/pbc.27646.
11. Hauch H; et al; 2021; Gastrointestinal Symptoms in Children With Life-Limiting Conditions Receiving Palliative Home Care; Front. Pediatr. 9:654531. doi: 10.3389/fped.2021.65453.
Síntomas neuro-psiquiátricos
1. Goldman A; Hain R; Liben S; (2021); Oxford Textbook of Palliative Care for Children; Third Edition, Oxford University Press.
2. Tilton A, Vargus-Adams J, and M.R. Delgado; (2010) Pharmacologic Treatment of Spasticity in Children; Semin Pediatr Neurol.
3. Barkoudah E, Glader L; (2021); Cerebral palsy: Treatment of spasticity, dystonia, and associated orthopedic issues. En: UpToDate, Post TW (Ed), UpToDate, Waltham, MA. (accedido el 1 de agosto del 2021).
4. Delgado MR, Hirtz D, Aisen M, Ashwal S, Fehlings DL, McLaughlin J, et al. (2010); Practice parameter: pharmacologic treatment of spasticity in children and adolescents with cerebral palsy (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology and the Practice Committee of the Child Neurology Society; Neurology; 74: 336-343.
5. Clonazepam: Pediatric drug information. En: UpToDate, Post TW (Ed), UpToDate, Waltham, MA. (accedido el 1 de agosto del 2021).
6. Hauer J, Houtrow A; 2017, Pain Assessment and Treatment in children With Significant Impairment of the Central Nervous System; Pediatrics (6); 139.
7. Cervantes-Blanco JM; (2017), Medicina Paliativa en neurología pediátrica. En: Manual de neurología y neurocirugía pediátricas. Editorial Alfil. México.
8. Traube C, Silver G, Reeder RW, Doyle H, Hegel E, Wolfe HA, et al. (2017) Delirium in Critically Ill Children: An International Point Prevalence Study. Crit Care Med;45(4):584-90.
9. Colville G Kerry S, Pierce C; (2008). Children's factual and delusional memories of intensive care. American Journal of Respiratory and Critical Care Medicine, 177:976-982 available from: PM:18244955
10. Peritogiannis V, Bolosi M, Lixouriotis C, Rizos D V; (2015) Recent Insights on Prevalence and Corelations of Hypoactive Delirium. Behav Neurol. 2015.
11. Bettencourt A, et al, (2017). Delirium in Children: Identification, Prevention, and Management. Crit Care Nurse, 2017, vol. 37 no. 3 e9-e18
12. Robyn P; (2017) Pediatric Delirium, The American Journal of Psychiatry Residents' Journal, Volume 12, 2, Pag 6-8.
13. Franken A, Sebbens D, Mensik J. (2019) Pediatric Delirium: Early Identification of Barriers to Optimize Success of Screening and Prevention. J Pediatr Health Care. 2019; 33(3):228-233. doi: 10.1016/j.pedhc.2018.08.004.
14. R Traube C, Silver G, Kearney J, Patel A, Atkinson TM, Yoon MJ, et al. (2014) Cornell Assessment of Pediatric Delirium: A Valid, Rapid, Observational Tool for Screening Delirium in the PICU. Crit Care Med 2014; 42(3):656R63.
15. R Smith H, Fuchs DC, Pandharipande P et al. (2009) Delirium: an emerging frontier in the management of critically ill children. Crit Care Med 2009; 25:593R64.
16. R Smith H, Boyd J, Fuchs DC, et al. (2011) Diagnosing delirium in critically ill children: Validity and reliability of the Pediatric Confusion Assessment Method for the Intensive Care Unit. Crit Care Med 2011; 39:150R7.
17. Ricardo Ramírez C, Álvarez Gómez M, Franco Vásquez G, (2018) Delirium en niños. Factores de riesgo, diagnóstico, manejo y cuidados; Universidad Pontificia Bolivariana 2018. ISBN: 978-958-764-555-2.
18. Herbert A, De LIma J, Seton C, et al.; (2008); A survey of sleeping patterns in children admitted to the hospital. Sleep Biologic Rythms 6 (Suppl i); A49.
19. Owens JA; Pharmacotherapy for insomnia in children and adolescents: A rational approach. En: UpToDate, Post TW (Ed), UpToDate, Waltham, MA. (accedido el 1 de agosto del 2021).
20. Sheldon SH; Medical disorders resulting in problem sleeplessness in children. En: UptoDate, Post TW (Ed), UpToDate, Waltham, MA. (accedido el 1 de agosto del 2021).
Síntomas dermatológicos
1. Ana María Villa-Arango, Margarita, Aría Velásquez-Lopera. et al. Chronic pruritu. Revista Alergia México. 2019,66(1):85-98.
2. Lagos A, Tirado-Sánchez, Ponce-Olivera RM. Actualidades en el tratamiento del prurito crónico. Dermatol Rev. Mex. 2016 mayo;60(3)229-246
3. Ma. José Ledo García, Mónica García Mañero. et al. El prurito y sus efectos sobre la piel. Enfermera dermatológica. No. 16. Mayo - agosto 2012.
4. Julia Benedetti, MD, Harvard Medical School, última modificación del contenido feb. 2019.
5. Ma. Isabel Arias Gómez, Graciela Guzmán Perera. Et al. Consenso Mexicano del Tratamiento del Prurito. Cuernavaca, Morelos 13 al 15 de enero 2006.
6. Ulloa BJ. Fredes CF. Current management of xerostomía. Rev. Otorrinolaringol. Cir. Cabeza Cuello vol.76 no.2 Santiago ago. 2016.
7. LÓPEZ J, JANÉ E, CHIMENOS E. Pronóstico y tratamiento de la boca seca. Revisión Sistemática. Med Clin (Barc)2014; 142(3): 119-24.
8. Cheng B. Rost M. Palliative care initiation in pediatric oncology patients: A systematic review. Cancer Medicine. 2019; 8:3-12.
Urgencias paliativas
1. Reséndiz AJ, Pérez GE, Olivas GE, et al. (2019). Guía clínica. Definición y clasificación de la epilepsia. Rev Mex Neuroci. Supp 20; 62 - 67.
2. Olmos LA, Ibarra AJ, Cornelio NJ, et al; Guía clínica. Estado epiléptico en niños y adultos (2019). Rev Mex Neuroci. Supp 20; 111-116.
3. Panayiotopoulos CP, Pharmacopeia of prophylactic antiepileptic drugs. En: The Epilepsies: Seizures, Syndromes and Management. (2005). Oxfordshire. Pp. 497 - 525.
4. Currow D., Clark K. (2006). Emergencies in palliative and suportive care. Oxford University Press. Pp: 100-105.
5. O´Neill Hunt M., McCrate Protus B., Penfield Winters J., Et al. (2014). Dyspnea. Pediatric paliative care consultant, guidelines for effective management of symptoms. 1ª edición. Alabama. HospiScript; Pp: 109-116.
6. Pérez, C. (2009). Atención Primaria de Salud. Acercamiento a familias de pacientes con cáncer de mama. Revista PsicologiaCientifica.com, 11(13). Disponible en: http://www.psicologiacientifica.com/atencion-primaria-familias-pacientes-con-cancer
7. F. Muñoz Cobos., JM. Espinosa Almendro., J. Portillo Strempell., MA. Benítez del Rosario. (2002). Cuidados paliativos: Atención a la familia. Volumen 30, número 9. Pp: 576-580.
8. Goldman A, Hain R, Liben S. (2006). Oxford Textbook of Palliative Care for Children. Oxford University Press. 1st Ed. Haematological Symptoms. Chapter 29 pág. 462-467.
9. Bacciedoni V., Casanovas A., Lavergne M. (2020). Recomendaciones para el manejo de la lisis tumoral. Arch Argent Pediatr, 118(2). Pp: S59-S63.
Manejo de síntomas refractarios (sedación paliativa)
1. Cacciavillano, Walter. Soporte clínico oncológico y cuidados paliativo en el paciente pediátrico. 1ª ed.
2. Aleksandra Korzeniewska, Eksterowickz, Et al. Journal of Pain and Symptom Management. Volume 48, Issue 5, Noviembre de 2014: 968-974.
3. Charissa T. Jagt- van Kampen, Marianne D. van de Wetering. The timing, duration, and management of syntoms of children with an icurable brain tumor: a retrospective study of the pallative phase, Neuro- Oncology Practice 2(2), 70-77, 2015
4. Patrick McGrath, Bonnie Stevens. Et al. Oxford Textbook of Paediatric Pain
5. Velasco Pérez Georgina. Escalera Analgésica en Pediatría, Acta Pediátrica Mex. 2014; 35:249-255.
6. Joana Afonso, Flávio Reis, Dexmedetomidina: Rol Actual en Anestesia y Cuidados intensivos. Rev Bras Anestesiol, 2012;62:1: 118-133
7. Wiffen PJ, Cooper, eE al. Opioids for cáncer-related pain in cchildren and adolecents, Cochrane Database of Systematic Reviews 2017.
CAPÍTULO VI
ATENCIÓN PSICOSOCIAL, ESPIRITUAL Y DUELO EN LOS CUIDADOS PALIATIVOS PEDIÁTRICOS
6.1 ATENCIÓN PSICOSOCIAL
Considerando la definición de Cuidados Paliativos (CP) es imperativo incluir los estándares en la calidad de la atención para establecer un abordaje integral que incluya aspectos físicos, psicológicos, sociales y espirituales, para el niño y su familia ante una enfermedad crónica que compromete la vida, proporcionando soporte, regulación emocional, paliando el sufrimiento durante el tiempo de vida y posterior con el manejo del duelo. (1)
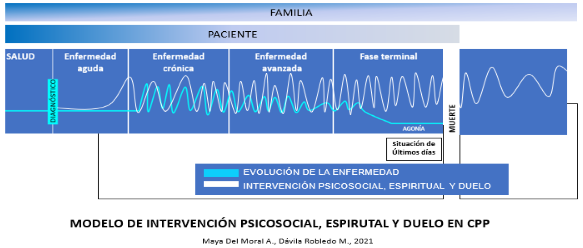
Diagrama 1.
Los cuidados paliativos son los cuidados de soporte que acompañan desde el diagnóstico y que no son excluyentes del tratamiento curativo, sino que complementan en beneficio del paciente y su familia. (2,3) El objetivo del control sintomático es mejorar las condiciones, brindar la posibilidad de un proceso vital confortable acorde a las características propias de su edad, enfermedad, aspectos socioculturales y familiar, así como permitir, dignificar una muerte natural, garantizando calidad y confort. Al mismo tiempo es imprescindible conocer las emociones que emergen en este proceso de enfermedad y muerte, para normalizarlas como parte de la condición humana e identificar los momentos en lo que el sufrimiento puede ser evitable, brindando estrategias para mejorar la adaptación del paciente y familia.
La intervención de psicología es esencial en el proceso de salud- enfermedad-muerte, tiene como objetivo principal la adaptación a la condición que limita y demanda, viviéndose como una crisis de cambio donde las emociones, pensamientos y conducta emergen tendiendo a fluctuar, en algunas ocasiones como factores protectores que permiten enfrentar y aprender de la situación y otras veces como causas de sufrimiento sin encontrar una ruta por donde dirigir la toma de decisiones. (4) Por lo anterior la obviedad de la vulnerabilidad que el ser humano enfrenta ante la enfermedad y posteriormente la muerte, requiere un soporte emocional continuo.
| | Factores para considerar en el niño y adolescente en CPP. |
| | Etapa de crecimiento y desarrollo (Físico, Psicológico, social y espiritual) incluyendo el desarrollo del lenguaje. |
| | Comprensión sobre la vida, la enfermedad y muerte. |
| | Estructura y dinámica familiar, identificando al cuidador primario. |
| | Conocimiento de la enfermedad y posible evolución de complicaciones. |
| | Contexto sociocultural y económico. |
| | Factores de riesgo y protección psicosociales para la adherencia terapéutica. |
| | Identificar los objetivos de la terapéutica para el paciente. |
Tabla 6.1
La intervención psicosocial en los Cuidados Paliativos Pediátricos (CPP), se debe considerar prioridad para identificar barreras o limitaciones en la atención emocional y social, de una forma más humana, ética y profesional ante la enfermedad incurable, la evolución de síntomas que disparan crisis y desajuste emocional. (6)
Atención psicosocial del niño/adolescente en CPP.
a. Comprensión de enfermedad y etapas del desarrollo; y
b. La evaluación de niños y adolescentes, para identificar su contexto familiar, sociocultural y educativo es un reto en constante evolución en el campo de la atención a la infancia.
La etapa pediátrica abarca la infancia y adolescencia con características muy específicas, en constantes cambios que impactan en su desarrollo, sin embargo, ante un diagnóstico y pronóstico desfavorable para la función, niños y adolescentes, expresan sentimientos, emociones y conductas que se disparan ante una crisis de salud. Por una parte, habilidades o períodos críticos que ya habían sido superados presentan una regresión y por otra parte a nivel cognitivo y conductual expresar madurez y comprensión de su cuerpo, gravedad incluso el deterioro progresivo.
| Etapas de desarrollo | Sentimientos, emociones y conductas. |
| Hasta los dos años | No entienden la enfermedad. Sufren por la separación de los padres. Manifestaciones de incomodidad y alteraciones de hábitos. |
| Dos a seis años | Comprenden lo que es una enfermedad. Una enfermedad siempre viene de fuera (etapa de fantasía). Enfermedad temporal. |
| Siete a doce años | Comienzan a percibir la muerte como algo irreversible y universal. Sienten miedo. Se cuestionan la seguridad de la vida. ¿Tú también te vas a morir? Curiosidad e interés por las reacciones de su cuerpo y sobre a muerte. |
| Etapa escolar (9 a 12 años) | Mayor conocimiento del cuerpo. Entiende lo que es enfermedad. Capacidad de colaborar en el tratamiento. En busca de explicaciones. |
| Doce años en adelante | Comprende la complejidad de la enfermedad y su tratamiento. Necesidad de tomar decisiones. |
Tabla 6.2 Comprensión de la enfermedad.
El significado de una enfermedad limitante para la función y la vida varía según la edad (Tabla 6.2), sin embargo, es inevitable que niños y adolescentes de diferentes diagnósticos se enfrenten a condiciones que limitan su vida a corto plazo y con ello es imperativo el apoyo psicológico que de soporte en pro de su calidad de vida. (7,8)
Al considerar el proceso de comprensión, se podrá planificar estilo, medios para una efectiva comunicación y soporte emocional, que permita con mayor calidad y calidez la colaboración con el niño y adolescente. El abordaje para evaluar a nivel emocional, cognitivo y conductualmente al paciente podrá ser de forma objetiva o subjetiva con instrumentos de evaluación que permitan plantear la intervención necesaria.
La intervención psicosocial considera la evaluación como parte de la detección de necesidades que impactan en las emociones, pensamientos y conducta de niño y/o adolescente incluyendo a su familia, brindando contención para mejorar su soporte y adaptación emocional. A la intervención se deben precisar los objetivos que puedan ser alcanzados desde los que se perciban como más preocupantes o amenazantes hasta los más sutiles que de confort y armonía.
Niño/adolescente en CPP. El abordaje de los aspectos psicosociales en el paciente pediátrico será de acuerdo con su condición en relación con la evolución y complicaciones de la enfermedad, a sus necesidades emocionales, espirituales, contexto familiar y social.
Ante la evolución se debe considerar la interacción con el paciente dependiendo de su funcionalidad (Tabla 6.3), considerada como el nivel en la perdida de la reserva energética y funcional de múltiples órganos y sistemas, que compromete la capacidad para afrontar las demandas del día a día y dar una respuesta.
| | Funcionalidad | |
| | Alta funcionalidad | Baja funcionalidad |
| · Acercamiento y contacto progresivo desde el momento diagnóstico · Utilizar como medio el juego para favorecer la interacción o sus gustos e intereses · Información y comunicación clara y congruente, adecuada a la edad · Conocer la etapa de desarrollo cognitivo del niño y/o adolescente para establecer el estilo y grado de comunicación · Ayudar a la expresión emocional en total aceptación | · Mantener el acercamiento y adaptación a su condición de interacción con el medio · Ayudar a la expresión emocional y forma de demostrar a las personas significativas su aprecio, agradecimiento y despedida. · Consolidar sentimientos, cohesión y asegurar sus cuidados. · Eliminar o atenuar síntomas que limiten su calidad de vida. · Apego y expresiones de los sentimientos. | |
Tabla 6.3
Reacción emocional del niño y el adolescente. Las reacciones psicológicas se incrementarán y fluctuarán con el tiempo, relacionado a síntomas más intensos, agudos o refractarios del paciente, ya que vislumbra la culminación de la vida y transformación de la esperanza, por ello el seguimiento psicosocial es la clave para un soporte emocional óptimo. (9) En la tabla 6.4 se presentan por etapas las reacciones psicológicas esperadas ante las diferentes condiciones de una enfermedad crónica o que pone en riesgo la vida, así como opciones de intervención de acuerdo con la etapa de esta. (10)
| DIAGNÓSTICO | REACCIÓN: Preescolar: Ansiedad de separación, enojo, confusión, llanto, cambios conductuales, modificación de hábitos, irritabilidad. Escolar: Ansiedad, reacciones regresivas, agresión/enojo, llanto. Adolescente: Aislamiento, mutismo, rechazo, tristeza, impotencia, enojo, conductas regresivas. INTERVENCIÓN: Preescolar: Acercamiento de personas significativas que brinden seguridad. Incorporación de rutina y hábitos. Terapia de juego. Modificación de cambios conductuales. Escolar: Contención emocional. Estrategias de afrontamiento. Adherencia terapéutica. Terapia de juego. Adolescente: Adaptación y autocontrol. Expresión emocional. Toma de decisiones. Adherencia terapéutica. |
| MAL PRONÓSTICO | REACCIÓN: Prenatal/neonatal: Incredulidad de los padres, esperanza de curación, frustración/impotencia, culpa, ansiedad, ambivalencia, tristeza, incertidumbre, desesperanza, preocupación, estrés. Preescolar: Mutismo selectivo, rechazo, tristeza, enojo, modificación de hábitos (sueño, alimentación), problemas de conducta. Escolar: Mutismo selectivo, incertidumbre, tristeza. Susceptible a la reacción verbal y no verbal de los demás. Problemas de conducta. Indiferencia. Enojo. Adolescente: Enojo, frustración, tristeza, aislamiento, abandono, desinterés, conductas de riesgo o autolesivas. INTERVENCIÓN: Prenatal/neonatal: Intervención en crisis. Regulación emocional. Propiciar la comunicación entre la pareja. Duelo anticipado. Toma de decisiones. Comunicación. Informes constantes sobre la situación médica. Garantizar los cuidados durante el embarazo y de soporte al neonato con calidad y calidez. Preescolar: Técnicas de distracción y juego. Apego seguro. Expresión de emociones y sentimientos a través del juego y arteterapia. Técnicas de respiración. Escolar: Técnicas de distracción y juego. Arteterapia. Musicoterapia. Técnicas de respiración y relajación. Adolescente: Permitir la elección de un confidente. Escucha activa. Expresión de emociones y sentimientos a través de gustos y preferencias. Importancia de la toma de decisiones. Conductas de autocuidado. Validar sentimientos. |
| AVANZADA | REACCIÓN: Preescolar: Mayor dependencia de cuidados, mayor apego con personas significativas, miedo, Llanto. Escolar: Inseguridad, miedo, enojo, rechazo, indiferencia, aislamiento. Adolescente: Aislamiento, desamparo, soledad, desesperanza, sufrimiento. INTERVENCIÓN: Preescolar: Confort, garantizar atención a síntomas para eliminarlos o atenuarlos, reforzar momentos de distracción, apego seguro, expresión de emociones. Escolar: Participación de su cuidado de acuerdo con su funcionalidad. Expresar sus sentimientos y deseos, así como sus miedos. Mantener interacción social. Regulación emocional. Garantizar atención a síntomas para eliminarlos o atenuarlos. Adolescente: Reforzar autoestima y autonomía. Disponibilidad para escuchar y atender sus preocupaciones. Participación en la conversación y opciones terapéuticas de su condición. Facilitar su interacción con pares y actividades significativas. Garantizar atención a síntomas para eliminarlos o atenuarlos. |
| AGONÍA | REACCIÓN: En todas las etapas, dependiendo de la evolución y síntomas presentes, expresarán miedo, temor, llanto, ser escuchados o por el contrario la imposibilidad de hablar limitará peticiones, incomodidad y malestar, incluso también tranquilidad y agradecimiento. INTERVENCIÓN: Prenatal/neonatal: Intervención en crisis. Facilitar recuerdo y despedida. Permitir el contacto físico con el bebé que da consuelo y posterior ajuste emocional. Acompañamiento de la pareja o familia. En general, en todas las otras etapas: Acompañamiento en la despedida. Expresión de sentimientos, emociones y agradecimiento. Garantizar hasta el último momento los cuidados y manejo de síntomas. Respeto al contexto sociocultural del paciente. Reforzar su legado y trascendencia desde la compasión. Facilitar su forma de despedirse apegándose a su fe y creencias. Acompañamiento de personas significativas. |
| MUERTE | INTERVENCIÓN: Prenatal/neonatal: Escucha activa. Respeto. Comprensión. Red social que de soporte. Sensibilidad y tiempo ante la despedida. Privacidad. Facilitar su forma de despedirse apegándose a su fe y creencias. Garantizar el cuidado médico de la madre y su soporte emocional. Respeto y cuidado del cuerpo. |
| Tabla 6.4 | |
Respuestas desadaptativas en el niño. Existen reacciones o respuestas emocionales desadaptativas que limitan y bloquean la expresión de las emociones y el aumento del sufrimiento: Inhibición emocional, respuestas somáticas, mutismo generalizado y aislamiento. El niño y adolescente es susceptible a percibir su medio hostil, agresivo, con mentiras y temores, incluyendo la culpa que limiten su relación con los demás por no sentirse más vulnerable emocionalmente o por culpa de ser el generador de sufrimiento. Identificar sus temores y preocupaciones permitirá evitar reacciones que tiendan a vivir estos momentos de un franco deterioro físico, en soledad. (9) Apegados a su nivel de desarrollo, características de la enfermedad y evolución, aspectos personales como gustos, intereses, personalidad y contexto o ambiente, junto con la evaluación de su soporte emocional, guiará la intervención para organizar su mundo incluso su despedida.
Familia. La familia ante estos eventos cursa por un proceso de alta demanda emocional y cognoscitiva, haciendo uso de sus recursos internos y externos, expresando emociones y sentimientos, omitiendo sus propias necesidades que fluctúan dependiendo de la evolución de la enfermedad, complicaciones y alivio/control de los síntomas; impactando de forma directa en su estado emocional, la forma de interactuar con el niño/adolescente en el proceso de duelo y entre los demás integrantes de la familia. Por lo tanto, es muy importante identificar las necesidades (Tabla 6.5) de los cuidadores primarios, de la estructura y dinámica familiar, fortalecer la toma de decisiones y conductas ante las diferentes situaciones clínicas y sus efectos psicosociales recurrentes, que pueden considerarse como factores de riesgo y/o protectores en el niño y su familia.
| | Necesidad de salvar, proteger y cuidar a su hijo |
| | Necesidad de saber cómo manejar la información y comunicación. |
| | Necesidad de dar continuidad a la dinámica familiar, incluyendo la atención a los hermanos. |
| | Necesidad de solventar y resolver la situación económica. |
| | Necesidad de conocer y aprender los cuidados al niño o adolescente. |
| | Necesidad de organizar y planificar las actividades incluyendo el descanso. |
| | Necesidad de expresión de las emociones. |
| | Necesidad de transformar la esperanza en relación con sus valores. |
| | Tabla 6.5 |
Reacción emocional en la familia: Las emociones y sentimientos que emergen de situaciones límite confrontan con el tiempo, expectativas y planes que quedan bloqueados por la incertidumbre. La familia al igual que el paciente, viven la experiencia de una enfermedad y mal pronóstico como una amenaza real y potencial a su integridad, cohesión y futuro. (9) Acompañada de confusión, enojo e inclusive agresividad en conductas y actitudes, la siguiente tabla (Tabla 6.6) concentra las reacciones y su intervención:
| | FAMILIA |
| DIAGNÓSTICO | REACCIÓN |
| Sentimientos de culpa. Frustración. Impotencia. Enojo. Incertidumbre. Esperanzas de curación. | |
| INTERVENCIÓN | |
| Contención emocional. Estrategias de afrontamiento. Solución de problemas/toma de decisiones. Adherencia terapéutica. Reorganización de los roles. | |
| MAL PRONÓSTICO | REACCIÓN |
| Impotencia. Ambivalencia. Rabia. Inseguridad. Desesperanza. Culpa. Fracaso. | |
| INTERVENCIÓN | |
| Contención emocional. Toma de decisiones. Información constate de la evolución de la enfermedad. Identificar sobrecarga en el cuidador y la familia. Integración en los cuidados y toma de decisiones de su hijo. Respetar los tiempos para cada familia e integrante sobre la asimilación de la información. Comunicación con el equipo de salud. | |
| AVANZADA | REACCIÓN |
| Agotamiento físico y emocional. Miedo. Tristeza. Incertidumbre. Depresión. Transformación de la esperanza. | |
| INTERVENCIÓN | |
| Planificación anticipada que de seguridad en los cuidados y en la presencia de posibles complicaciones. Movilizar recursos internos y externos que den soporte. Promover la expresión de emociones y sentimientos en cada uno de los integrantes de la familia. Participación y aprendizaje en los cuidados del cuidador primario y de toda la familia. Promover las habilidades sociales en la familia. Prevención y detección de conflictos Identificar por sus creencias socioculturales los rituales ante la muerte. Acompañamiento emocional hasta el momento de la muerte. | |
| AGONÍA | REACCIÓN |
| Ansiedad. Tristeza. Llanto. Miedo. | |
| INTERVENCIÓN | |
| Facilitar la despedida y rituales. Privacidad ante las muestras de despedida. Preparación del duelo inmediato. Valorar el soporte emocional. Ambiente de confianza para expresión de sentimientos y emociones. Redes de apoyo. Acompañamiento. | |
| MUERTE | REACCIÓN |
| Tristeza Llanto Shock. Reacciones físicas. | |
| INTERVENCIÓN | |
| Contención emocional. Respeto a las creencia religiosas o rituales. Promover el agradecimiento y expresión de sentimientos. Garantizar las necesidades básicas de los dolientes. Acompañamiento en trámites funerarios. |
Tabla 6.6
Reacciones desadaptativas en la familia. En la progresión de la enfermedad, mal pronóstico y muerte se considera normal las reacciones emocionales que la familia ha de enfrentar. Ante el contexto cambiante y la vulnerabilidad emocional, existen reacciones desadaptativas, que desde el primer contacto con los integrantes y sobre todo el cuidador primario se debería identificar para que se puedan predecir dichas conductas y ayudar a prevenirlas.
Las reacciones desadaptativas presentes son: la conspiración del silencio, claudicación familiar, sobrecarga, negación, conflictos de roles y límites, así como conflictos familiares presentes antes del diagnóstico y exacerbados por la situación de más demanda de cuidados y movilización de recursos para cubrir las necesidades del paciente. Una vez identificadas dichas reacciones desadaptativas se debe considerar una intervención específica para eliminar, atenuar o mediar la causa, favoreciendo la relación de cada uno de los integrantes en una mejor cohesión, respeto y consolidación de sentimientos para expresarlos antes del fallecimiento. (8)
En el equipo de salud. El personal de salud que atiende a pacientes crónicos en la búsqueda de curación o en su caso alargar el tiempo de vida, con los menos efectos secundarios, comunicar un mal pronóstico que enfrenta al final de la vida, está expuesto a respuestas de estrés ya bien descritas y en ocasiones a la presentación de características del síndrome de Burnout, por la alta exigencia física, emocional que representa la atención de un niño en condiciones críticas, la agonía, el sufrimiento y el comunicarse con su familia (Tabla 6.7).
| | EQUIPO DE SALUD |
| DIAGNÓSTICO | REACCIÓN |
| Expectativa de curación. | |
| INTERVENCIÓN | |
| Establecer alianza terapéutica (paciente-familia-equipo). Habilidades de comunicación. | |
| MAL PRONÓSTICO | REACCIÓN |
| Sentimiento de culpa. Fracaso. Confusión. Estrés. | |
| INTERVENCIÓN | |
| Trabajar en equipo interdisciplinario para establecer objetivos realistas. Compartir decisiones equipo-familia. Comunicación clara y abierta con la familia, para mantener congruencia y seguimiento en las decisiones. Empatía y escucha activa ante las necesidades-recursos del paciente y familia. | |
| AVANZADA | REACCIÓN |
| Agotamiento emocional y físico. Indiferencia. Fracaso profesional. Fracaso personal. Estrés. | |
| INTERVENCIÓN | |
| Valoración de estrés, fatiga por compasión y burnout. Habilidades de comunicación. Aprender estrategias de empatía y Ecpatía. Expresión de emociones. Compartir responsabilidad y toma de decisiones en equipo. Gestión y optimización del tiempo. | |
| AGONÍA | REACCIÓN |
| Estrés. Agotamiento físico y emocional. | |
| INTERVENCIÓN | |
| Toma de decisiones por eventualidades. Apoyarse por la planificación anticipada. Reparto de roles dentro del equipo. Aprendizaje para estrategias de respiración y relajación. Estrategias de escucha empática. | |
| MUERTE | REACCIÓN |
| Impotencia. Bloqueo de emociones. Reacciones físicas. | |
| INTERVENCIÓN | |
| En equipo valorar la intervención, con oportunidades de mejora. Reforzar estrategias de autocuidado y soporte para el equipo. Buscar y pedir ayuda para estabilidad emocional. Manejo del duelo de pacientes. Autoconocimiento sobre pérdidas/auto observación. Promover el desarrollo espiritual. Solicitar ayuda profesional. Hábitos saludables. Autorregulación emocional. | |
| Tabla 6.7 | |
Un tema importante para el equipo es la toma de decisiones y la comunicación con la familia para ofrecer manejo o intervención específica, como por ejemplo no reanimación, no ventilación mecánica, etc. que permite planear de forma anticipada el manejo al final de la vida, donde el trabajo en equipo es de gran importancia. (3)
Planificación anticipada: El conocer desde el diagnóstico al paciente permite conocer las circunstancias, el contexto de la enfermedad permite iniciar un control emocional en el que se llevará el proceso de la planificación de cuidados, incluyendo la prevención de crisis ante la falta de información, mala comunicación o confusión dependiendo de las expectativas de cada integrante.
Las acciones del equipo de salud ante la toma de decisiones, la adecuación de esfuerzo terapéutico les permite consolidar la decisión ante un balance de ventajas y desventajas que den seguridad a los familiares y sobre todo al paciente, sin un sentimiento de culpa que aumente su sufrimiento. Igualmente, importante el brindar contención a la expresión emocional del personal en el manejo del duelo anticipado, al saber que la relación con su niño/adolescente cambiará, y dependiendo del objetivo de las decisiones conocer bien los recursos internos y externos de la familia y del paciente siendo actores activos en este proceso, para así conocer las responsabilidades compartidas y confort del paciente. (11)
El equipo de salud debe mostrar disposición y apertura a la escucha de necesidades, potencializar recursos internos-externos del paciente y su familia para disminuir su percepción de vulnerabilidad e indefensión, por un control de la situación a través de la toma de decisiones con el balance de costo-beneficio y mantener un equilibrio entre la esperanza, una verdad soportable en el marco de los derechos humanos y la bioética.
Finalmente, en las últimas décadas la Psicología ha experimentado avances con evidencia científica en intervención con técnicas y estrategias para cubrir de forma holística las dimensiones del ser humano. La eficacia de intervenciones psicológicas con un sustento científico que están dando luz para dar seguimiento al soporte psicológico en condiciones límite como es la enfermedad crónica, la progresión de la enfermedad, la muerte y duelo como son la psicoeducación, técnicas de respiración y relajación e hipnosis. Se ha descrito el impacto favorable de las terapias cognitivo-conductuales como desensibilización sistemática, reestructuración cognitiva, entrenamiento en la inoculación de estrés entre otras que son aplicables, evaluando el caso pero que permite dar estabilidad a la emoción, pensamiento y conducta.
Y sin obviedad la entrevista sigue siendo el estándar para la relación bidireccional y humana que permite conocer las necesidades y recursos de las percepciones desde su interpretación de la crisis por las que están transitando. (4)
Incorporando lo más reciente como las terapias de tercera generación, con el enfoque humanista, resaltando el nivel espiritual y de valores como la Terapia de aceptación y compromiso, mindfulness, terapia narrativa basada en mindfulness, activación conductual. Con técnicas específicas como el Counselling, regulación emocional, escucha activa y compasión. (11)
6.2 ESPIRITUALIDAD EN CUIDADOS PALIATIVOS PEDIÁTRICOS
Un informe de la OMS (1990) afirma que la espiritualidad se refiere a aquellos aspectos de la vida humana, que tiene que ver con experiencias que trascienden los fenómenos sensoriales. La dimensión espiritual de la vida humana puede ser vista como un componente integrado junto con los componentes físicos, psicológicos y sociales. A menudo se percibe como vinculado con el significado y el propósito y para los que están cercanos al final de la vida, se asocia comúnmente con la necesidad de perdón, reconciliación y afirmación en los valores. (12)
Definición: "La espiritualidad es un aspecto dinámico e intrínseco de la humanidad a través del cual las personas buscan un significado, un propósito y una transcendencia últimas y experimentan una relación consigo mismos, con la familia, con los demás, con la comunidad, con la sociedad, con la naturaleza, con lo significativo y con lo sagrado. La espiritualidad se expresa a través de las creencias, los valores, las tradiciones y las prácticas". (13)
El acompañamiento espiritual como dimensión de los cuidados paliativos. El acompañamiento
espiritual es la práctica de reconocer, acoger y dar espacio al diálogo interior de aquel que sufre, para que él mismo pueda dar voz a sus preguntas y dar vida a sus respuestas. Es decir, ayudar a la persona a despertar o a sacar a la luz el anhelo, la búsqueda interior que toda persona puede tener" (SECPAL, 2008). La espiritualidad en los cuidados paliativos para pacientes pediátricos trabaja con el paciente y sus padres y/o cuidador primario.
| 1. Los modelos de cuidados espirituales ofrecen un marco de referencia para que los profesionales de la salud puedan conectar con sus pacientes, escuchar sus miedos, sueños y dolor, colaborar con sus pacientes como aliados en su cuidado y proveer, a través de la relación terapéutica, una oportunidad de sanación. |
| 2. La sanación se distingue de la curación. Se refiere a la habilidad de una persona para encontrar alivio, consuelo, conexión, significado y propósito en medio del sufrimiento, la desazón y el dolor. |
| 3. Los cuidados espirituales están cimentados en marcos teóricos importantes, uno de los cuales es el Modelo Bio-psicosocial-Espiritual de Cuidados |
| 4. Otro de los fundamentos es un modelo de cuidados centrado en el paciente, en el que el enfoque de cuidados se centra en éste y en su experiencia de la enfermedad, en vez de centrarse en exclusivamente en la enfermedad. |
| 5. La visión de la persona como ser-en-relación es piedra angular del acompañamiento. |
| 6. La vida es esencialmente relaciones; y relación como tal implica trascendencia, un ir más allá de sí mismo por parte de aquello involucrado en la relación. |
| 7. La enfermedad puede ser comprendida como una disrupción en las relaciones adecuadas que constituyen la unidad e integridad de lo que conocemos como ser humano. |
| 8. La profesión sanitaria es, intrínsecamente, una profesión espiritual. Cuando interactúan un profesional de la salud y un paciente en una relación profesional, la transformación que tiene lugar es inherente al modelo propuesto de cuidados espirituales. |
| 9. Al cuidar de las personas que sufren, para el profesional de la salud se abre la oportunidad de transformación personal. Para estar abierto a ella, el profesional debe tener conciencia de las dimensiones espirituales en su propia vida y apoyarse en un proceso de reflexión para la práctica de la presencia compasiva con los pacientes. |
| 10. La espiritualidad entendida como nuestra naturaleza esencial de donde surge nuestro anhelo inagotable de plenitud es un universal humano. Se expresa a través de nuestra red de relaciones, las que establecemos con nosotros mismos, los demás y lo que nos trasciende. |
| 11. "Los que sufren no son los cuerpos, son las personas", El sufrimiento se da en el ámbito subjetivo: centrados sólo en lo objetivo los profesionales no lo pueden explorar ni atender. |
| 12. Los clínicos encuentran sufrimiento evitable y no evitable. Hay un sufrimiento que forma parte de nuestra condición existencial, pertenece a la experiencia del misterio y se puede trascender y acompañar, pero no resolver. |
| 13. Disponer de un modelo antropológico, que entiende a la persona como parte de la conciencia que aspira a la integridad, a la integración y la plenitud, puede ayudarnos a entender y atender el sufrimiento. |
| 14. El itinerario del proceso de trascendencia del sufrimiento se reconocen tres etapas, identificadas como: CAOS, etapa muda, de enclaustramiento o de lucha» ACEPTACION, de entrega o etapa expresiva o de transición» TRASCENDENCIA, maduración o de nueva identidad |
| 15. La trascendencia del sufrimiento, y disolución de la perspectiva limitada de la persona, abre un panorama ampliado de sí mismo y de la realidad, y es el camino más poderoso para restaurar la integridad a un nivel de conciencia superior. |
| 16. La sanación como proceso de recuperación de la integridad y armonía, a través de trascender el sufrimiento, puede ser una propuesta clave de la intervención compasiva en el acompañamiento espiritual. |
| 17. Las herramientas del acompañante son HOSPITALIDAD, PRESENCIA Y COMPASIÓN |
| 18. La presencia ecuánime y compasiva del terapeuta posibilita que el que sufre pueda adentrarse y atravesar y trascender conscientemente la visión limitada de sí mismo, y entregarse a la profundidad de su Ser. |
| 19. El acompañante debe desarrollar un nivel de conciencia, ecuanimidad y compasión y ser consciente de sus límites para poder acompañar. (14) |
| Tabla 6.8 Acompañamiento espiritual en los CPP |
Proceso de morir. Modelo para explicar la adaptación psico-emocional al proceso de final de vida.
Singh, partiendo de la observación del proceso que frecuentemente siguen los enfermos en los últimos días, propone un modelo para explicar la adaptación psicoemocional al proceso y los pasos que se dan en esta etapa son: (14)
1. Etapa de caos, caracterizada por la lucha, la negación, la depresión, negociación, y por el miedo a perder lo que consideramos nuestra integridad (es el miedo a la pérdida del EGO) o el miedo a la pérdida de los mecanismos compensatorios;
2. Etapa de rendición o renuncia, entrega, aceptación, soltar, dejarse, dejar de luchar, etc., lo que en la práctica coloquialmente decimos "tirar la toalla", pero no como un planteamiento de derrota, sino de entrega; y
3. Trascendencia, Llamado así por Singh, cuando finalmente se ha hecho esta entrega, la persona entra en un nuevo espacio de conciencia, un estado modificado de conciencia, un espacio de paz, serenidad, gozo, bienestar, que podemos observar en las fases finales de algunos enfermos. (14)
Proceso del paciente: Se caracteriza por en tres fases. Singh, describe el proceso diciendo: "El único camino hacia el ámbito transpersonal es a través del examen y entrega completa del sentido personal del yo. Cuando en una enfermedad terminal uno comprende que no tiene escapatoria de su sufrimiento, entonces empieza a comprender. Las intuiciones que abren nuestra nueva comprensión solo llegan a través de los agujeros que se producen cuando se agota nuestra resistencia, entonces empezamos a percibir la verdadera naturaleza de nuestro SER, (Aceptación), es entonces cuando empezamos a disolver nuestra mente ordinaria...la Luz empieza a entrar a través de las brechas de su ausencia. Este es el principio de la plenitud de conciencia, es el principio de la apertura espiritual. Es la entrega de la lucha, del apego, del desespero (La trascendencia). (14)
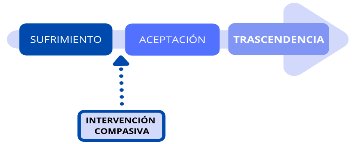
Diagrama 2. Proceso del paciente.
Metodología de intervención espiritual en la clínica
Detección. Se realiza a partir de diversos indicadores de expresión emocional, valores o conflictos éticos, que acompañan la experiencia espiritual, por lo que hay que estar atentos a: (13)
· Preguntas radicales que surjan de forma espontánea del paciente;
· Comentarios que se relacionen con la taxonomía de necesidades espirituales del paciente pediátrico;
· Afirmaciones que reflejen temor o preocupación por no sanar y morir, lo que ocurrirá consigo y/o con sus padres y sus seres queridos si no se cura, etc.;
· Enunciados que describen potenciales o reales recursos espirituales; y
· Objetos que evocan vínculos con lo espiritual, como rosario, biblia, libro de oraciones, cuentos religiosos, estampas, etc.
Exploración. Se sugiere que los profesionales del equipo interdisciplinario de cuidados paliativos hagan preguntas de rutina en relación con la presencia y relevancia de la espiritualidad, en el contexto de la historia clínica. (13) Aquí se presentan dos instrumentos de evaluación simples y prácticos para la exploración de la espiritualidad, aplicables a paciente a partir de los 8 años (cuando el niño o niña empieza a tener pensamientos concretos con relación a la espiritualidad), así como también pueden ser utilizados con sus cuidadores primarios.
· Modelo FICA de Evaluación Espiritual Breve. (15) Puchalski (2001) creó un modelo breve de evaluación espiritual basado en el acrónimo FICA: Fe, Importancia, Comunidad y Acción. (González Rivera, Espiritualidad en la Clínica); y
· Modelo iCARING de Evaluación Espiritual Breve. Hodge (2015) desarrolla el modelo de evaluación breve con el acrónimo: importancia, Comunidad, Activos y Recursos, Influencia, Necesidades y Metas.
| Acrónimo | Área | Pregunta de ejemplo |
| F | Fe | ¿Te consideras una persona espiritual o religiosa? |
| I | Importancia | ¿Qué tan importantes son las creencias espirituales y la fe en sus vidas? |
| C | Comunidad | ¿Formas parte de alguna comunidad religiosa o espiritual? |
| A | Acción | ¿Le gustaría que platiquemos de asuntos relacionados a tu fe/espiritualidad/religión en terapia? |
| Tabla 6.9 Modelo FICA | ||
| Acrónimo | Área | Pregunta de ejemplo |
| i | Importancia | ¿Qué tan importante es la espiritualidad/religión para ti? |
| C | Comunidad | ¿Formas parte de alguna comunidad religiosa o espiritual? |
| A R | Activos y Recursos | ¿Tienes alguna creencia o práctica espiritual que te sirva de ayuda y fortaleza en los momentos difíciles? |
| I | Influencia | ¿Existe relación entre tu espiritualidad y tus problemas presentes? ¿Crees que tu espiritualidad te puede ayudar en este momento? |
| N | Necesidades | ¿Tienes alguna necesidad o preocupación espiritual que desees trabajar en terapia? |
| G | Metas | ¿Te gustaría que incluyamos tu espiritualidad en la terapia? ¿De qué manera? |
| E | Efectos en el cuidado médico y efectos existenciales | ¿Me permites ayudarte a trabajar con los recursos espirituales que son fortaleza para ti? ¿Existe conflicto entre el tratamiento y tus creencias? ¿Te gustaría incluir como parte del tratamiento a algún líder religioso o guía espiritual? |
| Tabla 6.10 Modelo iCARING | ||
Nota: Estos modelos muestran ejemplos de preguntas para explorar cada área de la espiritualidad, pero debe adecuarse a la edad del niño a partir de los seis años cada pregunta, y se recomienda apoyarse en esta exploración con títeres, cuentos, juguetes, dibujos, etc. de manera que se logre con el niño la comunicación efectiva que se requiere en la evaluación, sin generar estrés o tensión en el paciente.
El acompañamiento espiritual como intervención terapéutica
Intervención Compasiva:(12) Los pacientes pediátricos en cuidados paliativos se dan cuenta lo que pasa con su enfermedad, no sólo identifican los cambios que ocurre en su cuerpo, sino también identifican que sus emociones y el contexto que los rodea se modifica, pues perciben preocupación, tristeza, estados de ánimo diferentes tanto en familiares como en el equipo de salud que lo atiende, en consecuencia surgen dudas, temores, incertidumbre en el paciente menor de edad, y no siempre se atreven a preguntar, es en este momento cuando se debe brindar la intervención compasiva, acompañada de creatividad, empatía, escucha activa, manejo de silencios y atención plena.
El acompañamiento espiritual como intervención terapéutica se basa en la intervención compasiva, en sintonía con el sufrimiento del enfermo, donde el profesional comparte al mismo tiempo su vulnerabilidad, su propia experiencia trascendente y aporta su presencia como sanador herido. Esta intervención puede ayudar al enfermo a cruzar el puente que lleva del sufrimiento a la aceptación, la entrega y hacia la trascendencia, con ello a la sanación. Entendida ésta como recuperación de la integridad y coherencia a un nivel de conciencia superior al previo. A través de la intervención compasiva, el que sufre y el que le acompaña acaban en un espacio distinto caracterizado por el crecimiento y la visión más madura de la realidad. Es fundamental para atender el sufrimiento, la disponibilidad del clínico para diagnosticarlo, su interés y para conocer sus causas, identificar el grado y los recursos, estrategias y posibilidades del enfermo para afrontarlo. (14)
Pasos para la Intervención Compasiva:
· Establecer una relación de confianza y un vínculo terapéutico;
· Identificar el sufrimiento;
· Identificar las causas del sufrimiento;
· Intentar resolver o desactivar las amenazas que puedan resolverse.
· Explorar los recursos y capacidades del paciente para trascender su sufrimiento; y
· Intervención Compasiva, orientando al paciente hacia la búsqueda de una visión transcendida de lo que percibe como amenaza.
Atención centrada en la persona: Desde la atención centrada en la persona no es necesario que el equipo interdisciplinario elabore un plan de atención en función de lo que consideran mejor para el paciente, desde este enfoque la elaboración del plan de atención parte de preguntar a la persona qué quiere y cómo lo quiere, partiendo de aquí el equipo de profesionales de cuidados paliativos diseña las estrategias para facilitar al paciente a alcanzar sus metas.
Desde la metodología de atención centrada en la persona se busca:
· Favorecer la independencia funcional de la persona el mayor tiempo posible;
· Crear las condiciones para que la persona sea capaz de dirigir su vida en función de sus deseos, creencias, gustos e intereses;
· Estrategias para llevar a la práctica la atención centrada en la persona;
· Formar y sensibilizar al personal en el modelo de atención centrada en la persona. Implica un cambio de mentalidad y enfoque;
· Introducir los cambios con el personal que se ofrezca como voluntario, para evitar resistencias iniciales;
· Evaluar la situación actual y definir hasta dónde quieren llegar y posteriormente analizar ¿Qué hacer para llegar hasta ahí?;
· Asignar un profesional de referencia, que será el encargado de facilitar que el paciente logre su mayor autonomía física y moral/espiritual;
· Elaborar una historia de vida del paciente, de preferencia sea el profesional de referencia junto con el paciente; y
· Elaborar fichas relacionadas con los intereses, preferencias y deseos del paciente, debe contener detalles sobre en qué les gustaría invertir su tiempo, en qué actividades desea participar, en lo posible, etc.
Diferencia entre la atención médica tradicional, el enfoque de los programas contra las enfermedades y la atención centrada en la persona. Fuente: Martínez, 2015*. (15)
| Atención médica de carácter convencional | Programas contra enfermedades | Atención centrada en la persona |
| Se centra en la enfermedad y las acciones están dirigidas a la curación. | Se orientan en las enfermedades. | Se orientan en las necesidades de salud. |
| Las relaciones entre el profesional y el paciente se limitan al momento de la consulta. | Las relaciones entre los profesionales y el paciente se restringen al momento de la actuación. | Las relaciones son prolongadas. |
| La atención es exclusivamente curativa. | La atención se centra en luchar contra las enfermedades. | La atención es integral, continua y se centra en la persona. |
| Responsabilidad exclusivamente de asesoramiento al paciente en el momento de la consulta. | Responsabilidad sobre los objetivos de lucha contra las enfermedades. | Responsabilidad sobre la salud a lo largo del ciclo vital. |
| Los pacientes son consumidores de la atención que reciben. | Los grupos de poblaciones son los destinatarios de las intervenciones de luchas contra las enfermedades. | Las personas son asociados en la gestión de su salud y la de su comunidad. |
| Tabla 6.11. Diferencia entre la atención médica tradicional, el enfoque de los programas contra las enfermedades y la atención centrada en la persona. | ||
Necesidades espirituales del niño. C. Jomain (1987), define en 1984 las necesidades espirituales en un sentido amplio: se trata de necesidades de las personas creyentes o no, a la búsqueda de la nutrición del espíritu, de una verdad esencial, de una esperanza, del sentido de la vida y de la muerte, o también deseando transmitir un mensaje al final de la vida. (18)
Las necesidades espirituales son aquellos aspectos del ser humano relacionados con la dimensión más trascendental, no siempre se expresan y vivencian a través de la religiosidad. El satisfacer estas necesidades se traduce en lograr paz interior, aceptar el morir dando sentido a la vida, reconciliándose consigo mismo, los demás y aquello en lo que uno cree. (19) Las necesidades espirituales son inherentes al ser humano, emergen del interior de la persona y se manifiestan de manera transversal en cada cultura. (20)
Existe una concepción equivocada entre lo que es la espiritualidad y lo que es religión. El aspecto espiritual incluye la esencia del ser humano, la esperanza, la autoestima, el significado de la vida, las metas, las ilusiones y la interrelación con otros, en una palabra, espiritualidad corresponde a la "dignidad del ser humano. No debemos olvidar que los niños son espirituales. La conexión espiritual con el medio que los rodea
permitirá dar a estos pacientes un significado mayor a sus vidas. Los niños en etapa terminal tienen creencias espirituales muy profundas, las cuales emergen aún más al momento en que nos cuestionan sobre la vida y la muerte. La búsqueda del significado y el entendimiento del proceso están en relación directa con la edad, la relación familiar y/o emocional que se tiene con el paciente, por lo que es indispensable conocer las diferentes necesidades y percepciones, de acuerdo con el lugar que cada uno ocupa en el proceso. (21)
Los eventos que acontecen durante el proceso de muerte son definidos como "la transformación espiritual a través de la disolución gradual del ego y lo que rodea al individuo llevándolo a su parte más básica", en los niños existe una habilidad natural de llevar a cabo esta transición, ya que están mucho más conscientes de su condición elemental, además de que tienen un menor desarrollo del ego. Durante el proceso de muerte, los niños se transforman en los "maestros de vida" poniendo ante nuestros ojos las riquezas que dan las experiencias humanas, nos dan enseñanzas de humildad que nos muestran la belleza de la esencia de la vida. (21)
Concepto de espiritualidad en menores de edad. (21)
| Edad | Características | Concepto de espiritualidad | Desarrollo espiritual | Intervenciones |
| 0-2 años | Relación sensorial y motora con el medio ambiente. Limitación en la comunicación verbal, alcanza objeto de permanencia, puede percibir "que algo anda mal." | Tiene limitantes en la comunicación y lenguaje por su corta edad, su "espiritualidad" se manifiesta en la necesidad de sentirse amado y protegido, sintiendo confort al satisfacer sus necesidades básicas. | La fe se refleja en confianza y esperanza en los otros, necesitamos sentido de autoestima y amor. | Proporcionar el mayor confort físico al niño, a los familiares y a los objetos transicionales (juguetes favoritos) en forma constante. |
| 2-6 años | Pensamiento mágico, egocentrismo, el pensamiento es irreversible, juego simbólico, desarrollo de las habilidades en la comunicación verbal. | Empieza a formar habilidades de comunicación y un pensamiento mágico y egocentrista. Sí los padres practican algún culto y realizan rituales el niño los va incorporando a su vida, pero aún no tiene clara percepción de pensamiento subjetivo su aprendizaje es por imitación y conceptos básicos. | La fe mágica e imaginativa, participación en rituales, es importante necesidad de valor. | Minimizar la separación de los padres, corregir las percepciones de enfermedad como castigo. Evaluar el sentido de culpa y modificarlo si es que está presente, usar términos precisos (morir y muerte). |
| 6-12 años | Pensamientos concretos. | Ya tiene pensamientos concretos y puede tener dentro de una espiritualidad religiosa conceptos más claros para el bien y el mal, de dios, pecado "hacer el bien", conecta identidad ritual y personal. | Preocupaciones de fe para el bien y el mal, puede aceptar interpretaciones extremas de la verdad. | Evalúa el miedo a ser abandonado, ser honesto, proporcionar detalles concretos si son preguntados. Apoyar los esfuerzos del niño para alcanzar el control y dominio, mantener el contacto con padres. Permitir al niño participar en la toma de decisiones. |
| 12-18 años | Pensamiento generalizado, la realidad se vuelve un objetivo. Capacidad de reflexión, imagen corporal, autoestima. | Tiene capacidad de reflexión, de autoestima, se hace preguntas existenciales, evolución de la relación con un ser supremo dentro de espiritualidad religiosa, y busca el significado y propósitos del valor de la vida. Empieza a buscar conscientemente un sentido de vida. | Comienza a aceptar la interpretación interna de la verdad. Evolución de la relación con Dios o un ser supremo. Busca el significado de propósitos y valor de la vida. | Reformar la autoestima del niño, permitir al niño expresar sus sentimientos más profundos. Permitir la privacidad, promover su independencia, promover contactos con sus padres. Permitir al niño participar en la toma de decisiones. |
Tabla 6.12
6.3 DUELO
Cuando un paciente pediátrico y su familia se enfrentan a una enfermedad crónica compleja, progresiva y que amenaza su vida se presentan procesos de duelo durante las diferentes etapas de la enfermedad causando:
· Dolor y sufrimiento.
· Reacciones abrumadoras y desconcertantes. (22)
Estos procesos de duelo comienzan como ajuste al diagnóstico y tratamiento. El apoyo al duelo es un componente esencial en los cuidados paliativos pediátricos, sin embargo, por lo general no se cuenta con los recursos suficientes, no se ha investigado lo suficiente y no se aplica de manera sistemática, siendo que debe brindarse un apoyo multifacético, interdisciplinario y holístico enfocado a las nuevas realidades, cambios y pérdidas que el paciente, su familia y el equipo médico pueden experimentar. (23)
Definición de duelo. El duelo (del latín dolium, dolor, aflicción) (24) es la angustia experimentada después de una pérdida significativa, generalmente la muerte de una persona amada. El duelo a menudo se distingue de la pérdida y el luto. No todas las pérdidas resultan en una fuerte respuesta de dolor, y no todo el dolor se expresa públicamente. (25)
El duelo a menudo incluye:

Diagrama 3.
Cuando se experimenta dolor intenso en el proceso de duelo se puede convertir en una amenaza para la vida a través de la alteración del sistema inmunológico, el auto descuido y los pensamientos suicidas. El duelo también puede tomar la forma de arrepentimiento por algo perdido, remordimiento por algo hecho o dolor por un percance en uno mismo. (25) El duelo es una reacción natural y subjetiva con una intensidad y duración proporcionales a la dimensión y significado de la pérdida. Es un momento de crisis, es decir, un período crucial o momento decisivo en la vida de una persona que se transforma, frecuentemente, es un acontecimiento vital estresante frente al que carecemos de recursos para afrontar. Pero el duelo no es una enfermedad, sino un proceso doloroso, a veces esperado y otras no. (26)
Manifestaciones del duelo en el adulto
· El duelo NO es un trastorno psiquiátrico, sino una reacción emocional y conductual normal a la pérdida y las reacciones variarán para cada individuo; (27)
· Durante el proceso de duelo se pueden presentar manifestaciones cognoscitivas, afectivas, fisiológicas que se consideran normales; (28)
· Es importante conocer las manifestaciones normales en el proceso de duelo, sabiendo que su intensidad y las alteraciones que provoca en el doliente van a depender de varios factores: la relación emocional y de dependencia con el ser o situación perdido, las circunstancias de la muerte, el tiempo de preparación para la pérdida, etc.; y (29)
· Resulta relevante conocer los recursos de los que disponen los supervivientes y las estrategias de afrontamiento, tanto en el ámbito personal como familiar y social, así como las reacciones de respuesta en situaciones emocionales intensas previas en la experiencia del doliente. (30)
| Manifestaciones normales del duelo en adultos. (Adaptado de Monografía de atención al duelo en Cuidados Paliativos, SECPAL 2014). | |
| COGNOSCITIVAS | AFECTIVAS |
| · Incredulidad/Irrealidad. · Confusión. · Alucinaciones visuales y/o auditivas fugaces y breves. · Dificultades de atención, concentración y memoria. · Preocupación, rumiación, pensamientos e imágenes recurrentes. · Obsesión por recuperar la pérdida o evitar recuerdos. · Distorsiones cognoscitivas · Revisión de aspectos religiosos. | · Impotencia/Indefensión. · Insensibilidad. · Anhelo. · Tristeza, apatía, abatimiento, angustia, ansiedad, hostilidad. · Ira, frustración y enfado. · Culpa y autorreproche. · Soledad, abandono, · emancipación y/o alivio. · Extrañeza con respecto a sí mismo o ante el mundo habitual. |
| FISIOLÓGICAS | CONDUCTUALES |
| · Aumento de la morbimortalidad. · Vacío en el estómago y/o boca seca. · Opresión tórax/garganta, falta de aire y/o palpitaciones. · Dolor de cabeza. · Falta de energía/debilidad. · Alteraciones del sueño y/o la alimentación. | · Conducta distraída. · Aislamiento social. · Llorar y/o suspirar. · Llevar o atesorar objetos. · Visitar lugares que frecuentaba el fallecido. · Llamar y/o hablar del difunto o con él. · Hiperactividad-hipoactividad. · Descontrol u olvidos en las actividades de la vida diaria. |
Tabla 6.13.
Duración del duelo. La duración del duelo es muy variable dependiendo de cada persona y situación. En la bibliografía clásica se apunta como duración 1 año. Sin embargo, en estudios más recientes parece haber consenso en la idea de que después de una pérdida importante, el doliente comienza a recuperarse a lo largo del segundo año después de la perdida. Independientemente del tiempo transcurrido desde la muerte, podremos considerar que el duelo ha terminado cuando el doliente tiene la capacidad de recordar y hablar de la persona fallecida sin dolor, y cuando recobra la capacidad para establecer nuevas relaciones y aceptar los retos de su vida (29)
Tareas del duelo. El duelo, al ser un proceso universal e inevitable, ha sido objeto de estudio por diversos autores y muchos han intentado establecer sus diferentes tareas.
| ENFOQUE BASADO EN LAS TAREAS DEL DUELO. (30) | ||
| TAREAS DEL DUELO | WORDEN (2004-2013) | NEIMEYER (2007, 2012) |
| 1. Aceptar la realidad. 2. Trabajar las emociones y experimentar el dolor. 3. Adaptarse al entorno sin el ser querido. (Adaptaciones externas, internas y espirituales) 4. Recolocar y recordar al ser querido | 1. Reconocer la realidad de la pérdida 2. Abrirse al dolor. 3. Revisar nuestro mundo de significados. 4. Reconstruir la relación con lo que se ha perdido 5. Reinventarnos a nosotros mismos. | |
Tabla 6.14
Modelo de procesamiento dual del duelo
· El modelo de procesamiento dual del duelo integra una taxonomía que describe las maneras en que la gente llega a un "acuerdo" con la pérdida del ser querido, y explica como los dolientes están orientando constante y alternadamente su atención hacia la pérdida o hacia la restauración;
· Cuando su orientación es hacia la pérdida los dolientes trabajan su duelo, expresan sus emociones, interpretan, le dan significado a dicha experiencia y a la vida posterior a la pérdida;
· Cuando su orientación es hacia la restauración, el individuo se distrae de esas experiencias de duelo, focalizando la atención en la reorganización de su vida de manera que busca activamente nuevas actividades, roles y relaciones interpersonales;
· Este modelo de procesamiento dual del duelo ayuda a comprender el funcionamiento del duelo en la vida cotidiana del individuo. Se está oscilando constantemente, entre el sentir y recordar hechos específicos de la pérdida o, enfocándose en situaciones inherentes de la vida como; buscando actividades y relaciones nuevas para contrarrestar las sensaciones de anhelo y vacío que dejó la pérdida del nuestro ser querido o evitar el dolor; y
· Cada individuo puede focalizar su atención alternadamente entre la pérdida o la restauración, la forma en que le dé significado a cualquiera de los dos procesos influirá en la funcionalidad del sujeto o en la posible aparición de duelo complicado. (32)
Diagrama 4
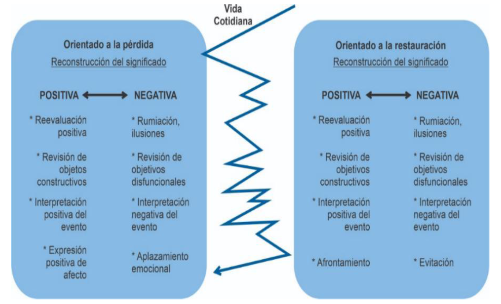
Mediadores del duelo. Existen factores que influyen en el proceso de duelo, estos se llaman mediadores del duelo. Es importante tener en cuenta estos factores, ya que la combinación de éstos podría hacer que se incremente la probabilidad de duelo complicado, ya que pueden afectar la naturaleza, la intensidad y la duración del proceso normal de duelo, éstos se presentan a continuación: (28)
| Mediadores del duelo | |
| Quién era la persona, objeto o situación significativa | La relación que tuvo una persona en duelo con la persona que murió, el objeto o situación que perdió. |
| La naturaleza del apego | · La fuerza del apego: (la intensidad del vínculo). · La seguridad del apego. · La ambivalencia en la relación. · Los conflictos con el fallecido, objeto o situación significativa. |
| Tipo de muerte | · Como murió la persona. · Las muertes se catalogan bajo las categorías NASH: natural, accidental, suicidio y homicidio. · Dónde se produjo la muerte a nivel geográfico · Si había algún aviso previo o se trata de una muerte inesperada. |
| Antecedentes históricos | · Si ha tenido pérdidas anteriores y cómo se elaboraron dichos duelos. · La historia de salud mental previa de la persona. |
| Variables de personalidad | · Edad. · Sexo. · Inhibición de sentimientos. · Cómo maneja la ansiedad y cómo afronta las situaciones estresantes. |
| Variables sociales | · Conocer los antecedentes sociales, étnicos y religiosos del superviviente. · El grado de apoyo emocional y social percibido que se recibe de los demás, tanto dentro como fuera de la familia. |
| Otros tipos de estrés simultáneos | · Cambios simultáneos y crisis que surgen después de la muerte, incluyendo graves cambios económicos. |
| Tabla 6.15 Mediadores del duelo | |
Tipos de duelo:
1. Duelo retardado, inhibido o negado. Se presenta en algunas personas en momentos iniciales, cuando parece mantener el control de la situación sin mostrar sufrimiento. El doliente no acepta la realidad de la pérdida;
2. Duelo complicado o trastorno por duelo prolongado. En muchas ocasiones es difícil de distinguir de la depresión, el trastorno de estrés postraumático o ansiedad, que a veces están asociados con el duelo, por lo que su definición es muy discutida. Denominado actualmente "trastorno por duelo complicado" y se diagnostica con los criterios de DSM 5; y
3. Duelo anticipado. (28) Proceso de desapego emocional que se da antes de la muerte del ser querido. Puede favorecer:
· El reconocimiento de la realidad de la pérdida de forma gradual;
· La resolución de asuntos inconclusos con su ser querido que va a morir;
· Ayudar a cambiar algunos aspectos sobre sí mismos y la vida;
· Estar preparado para la pérdida y comenzar una planificación del futuro; y
· Este duelo no disminuye el dolor posterior. Ayuda a prepararse para la pérdida e impide que se desborden en gran medida los recursos personales del doliente. En principio es de gran ayuda, aunque en algunas situaciones puede suponer el abandono del enfermo.
Aspectos importantes:
· Depresión o sintomatología depresiva;
· Experiencia del fallecimiento de forma anticipada o ensayo mental del mismo;
· Preocupación exagerada por la persona que se está muriendo; y
· Anticipación y reajuste de las consecuencias del fallecimiento.
Duelo complicado. Es aquel en el cual "la persona está desbordada, recurre a conductas desadaptativas, o permanece en este estado sin avanzar en el proceso del duelo hacia su resolución".
Las personas que tienen un mayor riesgo de sufrir un duelo complicado son quienes:
· Experimentan una pérdida repentina o en circunstancias catastróficas;
· Están aisladas socialmente;
· Se sienten responsables de la muerte y aquellas personas que mantenían una relación de intensa ambivalencia o dependencia del fallecido;
· Después de la pérdida son más intensos y persistentes los síntomas de angustia que experimentan;
· Las personas en duelo requieren una mayor demanda de servicios;
· Médicos y hospitalizaciones frecuentes que las personas con pérdidas similares cuyo duelo es menos intenso y de menor duración. Se ha observado que estos efectos duran entre 4 y 9 años después de la muerte.;
· Factores para considerar para atención profesional en duelo;
· Siempre que el doliente pida ayuda expresa para su proceso;
· Si el profesional valora que la ayuda es necesaria; y
· La concomitancia de factores de riesgo de duelo patológico sin la presencia de factores protectores. (29)
Criterios de duelo complicado del DSM-5: Este trastorno se encuentra clasificado en el Manual Diagnóstico y Estadístico de Trastornos Mentales (DSM-5, 2013), dentro de los Trastornos de Trauma y Estresores. (Valorar como duelo complejo persistente: A+B+C+D+E) (29)
Criterio A: El individuo ha experimentado la muerte de un familiar o amigo cercano hace al menos 12 meses;
Criterio B: Durante el fallecimiento ha experimentado por lo menos 1 de los siguientes síntomas, diariamente o en grado intenso o perturbador:
· Anhelo/añoranza persistente del fallecimiento. En niños pequeños la añoranza puede presentarse mediante el juego y el comportamiento;
· Pena y malestar emocional intensos en respuesta a la muerte;
· Preocupación en relación con el fallecido;
· Preocupación acerca de las circunstancias de la muerte; y
Criterio C: Desde el fallecimiento ha presentado por lo menos 6 de los siguientes síntomas diariamente o en un grado intenso o perturbador:
· Deseos de morir para estar con el fallecido;
· Dificultad para confiar en otras personas desde el fallecimiento;
· Sentimientos de soledad o desapego de otras personas desde la muerte;
· Sentir que la vida no tiene sentido o está vacía sin el fallecido.
· Confusión acerca de su papel en la vida, o disminución de la identidad propia; y
· Dificultad a mantener intereses o hacer planes futuros desde la pérdida.
Criterio D: La alteración provoca malestar clínicamente significativo, o deterioro en las áreas social, ocupacional o de otro tipo de funcionamiento;
Criterio E: La reacción de duelo debe ser desproporcionada o no acorde con las normas culturales, religiosas, o adecuadas a la edad del doliente.
| Factores protectores | ||
| Estrategias de afrontamiento | Deducidos de factores de riesgo | Otros factores protectores |
| Estrategias de afrontamiento dirigidas al problema. Estrategias de afrontamiento dirigidas a las emociones. | Apoyo familiar. Ocupación laboral. Sentimiento de utilidad. Conocimiento del pronóstico de enfermedad ajustado a realidad. Ausencia de problemas económicos. | Fluidez comunicativa. Percepción de autoeficacia. Sentimiento de utilidad en el cuidado del enfermo. Habilidad para la planificación y resolución de problemas. Flexibilidad mental. Autocuidado. Capacidad para encontrar sentido a la experiencia significativas a edad temprana. Reacción emocional intensa en el momento de la muerte. |
Tabla 6.16
| Factores de riesgo | ||
| Factores circunstanciales de la muerte | Factores personales | Factores interpersonales |
| Muerte inesperada. Muerte violenta. Estresores psicosociales concurrentes. Muerte estigmatizada. Sintomatología no controlada. | Edad. Género. Personalidad. Antecedentes psicopatológicos. Pérdidas significativas a edad temprana. Reacción emocional intensa en el momento de la muerte. | Vinculo de dependencia. Relación ambivalente. Percepción de escaso apoyo psicosocial. |
Tabla 6.17
Niveles de intervención para el duelo.
Nivel I. Información, apoyo y acompañamiento, por el equipo: médicos, enfermeras, psicólogos, trabajadores sociales, administrativos. Dependiendo de las funciones, formación y vínculo con el paciente y su familia, estableciendo durante el proceso asistencial.
Nivel II. Asesoramiento por el equipo: médicos, enfermeras, psicólogos, trabajadores sociales.
Nivel III. Intervención especializada. Dirigida a dolientes de alto riesgo, duelo complicado, trastornos relacionados con el duelo, realizada por profesionales especializados (Psicólogos y Psiquiatras. (29)
Intervención en duelo. La atención al duelo debe abarcar los tres periodos relevantes en torno al momento de la pérdida: antes del fallecimiento, durante el proceso de agonía y después del fallecimiento. La valoración de predictores de riesgo y factores protectores nos permitirán identificar aquellos dolientes que probablemente necesitarán más apoyo en su proceso de duelo. (29)
Antes del fallecimiento: (29)
· El objetivo específico de esta fase será cuidar y ayudar a despedirse al enfermo, familia y/o personas allegadas y significativas.
Paciente
· Garantizarle atención integral;
· Control adecuado de síntomas repercute a nivel psicológico para la elaboración del duelo;
· Detectar, valorar y resolver necesidades y conflictos psicosociales y espirituales;
· Favorecer la expresión emocional. Prevenir o aliviar sentimientos de culpa;
· Promover resolución de temas pendientes.
· Identificar factores de riesgo psicológico o psiquiátrico t derivar para valoración e intervención.
· Valorar información de la que dispone el paciente respecto al diagnóstico y pronóstico.
· Comunicación al paciente respecto a lo que sabe, lo que quiere saber, y lo que puede saber, adecuado a su edad.
Familia
· Garantizar la atención integral y constante a la familia durante el proceso de enfermedad;
· Informar y comunicar con calidez y claridad sobre el diagnóstico y pronóstico, así como los cambios y planes que se pueden prever y/o presentar;
· Mediar en situación de conflicto;
· Orientar sobre necesidades de organización y dinámica familiar;
· Promover pautas de participación y actuación de todos los integrantes de la familia;
· Reforzar su capacidad de cuidar a su ser querido, y dar soporte en aprendizaje de dichos cuidados;
· Establecer con su paciente una comunicación clara y congruente a las necesidades de ambos.
· Promover la movilización de recursos internos y externos (sociales y de salud).
Equipo de salud
· Planificación de los cuidados con las necesidades del paciente y la familia para establecer normas de actuación y prevención de riesgo de claudicación familiar;
· Identificar la relación del paciente con sus familiares para favorecer la comunicación y poder lograr una triada terapéutica de confianza; y
· Valorar y potenciar recursos, soporte emocional y físico percibido.
Intervención específica recomendada durante la fase de últimos días. (29) Paciente:
· Evaluación y control constante de síntomas. Aliviar el sufrimiento;
· Favorecer la expresión emocional y la comunicación, normalizando pensamientos y validando emociones;
· Facilitar los ritos religiosos o espirituales que ayuden a esta situación; y
· Permitir visitas o facilitar los medios para despedida de los seres amados.
Después del fallecimiento Intervención específica recomendada. (29)
Familia.
En hospital:
· Facilitar la mayor privacidad posible. Acompañar hasta que lleguen otros familiares; y
· Posibilitar despedida del fallecido y colaboración en cuidado post mortem, si es su deseo.
Durante el duelo:
· Facilitar la comprensión de la realidad de la pérdida. Clarificar dudas del fallecimiento;
· Validar sentimientos y permitir expresión emocional, acompañar a la familia transmitiendo tranquilidad;
· Revisar, reforzar y reconocer los cuidados ofrecidos por la familia, personas allegadas y cuidadores, al enfermo, de la forma más objetiva posible, resaltando los aspectos más positivos;
· Facilitar la solución de problemas concretos, como, por ejemplo, el certificado de defunción;
· Explorar si existe sentimiento de culpa;
· Reorientar posibles creencias que puedan dificultar la expresión de sentimientos, por ejemplo, "mejor no recordar para no sufrir y olvidar";
· Informar sobre la evolución del duelo normal y sus fases;
· Informar de programas específicos de atención en duelo;
· Animar a retomar el cuidado de su salud, así como ir recuperando poco a poco sus actividades rutinarias diarias y sus relaciones sociales; e
· Identificar a quienes presenten riesgo de duelo complicado o trastornos relacionados con la pérdida, para canalizarlos al servicio de salud correspondiente.
Equipo de salud.
· Aprender técnicas de despedida para el manejo de pérdidas de forma personal y profesional;
· Promover despedirse de los padres y mostrar disponibilidad en caso de que se necesite algo del equipo de cuidados paliativos que ha atendido al paciente fallecido, posteriormente; y
· Ofrecer reuniones de todo el equipo, en las que se expresen emociones, sentimientos y experiencias relacionadas con el acompañamiento brindado al paciente y su fallecimiento, para minimizar riesgos de burnout.
Instrumentos de evaluación. DSM-5. Para evaluar trastornos asociados a la pérdida y duelo complejo persistente. (34)
Duelo en niños y adolescentes ante la pérdida de ser querido. Los niños, como los adultos, sufren con las pérdidas, hablar sobre la muerte, la enfermedad y el dolor es esencial. Poder llorar la muerte de un ser querido y afrontarla antes de que se produzca, en el momento en que ocurre y después. El concepto de la muerte es abstracto y complejo, de ahí que la forma de abordarlo y comprenderlo dependa de aspectos como la edad y el nivel de desarrollo evolutivo del niño y adolescente (Tabla 6.18). (29) (35)
| ETAPAS DE DESARROLLO | CONCEPTO DE MUERTE |
| Etapa prelingüística (0 a 3 años) | Son sensibles a cualquier cambio que ocurre en su entorno, sobre todo en la separación de cuidadores significativos. No comprende el concepto de muerte. |
| Etapa preescolar (3 a 5 años) | Vive en el momento presente. Negación de la muerte como un acontecimiento final (irreversible). La familia es el centro de su mundo emocional. El pensamiento mágico se impone, (cuidado con la culpa) |
| Etapa escolar (6 a 8 años) | Comienzan a percibir la muerte como algo irreversible y universal. Sienten miedo. Se cuestionan la seguridad de la vida. ¿Tú también te vas a morir? Curiosidad e interés por las reacciones de su cuerpo y sobre a muerte. |
| Etapa escolar (9 a 12 años) | Concepción adulta del concepto de muerte. La perciben como muy lejana. Mayor dificultad para la comunicación, pero más necesidad de información. |
| Etapa adolescente (13 a 18 años) | Saben que la muerte es universal, inevitable e irreversible. Se cuestionan el significado de la vida. Necesitan ser escuchados. Reacciones emocionales intensas y dificultades en la expresión emocional. Negación y actitud evitativa frecuentemente. |
Tabla 6.18. Concepto de muerte en las diferentes etapas de desarrollo del menor.
Los padres, madres o responsables deben prestar atención a las respuestas normales a la muerte, así como a las señales de que un niño puede necesitar ayuda profesional. Es común que la niñez sienta una amplia gama de emociones en respuesta al fallecimiento de un ser querido, como impresión, tristeza, ansiedad o enojo. La manera de expresar estos sentimientos depende de su edad y desarrollo. En los diversos niveles de desarrollo, la niñez tiene una idea diferente de la irrevocabilidad de la muerte. (36)
Su enfoque para hablar de la muerte dependerá del nivel de comprensión que tenga cada niño de 4 conceptos principales de la muerte:
1. Irreversibilidad: La muerte es permanente;
2. Irrevocabilidad: Todo funcionamiento se detiene con la muerte;
3. Inevitabilidad: La muerte es universal para todos los seres vivos; y.
4. Causalidad: Las causas de la muerte.
La falta de comprensión de estas ideas por parte de la niñez afecta su capacidad para procesar lo ocurrido y afrontar sus sentimientos (36).
El concepto de la muerte en las diferentes etapas de desarrollo. (35) Las reacciones normales del duelo (29) en niños y adolescentes incluyen:
· Impresión e incredulidad;
· Recuerdos;
· Sueños;
· Lágrimas;
· Miedo después de la muerte de uno de los padres;
· Enojo; y
· Tristeza.
Indicación duelo complicado en niños y adolescentes. (29) Algunas de las reacciones más habituales según edad de los niños, que pueden indicar la existencia de un proceso de duelo que requiere ayuda, y que se mantienen por más de 6 meses después del fallecimiento del familiar, son:
Hasta los 7 años. Cambios en los juegos. Rotura de juguetes, nerviosismo, llamadas de atención constantes. Regresiones: aparecen conductas que ya había superado, más infantiles, como hacerse pipí de nuevo en la cama. Indiferencia: actúan como si no hubiera pasado nada.
Hasta los 12 años. Cambios en los juegos. Rotura de juguetes, nerviosismo, llamadas de atención constantes. Regresiones: aparecen conductas que ya había superado, más infantiles, como hacerse pipí de nuevo en la cama. Indiferencia: actúan como si no hubiera pasado nada
Adolescencia. Indiferencia ante lo sucedido. Aislamiento social o familiar. Rebeldía
Predictores de riesgo en niños y adolescentes (29):
· Ambiente inestable por no haber un familiar responsable de los cuidados y realizar esta tarea distintas personas;
· Dependencia con el progenitor superviviente y forma inadecuada de reaccionar este ante la pérdida;
· Segundas nupcias con una persona con la que existe una relación negativa;
· Pérdida de la madre para niñas de menores de 11 años y del padre en varones adolescentes;
· Falta de consistencia en la disciplina impuesta al niño o al adolescente;
· Indicadores de dificultad de afrontamiento en niños y adolescentes antes del fallecimiento del familiar; (29)
· Los niños también muestran sintomatología concordante con estar afrontando la pérdida. La siguiente sintomatología es indicadora de dificultad siempre que ésta se mantenga trascurridos más de 6 meses tras el fallecimiento.;
· Regresión a etapa anterior: Volver a orinarse, rabietas, volver a dormir con los padres;
· Cambios emocionales: mayor tristeza, irritabilidad, miedo a ser abandonado, pesadillas, oposicionismo, culpa;
· Tiene menos apetito, come con ansiedad; y
· Problemas en el rendimiento académico, aislamiento.
Importante en esta etapa: (29).
· Mantener la rutina del niño;
· Explicar lo que está pasando, adaptado a su edad;
· Mantener normas, dedicarles un espacio de expresión de emociones, de preocupaciones;
· Darles seguridad, que vamos a estar para cuidarles, dedicarles un tiempo especial;
· Observar cualquier cambio en el niño que nos sea significativo;
· Evaluar si está siendo atendido por psicólogo, psiquiatra; y
· Responder a las preocupaciones relacionadas con la muerte.
Los niños de distintas edades plantean diferentes preguntas sobre la muerte, cuanto más mayor más capacidad para entender. Si el padre/madre no se ve capaz, que busque a alguien que escuche y pueda dar respuesta a los niños y sus preocupaciones sobre la muerte y qué es lo que pasa después. El niño necesita tiempo y atención. Aunque delegue, procure estar presente. (29)
· Con los niños utilizar dibujos, muñecas o libros;
· Es probable que deseen dibujar sus sentimientos. Las preguntas pueden surgir mientras se le pregunta que es lo que dibuja, porqué elije determinados colores;
· Estar preparado para algunas duras preguntas sobre la vida y sobre después de la muerte;
· Estar preparado para duras preguntas acerca de lo que le sucede al cuerpo tras la muerte;
· Responder a todas las preguntas de forma simple y concreta, incluso con un "no lo sé";
· Recordar a los niños que no es culpa nuestra que una persona muera. Es una idea frecuente y es bueno hablarlo para evitar creencias erróneas;
· Es importante compartir la decisión sobre quién debe ir al funeral y al entierro;
· Preguntar quién quiere ir al funeral;
· Preguntar a los niños antes del funeral que sienten ante lo que está pasando.
· Permitir que cambien de opinión;
· Contar con ellos en las reuniones y comidas después del funeral;
· Posibilidad de desacuerdo con permitir la asistencia de los niños a los funerales;
· Asignar a alguien la supervisión de los niños durante el funeral;
· Permitir que el niño visite la iglesia o el lugar o el lugar donde se va a celebrar el funeral;
· Estar atentos a lo que los otras personas explican que pueda confundirlos; y
· Decirles que es correcto si no saben lo que sienten.
Instrumento para la evaluación del duelo en niños y adolescentes. DSM-5. Para evaluar trastornos asociados a la pérdida y duelo complejo persistente. (34)
Duelo en padres. En el caso del fallecimiento de un hijo nos encontramos ante un hecho que va contra natura. Estos procesos son muy difíciles de afrontar para el doliente y es importante trabajar en la prevención y en la identificación de factores de riesgo, hacer una valoración y soporte en caso de que sea necesario durante el proceso de duelo, para prevenir su complicación. (29)
Objetivos del protocolo de actuación en el duelo para equipos específicos de cuidados paliativos
· Ofrecer a los dolientes cuidados básicos y apoyo emocional;
· Detectar los factores de riesgo de duelo complicado y recomendar atención cuando proceda;
· Aportar tratamiento sintomático urgente si fuera preciso;
· Preparar a la familia para el momento del fallecimiento;
· Facilitar a los parientes la información necesaria para realizar los trámites administrativos y legales derivados del fallecimiento, como certificados de defunción, listado de tanatorios y funerarias, etc.;
· Habilitar entre los profesionales la información pertinente para proporcionar atención adecuada a las familias en los días previos al fallecimiento y durante el duelo, así como para la certificación del fallecimiento producido en el domicilio;
· En la atención del proceso del duelo, requiere una evaluación individualizada, prestando especial atención a la existencia de factores de riesgo que hicieran necesario un abordaje más específico, detectando y previniendo el duelo complicado (29). Las manifestaciones del duelo son más favorables si la persona doliente puede interactuar con los que comprenden o comparten su pérdida;
Las actuaciones de los profesionales irán encaminadas a:
· Control de síntomas;
· Informar a la familia sobre el diagnóstico y pronóstico;
· Comunicar el diagnóstico al enfermo;
· Informar a los familiares sobre las actividades que pueden realizar en el cuidado del enfermo e implicar al mayor número de posible de familiares;
· Estimular la comunicación paciente - familia;
· Preparar a la familia para la fase de agonía;
· Informar a la familia con cierta antelación de la proximidad de la muerte;
· Hay que recomendar que asista al funeral toda la familia;
· Acompañar a los familiares que lo soliciten y pidan ayuda para afrontar la situación de últimos días en el domicilio;
· Intervenir para prevenir la desviación patológica del duelo; en el caso de que hubiera aparecido canalizarla para su abordaje;
· Atender y seguir las situaciones en las que es más frecuente la evolución compleja o prolongada del duelo; y
· Valorar la posible aparición de psicopatología que precise de la ayuda especializada de los equipos de salud mental.
Diagrama de flujo: protocolo de actuación en el duelo. (29)(28)
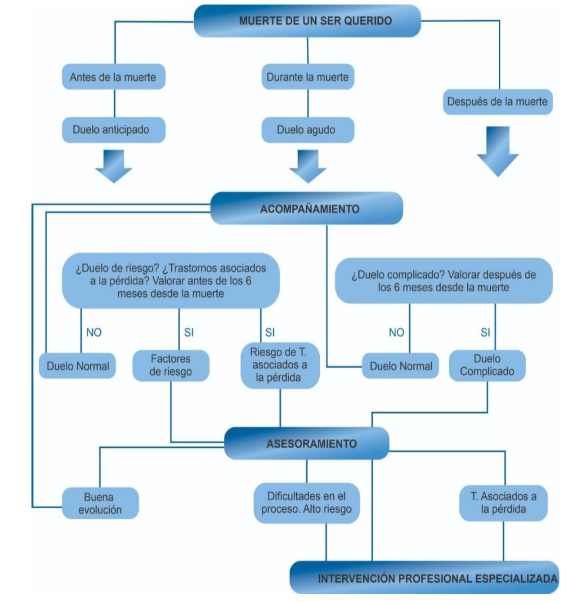
Diagrama 5. Protocolo de actuación en el duelo.
BIBLIOGRAFÍA.
1. Garduño, A. Guía práctica para la atención integral a niños en cuidados paliativos. 2019. Corinter. México. ISBN 978-607-7618-00-0
2. Deena R. Levine, Belinda N. Mandrell, RN, April Sykes, Michele Pritchard, RN, Deborah Gibson, MA, Heather J. Symons, David Wendler, and Justin N. Baker, Patients' and Parents' Needs, Attitudes, and Perceptions About Early Palliative Care Integration in Pediatric Oncology JAMA Oncol. 2017 Sep; 3(9): 1214-1220.Published online 2017 Mar 9. doi: 10.1001/jamaoncol.2017.0368: 10.1001/jamaoncol.2017.0368.
3. Johanna Taylor, Alison Booth, Bryony Beresford, Bob Phillips, Kath Wright, and Lorna Fraser. Specialist pediatric palliative care for children and young people with cancer: A mixed-methods systematic review Palliative Medicine 2020, Vol. 34(6) 731-775
4. Ester Alejandra Rosado Pulido; Cointa Arroyo Jiménez; Arturo Sahagún Morales; Argelia Lara Puente; Sofia Campos Ugalde; Rosalba Ochoa Palacios; Juan José Sánchez Sosa. Necesidad de apoyo psicológico y calidad de vida en el cuidador primario de pacientes pediátricos con cáncer Psicooncología 2021; 18(1): 137-156
5. Mercedes Bernada, Estándares de calidad en cuidados paliativos pediátricos Arch Pediatr Urug 2021; 92(1): e402
6. Vadeboncoeur, C and McHardy, M. Benefits of Early Referral to Pediatric Palliative Care for a Child with a Rare Disease. Pediatrics. 2018; 141(6): e20173417.
7. Meaghann S. Weaver, Katherine E. Heinze, Cynthia J. Bell, Lori Wiener, Amy M. Garee, RN Katherine P. Kelly, Robert L. Casey, Anne Watson, and Pamela S. Hinds, Establishing Psychosocial Palliative Care Standards for Children and Adolescents with Cancer and Their Families: An integrative review Palliat Med. 2016 March; 30(3): 212-223. doi:10.1177/0269216315583446.
8. Sisk BA, Feudtner C, Bluebond-Langner M, et al. Response to Suffering of the Seriously Ill Child: A History of Palliative Care for Children. Pediatrics. 2020;145(1): e20191741.
9. Cruzado Rodríguez J. A., Manual de Psicooncología, Ediciones Pirámides. 2014.
10. Currier, J.M.; Neimeyer, R.A.; Berman, J.S. The effectiveness of psychotherapeutic interventions for dued persons: A comprehensive quantitative review. Psychol. Toro. 2008, 134, 648-661. [CrossRef] [PubMed]
11. Alpízar Rodríguez D, Muñoz Murillo JP. Revisión bibliográfica. Diagnóstico del paciente en situación de últimos días. Med Leg. Costa Rica; 2016; 33 (1)
12. Barbero L. El apoyo espiritual en Cuidados Paliativos, lab hosp 2002, pág 263:5-24.
13. Puchalski C, Ferrell B, Virani R, Otis-Green S, Baird P, Bull J, et al. Improving the Quality of spiritual care as a dimension of palliative care: The report of the consensus conference. J Palliat Med 2009:12:885-90. Doi: 10.1089/jpm.2009.0142. pág. 11 Disponible: file:///C:/Users/maggi/Downloads/Improving%20the%20quality%20of%20sp%20care%20as%20a%20dimension%20of%20palliative.en.es.pdf
14. Enric Benito, Mónica Dones y Javier Barbero, EL ACOMPAÑAMIENTO ESPIRITUAL EN CUIDADOS PALIATIVOS, PSICOONCOLOGÍA. Vol. 13, Núm. 2-3, 2016, pp. 367-384 ISSN: 1696-7240 - DOI: 10.5209/PSIC.54442, Págs. 373-374, 376-377. Disponible: file:///C:/Users/maggi/Downloads/acompa%C3%B1amiento%20espiritual%20en%20el%20cuidado%20paliativo.pdf
15. Enric Benito Javier Barbero Alba Payás, EL ACOMPAÑAMIENTO ESPIRITUAL EN CUIDADOS PALIATIVOS Una introducción y una propuesta, Grupo de Trabajo sobre Espiritualidad en Cuidados Paliativos de la SECPAL, 82008), Págs. 78 Recuperado de: file:///C:/Users/maggi/Downloads/%20GUIA%20ESPIRITUALIDAD%20SECPAL%202008.pdf
16. Juan Aníbal González Rivera, ESPIRITUALIDAD EN LA CLÍNICA. Integrando la Espiritualidad en la Psicoterapia y la Consejería. Ediciones Psicoespiritualidad., Bayamón, Puerto Rico, 2015., Págs. 109, 110 y 112
17. Maitane Alejos Garro, El enfoque de Atención Centrada en la Persona. Plan formativo de sensibilización para los profesionales de referencia, Universidad de Navarra, Pamplona 2016, pág 17 recuperado de https://dadun.unav.edu/bitstream/10171/43684/1/El%20Enfoque%20de%20Atenci%C3%B3n%20Centrada%20en%20la%20Persona.pdf
18. J H Thieffry, Necesidades Espirituales del Enfermo terminal, lab hosp 1992: 24 (225-226) (222-36).
19. Torralba, F. Necesidades Espirituales del ser Humano. Cuestiones preliminares. Lab. Hosp 2004; 36 (271): 7-16
20. Maté J. Necesidades Espirituales en la práctica clínica- Ponencia presentada en el Sexto Congreso de la Sociedad de Catalano-Balear de Cuidados Paliativos, Terrassa, Barcelona, mayo 2007.
21. Chirino Y. Barceló. Cuidados Paliativos en Pediatría, Bol Med Hosp Infant Mex. 2010, México.
22. Friedrichsdorf SJ, Wolfe J, Remke S, Hauser J, Emanuel L (eds). The Education in Palliative and End-of-Life Care for Pediatrics Curriculum. PSI-05 Pérdida y duelo (versión para Latinoamérica). 2010-2015: 1-36.
23. Hudson P, Hall C, Boughey A, Roulston A. Bereavement support standards and bereavement care pathway for quality palliative care. Palliat Support Care. 2018;16(4):375-87.
24. Meza Dávalos EG, García S, Torres Gómez A, Castillo L, Sauri Suárez S, Martínez Silva B. El proceso del duelo. Un mecanismo humano para el manejo de las pérdidas emocionales. Rev Esp Med Quir. 2008;13(1):28-31.
25. Apa. org. [citado el 1 de agosto de 2021]. Disponible en: https://dictionary.apa.org/grief
26. Manual Pérdida y duelo: ante una situación de violación de DDHH [Internet]. Issuu.com. [citado el 1 de agosto de 2021]. Disponible en: https://issuu.com/ddhhcofavic/docs/manual_p_rdida_y_duelo.
27. López de Ayala García C, Galea Martín T, Campos Méndez R. Guía Clínica. Seguimiento del duelo en Cuidados Paliativos. Extremadura, España: Observatorio Regional de Cuidados Paliativos de Extremadura (Junta de Extremadura, Servicio Extremeño de Salud - FundeSalud); 2010.
28. Secpal.com. [citado el 1 de agosto de 2021]. Disponible en: http://www.secpal.com/Documentos/Blog/01_MONOGRAFIA%25205%2520-%2520OK 20140622%2520Para%2520imprenta%2520final%2520final.pdf+&cd=1&hl=es-419&ct=clnk&gl=mx.
29. psimae. Protocolo de Atención al Duelo en la Comunidad de Madrid - 2019 - Psimae [Internet]. Psimae.es. 2019 [citado el 1 de agosto de 2021]. Pág 32 Disponible en: http://psimae.es/protocolo-de-atencion-al-duelo-en-la-comunidad-de-madrid-2019/.
30. Worden JW. Grief counseling and grief therapy, fourth edition: A handbook for the mental health practitioner. 4a ed. Nueva York, NY, Estados Unidos de América: Springer Publishing; 2008
31. Llácer LA, Campos MR, Martín PB, Marín MP. Modelos Psicológicos del Duelo: Una Revisión Teórica. CdVS [Internet]. 2019 [citado el 1 de agosto de 2021];12(1). Disponible en: http://revistacdvs.uflo.edu.ar/index.php/CdVUFLO/article/view/176.
32. Researchgate.net. [citado el 1 de agosto de 2021]. Disponible en: https://www.researchgate.net/profile/Jose-Cruz-Gaitan/publication/329655368_Terapia_Cognitivo_Conductual_en_el_manejo_de_Duelo_Complicado/links/5d2b23f5458515c11c2ede19/Terapia-Cognitivo-Conductual-en-el-manejo-de-Duelo-Complicado.pdf
33. León-Amenero D, Huarcaya-Victoria J. El duelo y cómo dar malas noticias en medicina. An Fac Med (Lima Perú: 1990). 2019;80(1):86-91.
34. DSM 5 Completo [Internet]. Scribd.com. [citado el 1 de agosto de 2021]. Disponible en: https://es.scribd.com/document/432549652/Dsm-5-Completo: 789-92.
35. Fadq.org. [citado el 1 de agosto de 2021]. Disponible en: https://www.fadq.org/wpcontent/uploads/2020/06/02_Guia_Soporte_emocional_Fin_Vida.pdf+&cd=1&hl=es-419&ct=clnk&gl=mx
36. Unicef.org. [cited 2021 Aug 1]. Available from: https://www.unicef.org/elsalvador/media/3191/file/Manual%20sobre%20Duelo.pdf
Bibliografía adicional recomendada.
· Gutiérrez Capulín, Reynaldo; Díaz Otero, Karen Yamile; Román Reyes, Rosa Patricia (2016) El concepto de familia en México: una revisión desde la mirada antropológica y demográfica Ciencia Ergo Sum, vol. 23, núm. 3, Universidad Autónoma del Estado de México, México
· Koumarianou A, Symeonidi AE, Kattamis A, Linardatou K, Chrousos GP, Darviri C (2021). A review of psychosocial interventions targeting families of children with cancer. Palliative and Supportive Care 19, 103-118. https://doi.org/10.1017/S1478951520000449
· María Fregoso Vera, Samuel Jurado Cárdenas y Javier Gómez Vera (2016). Efectos de una intervención de sesión única sobre la ansiedad y depresión en cuidadores primarios informales Psicología y Salud, Vol. 26, Núm. 1: 69-80, enero-junio
· Olimpia Gómez Pérez y Nazira Calleja Bello (2016) Regulación emocional: definición, red nomológica y medición Vol. 8, No. 1, 96-117 ISSN-impresa: 2007-0926; ISSN-digital: 2007-3240 www.revistamexicanadeinestigacionenpsicologia.com
· Galimberti H. (2020) Diccionario de psicología. Editorial Siglo XXI México. https://psicologiaymente.com/psicologia
CAPÍTULO VII
COMUNICACIÓN EN LOS CUIDADOS PALIATIVOS PEDIÁTRICOS
La comunicación eficaz y colaborativa es esencial en los cuidados paliativos para el paciente pediátrico (CPPP) y es una habilidad que debe aprenderse y practicarse, en vía de fortalecer la relación médico-paciente-familia y promover un modelo de toma de decisiones informada y compartida. Cuando se produce una comunicación honesta y bidireccional, se crea confianza y se establecen buenas relaciones. (1)
La comunicación centrada en el paciente favorece la calidad de vida relacionada con la salud, la expresión emocional, la resiliencia, un mayor sentido de realización personal, el control de los síntomas, la adherencia a tratamientos terapéuticos y la satisfacción general de pacientes, sus familias y el equipo de salud. (2)
7. 1 DEFINICIÓN COMUNICACIÓN
Comunicar es hacer partícipe o transmitir a otra persona algo que se tiene: Información, Sentimientos, Pensamientos o Ideas. (3) La comunicación es una herramienta terapéutica esencial que da acceso al principio de autonomía, el consentimiento informado, la confianza mutua, la seguridad y la información que el paciente necesita para ser ayudado y ayudarse a sí mismo. Sus beneficios en el paciente, familia y equipo de salud son: (1,4)
· Coordinar las acciones del plan médico;
· Reducir los niveles de estrés generado en la actividad diaria;
· Reducir los niveles de ansiedad en situaciones que a menudo son traumáticas;
· Ahorrar el tiempo que se puede perder cuando hay malentendidos y conducir a mejor toma de decisiones y resultados;
· Calidad de vida; y
· Accesibilidad a la información de lo que está sucediendo para afrontar la enfermedad de manera más eficaz y adaptarse de manera funcional.
7.2 OBJETIVOS DE LA COMUNICACIÓN
1. Informar;
2. Orientar; y
3. Apoyar. (3)
7.3 ELEMENTOS DE LA COMUNICACIÓN
1. Emisor.
2. Receptor
3. Mensaje.
4. Canal.
5. Respuesta.
6. Código.
7. Referente (Es la realidad que es percibida gracias al mensaje)
8. Situación. (5)
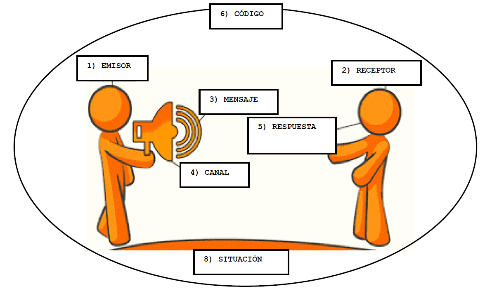
Imagen 1. Elementos de la comunicación.
7.4 CUATRO EJES QUE GUÍAN EL ALCANCE DE LA COMUNICACIÓN DENTRO DE LOS CUIDADOS PALIATIVOS PARA PACIENTES PEDIÁTRICOS (CPP)
1. Enfrentar fortalezas;
2. Proporcionar información adecuada de enfermedad y tratamiento;
3. Dar información sobre el soporte adecuado; y
4. Generar habilidades en el paciente y la familia para manejar su tratamiento y toma de decisiones.
7.5 COMUNICACIÓN COLABORATIVA
La comunicación colaborativa se refiere tanto al intercambio de información como a la naturaleza de la relación de colaboración entre las personas que se comunican, enfatizando las relaciones entre las personas, viendo la comunicación interpersonal y las relaciones como inexorablemente entrelazadas. (4)
Se distingue por el deseo de los participantes de realizar estas tareas: (6)
1. Establecer una meta común o un conjunto de metas que guíen los esfuerzos colaborativos;
2. Mostrar respeto mutuo y compasión por los demás;
3. Desarrollar una comprensión completa de nuestras diferentes perspectivas;
4. Asegurar la máxima claridad y corrección de lo que nos comunicamos y manejar los procesos intrapersonales e interpersonales que afectan; y
5. Tener apertura para recibir y procesar la información.
La comunicación colaborativa se fomenta al reconocer que "la situación" puede diferir desde varios puntos de vista, es decir: (4) Las discusiones honestas y compasivas sobre los objetivos de la atención y las esperanzas para los pacientes pueden brindar comunicación eficaz y las relaciones positivas que fomentan consuelo a las familias que están en duelo por la pérdida de un hijo. (4) "Vale más una verdad amorosa que una mentira piadosa".(7) Desde esta perspectiva:
1. Cada persona crea una representación de la realidad que puede ser diferente a la de otra persona. Esta refleja:
· Temperamento individual;
· Experiencia personal;
· La circunstancia social;
· Herencia cultural; y
· Manejo de conflictos interpersonales;
2. El cómo representamos una situación, hace que nos enfoquemos en ciertos aspectos mientras ignoramos otros, limitando la detección de otras variantes de ésta;
3. Se debe compartir el sentido de lo que está sucediendo y lo que significa para cada uno de los involucrados, para comparar y contrastar nuestras representaciones e identificar por qué nos hemos centrado en una sola forma de enfrentarlo.
7.6 UN ENFOQUE DE EQUIPO INTERDISCIPLINARIO PARA LA COMUNICACIÓN
Para un abordaje holístico de las necesidades físicas, emocionales, sociales y espirituales de los pacientes, como de sus familias, la atención debe brindarse a través de un equipo interdisciplinario que cuente con herramientas de comunicación y entrenamiento en estrategias para la toma de decisiones, el manejo de conflictos, comunicación de malas noticias y reuniones familiares. Para ello, la fórmula está en tener claro las circunstancias clínicas, las partes interesadas en el caso y la información que debe transmitirse al paciente y a la familia. (8)
7.7 MANEJO DE CONFLICTOS
En el curso de la prestación de atención clínica surgen conflictos. Estos conflictos pueden ser entre:
· Padres y médicos;
· Entre miembros de la familia;
· Entre miembros del equipo de salud; y
· Casi cualquier otra combinación de personas que se preocupan por el paciente.
A continuación, se ilustran algunas estrategias útiles para abordar los conflictos y tener conversaciones difíciles más productivas: (4)
Tabla1. Funciones básicas de la comunicación entre el paciente y el equipo de salud (9)
| FUNCIÓN | HERRAMIENTA DE COMUNICACIÓN Y SU OBJETIVO |
| Responder a las emociones | Evaluar y valorar la angustia. Ofrecer validación, empatía y apoyo. |
| Intercambiar información | Identificar la cantidad de la información que el paciente o el cuidador desea recibir. Reconocer la información disponible. Considerar los hallazgos presentados sin parecer despectivo. |
| Tomar decisiones | Asociarse con el paciente y la familia para identificar los objetivos de la atención. Alinear el plan de tratamiento con los objetivos establecidos. |
| Fomentar de relaciones sanadoras | Desarrollar la confianza, la comprensión y el compromiso mutuo. Aclarar los roles y las expectativas del paciente y el equipo de salud. |
| Habilitar la autogestión | Fomentar la participación en todos los aspectos de la atención. Invitar a preguntas de pacientes y familiares. |
| Gestionar la incertidumbre | Reconocer las limitaciones en el conocimiento. Nombrar las incertidumbres y abordar los temores asociados. |
7.8. CONCIENCIA PRONÓSTICA.
La conciencia pronóstica se define como la capacidad del paciente y su familia para comprender su pronóstico y la trayectoria probable de la enfermedad. Los pacientes desarrollan gradualmente la conciencia del pronóstico a través de un proceso cognitivo y emocional que se puede cultivar con el tiempo, mediante la interacción con un médico capacitado. (10)
Después de compartir el diagnóstico, el equipo de salud puede considerar un enfoque longitudinal que ayude al paciente y su familia a planificar y esperar cosas que probablemente pudieran ser posibles dentro del contexto de la enfermedad como: (8)
· Las formas en que la enfermedad puede afectar al niño;
· La probabilidad de curación;
· Las complicaciones esperadas; y
· La información sobre la trayectoria probable de la enfermedad.
· Los médicos deben (9) tener una idea de lo que el paciente ya sabe y es capaz de articular sobre el pronóstico; y comprender que la incapacidad de un paciente y su familia para integrar la información del pronóstico después de una o incluso varias conversaciones, es esperado. El paciente y su familia integran la información del pronóstico a un ritmo que pueden tolerar y que preserva su capacidad para funcionar en el mundo. La imagen 2 y tabla 2, ilustran esta perspectiva.
Imagen 2.
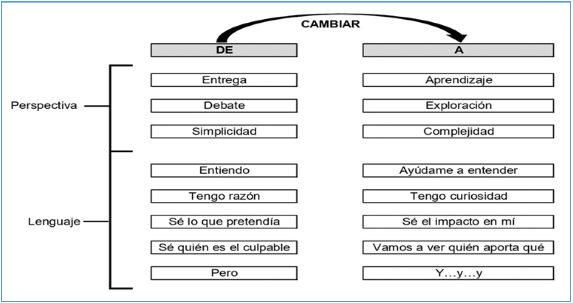
| Tabla 2. Pasos para cultivar la conciencia pronóstica a lo largo del tiempo (10) | |
| Paso 1. Evaluar la comprensión de la enfermedad y el pronóstico · ¿Qué le han dicho sobre la enfermedad/pronóstico de su hijo?; · ¿Cuál es su percepción de lo que depara el futuro?; · ¿Qué tan preocupado está?; y · ¿Qué es lo que más le ha preocupado? | |
| Paso 2. Facilitar el desarrollo de la conciencia pronóstica imaginando una salud más precaria · ¿Alguna vez ha pensado en cómo sería si su hijo se enfermara más?; · Sería bueno pensar en lo que podría suceder si su hijo se enfermara más; · Es bueno estar preparado en caso de que eso suceda. | |
| Paso 3. Evaluar la respuesta y considerar la urgencia de la necesidad de entregar información de pronóstico. | |
| Si el paciente y su familia es ambivalente acerca de la discusión sobre el pronóstico y la enfermedad es estable | · Retrasar en dar información del pronóstico · Repita los pasos 1 a 3 a lo largo del tiempo para cultivar la conciencia pronóstica. |
| Si el paciente y su familia es ambivalente sobre la discusión del pronóstico, pero la enfermedad está empeorando: | · Alinear con el paciente y su familia. · Nombra el dilema: "Parece que le resulta difícil hablar sobre la posibilidad de que su hijo se ponga más enfermo". |
| Si el paciente y su familia están listo para discutir el pronóstico, independientemente del estado de la enfermedad: | · Entregar información de pronóstico · Pregunte-cuente-pregunte: descubra lo que el paciente y su familia quieren saber, proporcione información y luego pregunte qué opina de ella · Combine la esperanza y la preocupación: "Espero que se sienta bien durante mucho tiempo, pero estoy preocupado porque sus condiciones se ven mucho peor". |
Hay que considerar que: (10)
· La comunicación pronóstica eficaz es una tarea difícil y es esencial practicarla y establecer prioridades;
· Los pacientes y las familias que comprenden el pronóstico están facultados para tomar decisiones informadas que se alinean con sus objetivos de atención establecidos;
· Que un enfoque comprometido para la toma de decisiones es importante para todos los pacientes, y es particularmente crítico para los pacientes que no tienen más opciones curativas.
· El afrontamiento que oscila entre más y menos realista, es un patrón normal. (11)
La negación:
· No es un signo de afrontamiento malsano;
· Es una herramienta para que los pacientes y sus familias integren de forma segura y lenta la realidad de la muerte a lo largo del tiempo; y
· Es importante tolerar esta variabilidad y recordar la necesidad de utilizar la negación como mecanismo de afrontamiento que cambia con el tiempo;
Afrontamiento normal:
· El afrontamiento es como un péndulo oscilante de conciencia, de más integrado y realista a menos
integrado e irrealista;
· Este tipo de afrontamiento no es "negación" en su sentido tradicional, sino más bien una integración saludable y pausada de información que, desde la perspectiva del paciente, de otro modo se sentiría inimaginable.
Elementos clave en la conciencia pronóstica: (11)
· Los miembros de la familia con un buen conocimiento del pronóstico pueden promover el conocimiento del pronóstico en el paciente;
· Si los cuidadores tienen una conciencia de bajo pronóstico, puede hacer que el afrontamiento y la integración del paciente sean más desafiantes;
· El objetivo de comunicación es permitir que el paciente y su familia participen en discusiones que exploren más abiertamente el curso probable de la enfermedad para ayudar en la integración psicológica y la estabilización de los datos pronósticos; y
· Los pacientes y familias que han integrado esta información difícil pueden participar de manera más eficaz en la toma de decisiones médicas compartidas con sus médicos.
7.9 COMUNICACIÓN CON LAS FAMILIAS AL FINAL DE LA VIDA Y DURANTE EL DUELO
Brindar orientación anticipada sobre el proceso de la muerte, es una obligación. A continuación, se dan tres recomendaciones básicas para tratar este tema de anticipación de la muerte: (4, 10)
1. Discutir con las familias los planes de manejo de síntomas y la disponibilidad del personal para garantizar el mayor nivel de comodidad posible para el paciente;
2. Ofrecer actualizaciones del estado clínico a medida que se acerca el final de la vida del paciente, de manera que les permita prepararse para el momento de la muerte; y
3. Desarrollar un plan de atención para el duelo, en colaboración con el paciente y la familia.
7.10 COMUNICACIÓN CON EL PACIENTE, La comunicación correcta, es aquella cuando se consigue que el niño adquiera confianza en el personal médico y en el desarrollo de la acción del cuidado. Ésta debe estimular la expresión de los sentimientos, pensamientos y expectativas. (4, 6, 10)
· Tener en cuenta lo que le paciente quiere o no saber. Preguntar antes de informar (individualizar la información);
· Personalizada, sencilla, abierta, honesta, veraz y consensuada con los padres; y
· Cuidar el lenguaje verbal. Usar el juego.
Comunicación verbal y no verbal. La comunicación no es un proceso que ocurra de forma lineal, sino en una red de información durante todo el proceso de cuidado al niño, comprendiendo tanto el lenguaje hablado como el no verbal y las actitudes que se presenten. Hacer interrogatorios al niño no suele ser efectivo. Los juegos son un buen camino para hacer que se comunique en una forma abierta y despreocupada. (6)
El juego como instrumento de comunicación en los cuidados paliativos pediátricos. (CPP). El juego: (1, 10)
· Es la forma más importante en que los niños aprenden, adquieren confianza y manejan las tensiones de la vida en su mundo;
· No es sólo una diversión. Proporciona estimulación para el desarrollo, distracción, exploración, socialización y entretenimiento;
· Permite a los niños la capacidad de comunicar sus ansiedades y miedos tácitos;
· Es una intervención terapéutica para los niños que han experimentado el shock de un diagnóstico que amenaza su vida o de procedimientos médicos traumáticos; y
· Favorece en los niños el desarrollo físico, emocional, social, cognitivo y del lenguaje. Estas habilidades son siempre importantes en la infancia, pero aún más cuando el niño está enfermo y fuera de su rutina normal.
Consideraciones importantes del juego: (1, 10) En los CPP, la mayoría de los niños han sufrido importantes trastornos y restricciones en su situación familiar normal, por lo que necesitan jugar incluso más que los niños sanos.
· La mayoría de los trabajadores sanitarios se sienten ansiosos por jugar con los niños y no saben cómo hacerlo;
· Los niños con enfermedades que limitan su vida son más propensos que otros niños a perder oportunidades de juego, a pesar de que necesitan jugar para ayudarles a sobrellevar y aceptar su enfermedad;
· El niño más enfermo puede ser ayudado a jugar;
· Para los niños con enfermedades que limitan su vida, o para los niños que han sufrido traumas y estrés, el juego es el medio más natural para liberarse de la agresividad, aceptar el trauma de la enfermedad y la muerte inminente e intentar tomar el control de su mundo; y
· Los juguetes deben ser seguros y estar limpios. En la mayoría de los entornos de CPPP existe un riesgo de infección cruzada, por lo que los juguetes deben mantenerse limpios y en buen estado y desecharse si se rompen o se vuelven inseguros.
7.11. COMUNICARSE CON LOS HERMANOS Y LA FAMILIA EXTENDIDA
La comunicación con los hermanos puede afectar considerablemente la forma en que una familia se adapta a la enfermedad y al tratamiento.
Imagen 3. Comunicación con hermanos y familia extendida.
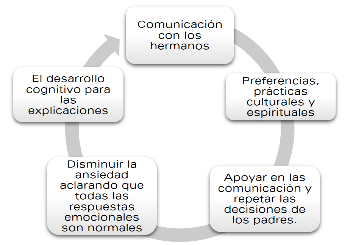
Los hermanos que reciben una comunicación adecuada de la condición clínica de su hermano tienen niveles más bajos de inadaptación a largo plazo.
Con ellos hay que tomar en cuenta que: (10) Al facilitar la comunicación con y entre todos los miembros de la familia, el equipo médico puede ayudar a los miembros de la familia a:
· Adaptarse a sus nuevos roles;
· Procesar sus emociones;
· Interactuar adecuadamente con el paciente; y
· hacer frente a las secuelas de la muerte de un niño si es el caso. 9
7.12. CONCEPTOS DE MUERTE Y ENFERMEDAD EN EL NIÑO / ADOLESCENTE.
En el camino de la curación y la salud, o de la enfermedad y la muerte, generar la capacidad de comprensión y contención de las alteraciones emocionales provocadas por estas, se convierte en el objetivo fundamental de las estrategias de comunicación, con el paciente, la familia y el equipo de salud, haciendo énfasis en los siguientes aspectos: (11) comprensión de información, contención emocional, toma de decisiones y aceptación, y adherencia a los cuidados paliativos.
Otro de los objetivos es buscar la causa del malestar emocional asociada a la enfermedad y su tratamiento, abordando los sentimientos de frustración, tristeza, depresión, ansiedad, aislamiento, vacío existencial, y otros.
Cuando la cura es incierta y los procedimientos riesgosos, dolorosos o invasivos como en ocasiones es el caso de los CPPP, la intervención psicológica debe conducir a una comunicación colaborativa en pro de que la decisión de los tratamientos sea tomada desde la historia individualizada, es decir, desde "el bien" para el paciente y no para "la ciencia" (12). Es fundamental enfatizar con la familia y el paciente: (13)
· Las fortalezas, potenciando los factores positivos.
· La información adecuada acerca de la enfermedad y el tratamiento.
· El apoyo y soporte psicológico/social necesario de acuerdo con la fase de la enfermedad.
· La guía y ayuda para encontrar los medios que faciliten mejor afrontamiento a la enfermedad.
· El desarrollo de habilidades para sentirse seguros y tranquilos.
Siendo así, en el contexto global médico y familiar, la información compartida a los niños y adolescentes sobre su enfermedad y la muerte deberá tomar en cuenta lo siguiente: (15)
Criterios generales para transmitir información a los padres y a los niños o adolescentes sobre su enfermedad y la muerte.
1. Cada niño tendrá una comprensión de la enfermedad y de la muerte, en función de su edad, por lo que expresarán sus sentimientos y miedos de manera diferente;
2. La comprensión del paciente dependerá de su desarrollo cognitivo-afectivo y del grado de afectación cognitiva generada por su padecimiento;
3. Las estrategias por implementarse deben tener en cuenta la etapa en la que se encuentra el paciente en su proceso de aprender, crecer, disfrutar, jugar, desarrollarse, pertenecer a un grupo social, buscar la oportunidad de autonomía e independencia, tener derecho a expresarse y tener derecho a sentir;
4. No dejar a un niño sin información, porque se le deja en manos de una interpretación de la realidad en base a sus miedos y fantasías;
5. Cuando hay negación de la situación de la enfermedad y de las dificultades que conlleva se confunde al niño y se aumenta su ansiedad;
6. El niño se da cuenta de que algo no está bien, por las condiciones propias de su cuerpo, por los gestos de sus familiares, por los otros niños enfermos, por el ambiente del hospital, etc.; y
7. La comunicación debe ser bidireccional con el niño para que él pueda formular preguntas, manifestar sus sentimientos y emociones, y desahogarse.
Derechos del niño enfermo. Aún en la actualidad se sigue luchando contra la idea de que el paciente pediátrico no tiene la capacidad de comprender el mundo que le rodea. Prevalece el significado de la palabra "infancia" en su raíz latina, que significa "incapacidad de hablar". Al pensarlo así, se sostiene que el niño es hablado por otro y que no tiene voluntad propia. Esta idea, en pleno siglo XXI, no debe prevalecer en la interacción que la familia y personal de salud sostienen con el paciente, ya que del lado del niño, es su derecho recibir información, y del lado del familiar y del equipo de salud es su obligación brindarla, por eso es importante que, a partir de los derechos del enfermo terminal que establece la OMS (1990), se dictan los derechos del niño enfermo para norman la actuación del personal de asistencia médica, los cuáles se mencionan a continuación: 15
· Tengo derecho a ser visualizado y concebido como sujeto de derechos y no propiedad de mis padres, médicos o de la sociedad;
· Tengo derecho a que se tome en cuenta mi opinión a la hora de tomar decisiones, ya que soy yo quien está enfermo;
· Tengo derecho a llorar, enojarme, sentir ira o frustración por mi enfermedad;
· Tengo derecho a jugar y a comportarme como niño/adolescente;
· Tengo derecho a que se contemplen mis necesidades en forma integral;
· Tengo derecho a que se me controle el dolor del primer momento;
· Tengo derecho a la verdad de mi condición, a que se responda con honradez y veracidad a mis preguntas;
· Tengo derecho a no tener dolor a la hora que se efectúen procedimientos, diagnósticos y terapéuticos;
· Tengo derecho a una muerte digna, rodeado de mis seres amados y de mis objetos más queridos;
· Tengo derecho a morirme en casa y no en el hospital si así lo deseo;
· Tengo derecho a sentir y expresar mis miedos;
· Tengo derecho a que se me ayude a elaborar mi muerte, así como a mi familia;
· Tengo derecho a negarme a recibir tratamiento cuando no exista cura para mi enfermedad si así lo deseo;
· Tengo derecho a recibir cuidados paliativos;
· Tengo derecho a fabricar fantasías;
· Tengo derecho a no estar solo; y
· Tengo derecho a ser sedado a la hora de enfrentar mi muerte, si así lo deseo.
Es esencial tomar cuenta el desarrollo cognitivo-afectivo que se enlaza con el concepto de enfermedad y de muerte, según las etapas de desarrollo del paciente: prelingüística, preescolar, escolar, preadolescencia y adolescencia. (15)
| Tabla 3. Desarrollo cognoscitivo-afectivo y concepto de enfermedad y muerte. (16) | |||
| Etapa | Desarrollo | Temores | Concepto de enfermedad y muerte |
| Etapa Prelingüística (0-18 meses) | Sensorio Motriz Respuesta al dolor, al malestar y a las personas extrañas. | A la ausencia de los padres. Al dolor. Al entorno hospitalario | No hay concepto del tiempo ni de la enfermedad |
| Etapa Preescolar (18 meses a los 5 años) | Desarrollo más significativo en lo lingüístico Reconoce las partes de su cuerpo. Existe pensamiento mágico/narcisista. | A portarse mal y que se les aparezca un monstruo. A dormirse y no encontrarse acompañado. Al dolor, a la ausencia de los padres y al entorno hospitalario | Sabe que parte de su cuerpo enferma y cree que la enfermedad está causada por factores externos o por accidentes. La muerte es un sueño donde se da pérdida de movilidad, separación, mal funcionamiento -temporal-. Los muertos respiran, comen y se trasladan de un lugar a otro. Pueden vivir la enfermedad como castigo, por malos comportamientos o pensamientos |
| Etapa Escolar (6 a 12 años) | Aumenta la interacción, competitividad social e interés por conocer y explicar su entorno. Madura el concepto del tiempo. Conoce las funciones de cada parte y entiende los factores internos y las causas. | A la mutilación. A la separación. Al rechazo del grupo social y por eso se aísla, se retrae y se comporta agresivo. A no poder participar en sus actividades diarias. | Expresa curiosidad por la muerte y por las reacciones sociales. Busca entender las causas de su enfermedad y los cambios que ocurren en el cuerpo. Cree que la muerte es selectiva y que sólo afecta a los ancianos. Tiende a personificar a la muerte. |
| Preadolescencia y Adolescencia (13 a 18 años) | Se afinan los conceptos de irreversibilidad, universalidad y permanencia de la muerte. | A morirse. A que mueran sus seres queridos. A cambios físicos. A perder sus cosas. A ser rechazado por el grupo social y a que se vea afectado su rendimiento. Por eso tiende a ser agresivo, aislarse y estar ansioso. Mayor preocupación por perder a sus amistades y en las consecuencias en su imagen y proyecto de vida, como consecuencia de la enfermedad. | La muerte ya no es selectiva; es universal. De la muerte no se regresa y constituye una desaparición permanente. La muerte representa el fin de proyectos. Existen causas desconocidas a la enfermedad. Se hace una abstracción de la vida después de la muerte. |
Preparación para el diálogo con el adolescente. Con base al cuadro anterior, se sugiere formular las siguientes preguntas antes de establecer la comunicación con el niño o adolescente. Estas incluso, pueden servir como guía para realizar el diálogo: (16)
Imagen 4. Guía de preparación para el diálogo con el niño y el adolescente
| A. · ¿Hay concepto de enfermedad o de muerte? · ¿Tiene concepto de temporalidad? · Si tiene el concepto de muerte, ¿qué entiende por ello? |
| · B. · ¿Reconoce cuál es la parte de su cuerpo que está enferma, y cuáles son sus consecuencias? · ¿Cómo explica la causa de la enfermedad? · ¿Se siente culpable por estar enfermo? |
| · C. · ¿Cree que morir es estar dormido? · ¿Expresa curiosidad por saber de qué se trata morir? · ¿Le preocupa lo que va a pasar después de morir? · ¿Le da miedo el dolor y el dejar a sus padres? · ¿Tiene un concepto de espiritualidad? |
Para que sea ajustada la comunicación con el paciente, siguiendo las particularidades de cada uno de ellos, se puede utilizar el siguiente listado de recomendaciones: (16)
· Partir de los conocimientos médicos que ya posee el niño sobre su dolencia, aprehensiones y temores;
· Emplear un lenguaje y un estilo de explicación asequible a su nivel cognitivo: juguetes y material de "psicoeducación" que permita visualizar sus dolencias;
· Dar información que abarque lo que pasa sobre los padres, el hospital, la actitud de los adultos y la conducta del personal sanitario;
· Estar abiertos a cualquier tipo de pregunta, dando respuestas realistas y teñidas de esperanza;
· No ir más allá de lo que el niño necesita o desea saber. Él marca el límite y la necesidad de información;
· La información diagnóstica inicial debe ser ofrecida en cuanto se disponga de ella para evitar que se genere demasiada ansiedad y procesos imaginarios traumáticos;
· Neutralizar temas de culpas; al contrario, reforzar la calidad del cuidado de los padres y su competencia;
· Propiciar una comunicación multidimensional: contacto visual, contacto físico, caricias, empatía y cercanía afectiva;
· Mantener una comunicación alegre y proactiva, buscando otros temas y otras propuestas para participar en actividades lúdicas o académicas que lo estimulen a vivir otras esferas;
· Respetar, pero también neutralizar las ideas religiosas que producen un mayor temor;
· Estar atento a las propias vivencias y emociones de uno mismo con respecto a la enfermedad y la muerte, para evitar que interfiera en la relación o incremente el nivel de angustia;
· Verificar lo que se ha entendido por la enfermedad, los procedimientos y la muerte; y
· Tratar a los padres como parte del equipo, recordando que ellos reforzaran la información que se da.
7.13 COMUNICAR MALAS NOTICIAS
Una mala noticia es toda aquella que afecta de forma drástica, negativa y grave a la visión que un individuo tiene de su futuro. Toda mala noticia, por tanto, tiene graves consecuencias adversas para los pacientes y sus familias; el impacto es proporcional a su efecto en el cambio de las expectativas del paciente. (17)
Es importante definir el elemento central de las malas noticias: es decir, tratar de identificar qué es lo que las hace tan malas para el paciente. En la mayoría de los casos esto es obvio, como el diagnóstico de una enfermedad grave que limita la vida y, en consecuencia, tener que enfrentarse a una vida limitada y/o a la pérdida de funciones y/o de calidad de vida. (17)
La tarea general de comunicar malas noticias se puede subdividir de manera útil en tres fases: preparación, entrega y seguimiento. (3)
Imagen 5 Protocolo para dar malas noticias.
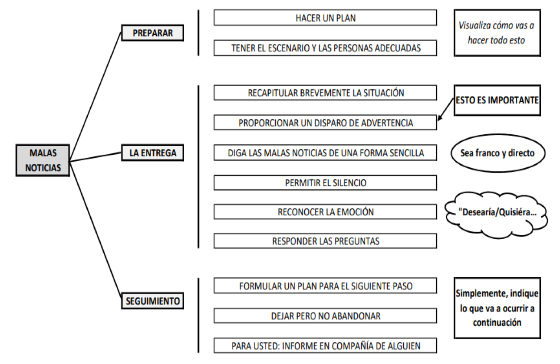
Protocolo confort. Es un protocolo que describe siete principios como marco para el desarrollo de una comunicación integral, en el campo de la enfermería. COMFORT es un acrónimo, cuyas siglas son: 2
· Comunication (comunicación),
· Orientation and Opportunity (orientación y oportunidad),
· Mindfulness (tener conciencia de),
· Family (familia),
· Oversight (vigilancia),
· Reiterative and Radically adapt messages (repetir y adaptar gradualmente los mensajes), y
· Team (equipo).
Protocolo Spikes
| Pasos | Ejemplos |
| 1. Entorno | Prepárese: Lugar, contexto y acuerdos entre el equipo |
| 2. Percepción | Escuchar antes de hablar: ¿Qué sabe o que entiende sobre la enfermedad de su hijo? |
| 3. Invitación | Pida permiso: ¿A ustedes les gustaría recibir toda la información disponible de una forma detallada? ¿O más bien desean una idea general de lo que está sucediendo sin demasiado detalle? |
| 4. Comunicar | Comparta la información: "Desafortunadamente, la biopsia muestra que José tiene cáncer" |
| 5. Empatía | Responda a las emociones: "Entiendo lo difícil que puede ser pensar en la posibilidad de enfermarse más de este cáncer" |
| 6. Estrategia | Explique el plan a seguir: Antes de finalizar la reunión, quiero que repasemos las metas de cuidado o el plan a seguir |
Tabla 4 Protocolo SPIKES (2000), conocido en español como EPIDEE. (2,7)
Ejemplo de comunicación de malas noticias. La forma en que se entrrega la información puede afectar el ajuste del paciente y la familia a la enfermedad y al tratamiento, tanto positiva como negativamente. (7,8)
| COMPONENTES | PAUTAS CLAVE | EJEMPLOS |
| Preparar la configuración | Lugar tranquilo. Todas las partes deseadas presen-tes y sentadas. | |
| Obtener comprensión | Tomar la iniciativa, preguntar a la familia para describir su actual comprensión | "¿Qué has escuchado hasta ahora sobre lo que está pasando?" |
| Proveer "disparo de advertencia" | | "Me temo que tenemos noticias difíciles de discutir". "Desafortunadamente, los resultados no mostraron lo que esperábamos". |
| Dar el diagnóstico | Usar un lenguaje claro. Evitar los eufemismos. Usar el nombre de la enfermedad. | "Su hijo tiene leucemia, que es un tipo de cáncer". |
| Hacer pausa | Parar de hablar Permitir que la familia procese la información. Provocar preguntas | |
| Discutir tratamiento | Discutir el lugar y la duración esperada del tratamiento. Explicar las diferentes modalidades. Proporcionar opciones. | "Usaremos una combinación de cirugía seguida de medicamentos llamados quimioterapia para tratar el cáncer. La mayor parte de la quimioterapia se administrará durante las hospitalizaciones que duran entre 3 y 5 días. En general, el tratamiento durará aproximadamente seis meses". |
| Hacer pausa | Parar de hablar Permitir que la familia procese la información Provocar preguntas. | |
| Definir metas de cuidado | Proporcionar una comunicación clara y honesta con respecto a la intención curativa | "El objetivo de la terapia es curar el cáncer de su hijo". "Desearíamos que en este momento existiera algún tratamiento curativo para el cáncer de su hijo. Por lo que ahora el objetivo del tratamiento será minimizar los síntomas y mejorar su calidad de vida". |
| Hablar de la causalidad | Disipar las preocupaciones de que la enfermedad sea el resultado de algo que el niño o la familia hicieron o no hicieron. | "No sabemos qué causa este tipo de cáncer, pero sabemos que no hay nada que usted o su hijo hayan hecho para causarlo. Hiciste lo correcto al traer a su hijo cuando lo hizo". |
| Resumir clave | Repetir el diagnóstico, los objetivos del tratamiento y la discusión de la causalidad | "Por hoy, lo que es importante que entienda es que su hijo tiene cáncer y planeamos tratarlo con quimioterapia; el objetivo del tratamiento es curar. No hay nada que usted o su hijo pudieron haber hecho para evitarlo. Esto no es su culpa" |
| Concluir conversación | Ofrecer la tranquilidad de que la información se discutirá nuevamente en futuras visitas. Planificar para la próxima visita. Proporcionar información de contacto para cuestiones urgentes. | Discutiremos toda esta información nuevamente, así que no se preocupe si no puede recordar todo. Lo veré en la clínica de nuevo mañana por la tarde. Si tiene alguna inquietud antes de esa fecha, siempre puede llamar a la clínica en ... |
Tabla 5. Ejemplo de comunicación de malas noticias
Pasos para la comunicación en reuniones familiares. (2)
En el inicio:
Asegurarse de que todos están sentados cómodamente.
· Presentar a todos los asistentes;
· Proponer un orden del día y pedir a la familia que contribuya en él;
· Aclarar lo que todos entienden sobre la situación del paciente.
En la planificación:
· Invitar a la familia a una reunión, mencionando el propósito;
· Decidir con la familia y con el personal cuándo, dónde y quién debe asistir;
· Permitir que la familia escriba sus preguntas o preocupaciones;
· Asegurarse de que el personal clínico está informado y de acuerdo;
· Decidir quién dirigirá la reunión.
En el diálogo:
· Escuchar más, hablar menos;
· Ser curioso y hacer preguntas;
· Tolerar el silencio;
· Reconocer las emociones;
· Procurar establecer metas de cuidado claras y definidas;
· Discutir el pronóstico sin rodeos, pero reconociendo la incertidumbre;
· Expresar sus propias preocupaciones y deseos en relación con el bienestar del paciente;
· Explorar la gama de lo que cada uno espera, dada la situación;
· Proporcionar información concreta sobre las opciones de tratamiento paliativo y no paliativo;
· Ser ecuánime y afirmar las opciones de tratamiento; y
· Si no se llega a un consenso, planificar el diálogo y quizás la recopilación de información.
Acciones y seguimiento:
· Comunicar los objetivos de la atención al resto del personal clínico;
· Asegurarse de que todos los pasos de atención acordados se realicen de manera oportuna; y
· Celebrar reuniones de seguimiento según lo acordado.
Conclusión:
· Revisar el orden del día y asegurarse de que se han tratado todos los temas;
· Reiterar los objetivos de atención acordados;
· Reafirmar los próximos pasos acordados para la atención;
· Confirmar el acuerdo;
· Si no hay consenso, reconocerlo y exponer el plan para avanzar hacia el consenso;
· Decidir cuándo volver a reunirse; y
· Agradecer a toda su contribución.
7.14 CONSPIRACIÓN DE SILENCIO.
La Conspiración de silencio o también llamado Pacto de Silencio es una barrera en torno a la verdad. (18, 19) Se define como el acuerdo implícito o explícito por parte de los familiares, amigos y/o profesionales de la salud de cambiar, ocultar u omitir la información que se le da al paciente, ya sea de manera parcial o total acerca del diagnóstico y/o pronóstico y/o gravedad de su estado real, sin tener en cuenta los deseos de saber del mismo. (20, 21)
Tipos de conspiración de silencio. (20)
· Conspiración adaptativa. El paciente es la persona que niega, evita, no habla, o no quiere saber su diagnóstico o pronóstico; (20)
· Conspiración inadaptada. La familia y/o los profesionales de la salud son los que tienen dificultades para establecer técnicas de comunicación claras. Al mismo tiempo, la actitud de los agentes involucrados puede motivar este proceso, ya que los familiares podrían ser aquellos que no responden u ocultan información a los pacientes cuando hacen preguntas. Sin embargo, el equipo de salud también podría desarrollar este patrón de comportamiento cuando notan una actitud pasiva de los pacientes y sus familias; (20)
Es importante señalar que tanto los miembros de la familia como los equipos de salud, se involucran en la divulgación de información de dos formas: (21)
· Correctores conspiradores absolutos que retienen todos los datos, hechos, gravedad de la enfermedad, detalles de diagnóstico, progresión de la enfermedad y pronóstico de la enfermedad de los pacientes; (21) y
· Correctores conspiradores parciales que informan a los pacientes sobre los diagnósticos, pero se niegan a recibir o dar cualquier información sobre los pronósticos. (21)
Causas de la conspiración de silencio. La finalidad principal es "evitar el sufrimiento" que consideran innecesario en el paciente y protegerlo del impacto emocional causado por la información. (18, 2)
Otras posibles razones son:
· Miedo a repercusiones negativas que puedan derivarse de la revelación de la verdad: depresión, pérdida de interés por la vida, locura, empeoramiento del estado físico y sufrimiento innecesario;
· Modelo de atención paternalista;
· Dificultades de comunicación en el entorno del paciente, familia y equipo de salud;
· Falta de tiempo y el ambiente inadecuado para proporcionar la información al paciente y su familia;
· Falta de formación del equipo de salud con respecto a la comunicación de malas noticias en el paciente al final de la vida y poca pericia en el manejo de situaciones emocionales fuertes;
· Complejidad de establecer un diagnóstico preciso;
· No aceptar que no existe la posibilidad de cura terapéutica para el paciente, significa el sentimiento de fracaso del médico y sentimiento de frustración de la familia;
· Creer que hablar de enfermedad en fase terminal es sinónimo de "no hay nada más que hacer";
· Dificultad para discutir temas de final de la vida asociada a los tabúes generados en nuestra sociedad;
· Creer que decir la verdad puede disminuir la esperanza o acelerar la muerte, generar depresión e intento de suicidio; y
· Asumir que los pacientes no quieren conocer su estado.
Consecuencias de la conspiración de silencio. (18, 21)
En el paciente:
· Pérdida de la autonomía en la toma de decisiones respecto a su salud;
· Sentimiento de frustración ante un deterioro evidente con desconocimiento de causa y sin mejoría a pesar de los tratamientos recibidos;
· Desconfianza con la familia y/o cuidador principal de quienes pasa a depender completamente;
· Aislamiento social, el sentirse incomprendido, solo, engañado, abandonado, se hace complicada la expresión de emociones, con incapacidad para permitir el cierre de asuntos importantes;
· Falta de confianza en el equipo asistencial y bloqueo de la comunicación con el equipo sanitario;
· Pérdida de la satisfacción de necesidades espirituales que aparecen ante la muerte, como, por ejemplo: orar, reconciliación, soledad-silencio, gratitud; y
· Preocupaciones fuera de proporción: ansiedad, miedo, depresión, confusión e ira.
En la familia
· Negarse a aceptar una posible muerte, establecen patrones silenciosos que provocan bloqueos de comunicación en el sistema familiar. Con frecuencia esto provoca dificultad o incapacidad psicológica para elaborar el duelo, antes y después de la muerte del ser querido;
· Bloqueo de comunicación entre la familia y el paciente;
· Alteración del afrontamiento de la muerte, calidad de vida en los últimos días y duelo posterior al fallecimiento;
· Agotamiento y costo emocional elevado; y
· Aparición de toma de decisiones erróneas, al desconocer la información completa y verídica, que favorecen el sentimiento de culpa en la familia.
En el equipo de salud
· Tendencia a emitir juicios y valoraciones equivocadas;
· Síndrome de desgaste profesional;
· Afectación al sistema de salud al establecer una barrera de comunicación en torno a la verdadera naturaleza de la enfermedad;
· Falta de empatía entre el equipo de salud, el paciente y su familia;
· Deshumanización del proceso de atención al final de la vida.
Recomendaciones para evitar la conspiración del silencio. (18, 20, 22)
· Mantener una actitud empática con el paciente y familia;
· Sentar las bases adecuadas de comunicación desde el inicio de la relación médico, paciente y familia;
· El paciente debe estar acompañado de sus cuidadores y familia;
· No engañar, ni mentir; de lo contrario se perderá la confianza en el equipo de salud y/o familia;
· Brindar la información de manera paulatina, a partir de lo que el paciente ya conoce y aún no ha expresado y de aquello que desea saber;
· Favorecer el duelo anticipado; y
· Dar a conocer las consecuencias de la conspiración de silencio.
BIBLIOGRAFÍA
1. Amery J. A really practical handbook of children's palliative care. Lulu Publishing Services; 2016: 23-43; 155-171.
2. Martin EJ, Rich SE, Jones JA, Dharmarajan KV. Communication skill frameworks: applications in radiation oncology. Ann Palliat Med. 2019;8(3):293-304.
3. Feudtner C. Collaborative communication in pediatric palliative care: a foundation for problem-solving and decision-making. Pediatr Clin North Am. 2007;54(5):583-607, ix.
4. SECPAL [Internet]. Secpal.com. [cited 2021 Aug 9]. Available from: https://www.secpal.com/biblioteca_guia-cuidados-paliativos_12-informacion-y-comunicacion
5. Marcuello García AA. Técnicas para la comunicación eficaz [Internet]. Psicologia-online.com. Psicologia-online.com; 2018 [cited 2021 Oct 5]. Available from: https://www.psicologia-online.com/tecnicas-para-la-comunicacion-eficaz-3124.html
6. Rojo Pérez M. CUIDADOS PALIATIVOS PEDIATRICOS: LA COMUNICACIÓN CON EL NIÑO Y LA FAMILIA. Revisión bibliográfica [Internet]. [España]: Universidad de Valladolid; 2015 [cited 2021 Aug 1]. Available from: https://uvadoc.uva.es/bitstream/10324/11817/1/TFG-H223.pdf.
7. Quintero XG. Taller EmPalPed: Mensajes Esenciales en Cuidados Paliativos y Dolor en Niños. Programa Cuidados Paliativos Pediátricos "Cuidando De Ti" [Colombia]: My Child Matters, Fundación Valle de Lilli y Universidad ICESI; 2021.
8. Blazin LJ, Cecchini C, Habashy C, Kaye EC, Baker JN. Communicating effectively in pediatric cancer care: Translating evidence into practice. Children (Basel) [Internet]. 2018;5(3). Available from: http://dx.doi.org/10.3390/children5030040
9. Jackson VA, Jacobsen J, Greer JA, Pirl WF, Temel JS, Back AL. The cultivation of prognostic awareness through the provision of early palliative care in the ambulatory setting: a communication guide. J Palliat Med. 2013;16(8):894-900.
10. Downing J, editor. Children's palliative care: An international case-based manual. 1st ed. Cham, Switzerland: Springer Nature; 2020: 74-85, 165-174.
11. Zas Ros B. La psicología en las instituciones de Salud. In Cuba; 2000.
12. Devereux G. De la ansiedad al método en Las ciencias del comportamiento. Siglo XXI Ediciones; 1998.
13. Carrasco U, Estefania A. Necesidades básicas de los cuidadores primarios de niños con cáncer. México: Universidad de las Américas; 2013.
14. García Ramos JC. Psicología Hospitalaria y de Enlace 29/06/2013 en Instituciones de Salud. Http//saludmental-queretarobligoo.com mx/tag/psicología. 2013
15. Quesada Tristán L, Cárdenas Mata AC. Cuidado Paliativo Pediátrico en Medicina Paliativa en la Cultura. Latina; España: Ediciones Aran; 1999.
16. Trill MD. Psico-Oncología. España: ADES; 2003
17. Defining Bad News [Internet]. Stanford.edu. 2013 [cited 2021 Sep 13]. Available from: https://palliative.stanford.edu/communication-breaking-bad-news/defining-bad-new/
18. Espinoza-Suárez NR, Zapata del Mar CM, Mejía Pérez LA. Conspiración de silencio: una barrera en la comunicación médico, paciente y familia. Rev Neuropsiquiatr. 2017; 80(2):125-136.
19. Ruiz-Benítez M, C CM. El pacto de silencio en los familiares de los pacientes oncológicos terminales. Psicología. 2008: 53-69.
20. Cerdas -Vargas B. Técnicas para romper con la conspiración del silencio en la enfermedad terminal. Rev Med Cos Cen 2010; 67 (595) 461-467.
21. Díaz-Cordobés JL, Barcia JA, Gallegos-Sánchez J.M, Barreto P., Conspiración de Silencio y malestar emocional en pacientes diagnosticados de Glioblastoma multiforme. Psicooncología 2012 9(1), 151-159.
22. Achury D.M., Pinilla M. La comunicación con la familia del paciente que se encuentra al final de la vida, Enfermería Universitaria 2016; 13(1):55-60.
CAPÍTULO VIII
CONSIDERACIONES BIOÉTICAS EN LOS CUIDADOS PALIATIVOS PEDIÁTRICOS
8.1 INTRODUCCIÓN
Resulta fundamental que los profesionales dedicados a los cuidados paliativos pediátricos cuenten con conocimientos de bioética que apoyen en la toma de decisiones, así como elementos teóricos y metodológicos para guiar el proceso deliberativo.
En este sentido, la bioética combina el rigor filosófico con el aporte de diversos campos del conocimiento, para ofrecer claridad en torno a fenómenos morales complejos, como también involucra a los usuarios de los servicios y a sus familias en el cuidado de su propia salud y promueve que el proceso de toma de decisiones sea autónomo e informado. Para ello, se requiere un cambio de paradigma en la relación médico-paciente, en la que se sitúen los intereses y bienestar de niñas, niños y adolescentes en el centro del proceso de atención; asimismo, en cuanto a la dinámica de los equipos de salud, promueve el diálogo horizontal y el intercambio de experiencias y puntos de vista, asegurando los más altos estándares de calidad y seguridad a lo largo de este proceso, con perspectiva de derechos humanos y en virtud de resguardar el interés superior de la niñez y sus libertades fundamentales al momento de evaluar y ponderar el equilibrio entre los beneficios y los riesgos de un tratamiento y evitar la carga desproporcionada de intervenciones que vulneren la dignidad de la persona.
Los avances de la ciencia y la tecnología han favorecido la preservación de la vida, incluso en condiciones no propicias para ello; en este contexto, los comités hospitalarios de bioética tienen la posibilidad de apoyar al personal sanitario, a los usuarios y familias, particularmente en el momento en el que se decide interrumpir el tratamiento y dirigir los esfuerzos al cuidado paliativo.
8.2 MARCOS TEÓRICOS
La deliberación bioética está y debe estar al alcance de todas las personas. Sin embargo, para que esta deliberación sea verdaderamente reflexiva y crítica necesita ser sistemática y rigurosa. Los marcos teóricos en ética proporcionan estas cualidades.
A continuación, se describen brevemente algunos de los marcos teóricos más utilizados, usualmente de forma combinada, en la deliberación bioética sobre los dilemas de cuidados paliativos en pediatría.
Ética utilitarista. Este marco teórico ético consiste en poner el foco de atención en las consecuencias de una decisión y tratar de maximizar la utilidad usando la máxima utilitarista del mayor bien para el mayor número de personas. Aunque hay muchas versiones del utilitarismo se recomienda la combinación de este con otros marcos bioéticos, el uso del utilitarismo duro puede resultar una postura muy economicista y atentar contra la integridad y la dignidad humanas. (1)
Ética deontológica. Desde esta posición ética se hace hincapié en los deberes y derechos. La ética deontológica que nace con Kant se preocupa de la universalización de los juicios éticos y de nunca tratar a las personas como meros medios para alcanzar un fin, sino también como fines en sí mismos.
Ética de las virtudes. Los autores de esta escuela ética proponen un retorno a la virtud del personal de salud y de la ciudadanía en general, entendida esta como la acción de habituarse a tener buenas disposiciones hacia los demás. Neoaristotélicos como MacIntyre exponen que el foco de la ética debe estar más en qué tipo de personas debemos ser, que en qué acciones debemos realizar. De este modo la ética se transforma en la prudencia dirigida a la consecución de la felicidad.
Ética del cuidado feminista. Autoras como Martha Nussbaum proponen la incorporación de ciertas virtudes construidas socialmente como femeninas a las teorías éticas. Ejemplos de estas virtudes serían la cooperación y el cuidado en contraposición con una sobrevaloración de la autonomía llevada a cabo por teorías de la justicia predominantemente masculinas. Teniendo en cuenta que estos cuidados, lejos de ser imparciales e impersonales, se llevan a cabo en instituciones sociales como la familia (cualquier tipo de familia) y cuya distribución de cargas debe ser reflexionada.
8.3 MARCOS METODOLÓGICOS EN APOYO A LA TOMA DE DECISIONES
Nueva Casuística o Ética de Casos. En 1988 Toulmin y Jonsen, rehabilitan la Casuística en el discurso ético moderno y la proponen como un método de razonamiento moral que aplicado correctamente permite tomar decisiones sensatas y razonables en problemas morales complejos. Junto a Siegler y Winslade en su libro Clinical Ethics, proponen el análisis de cuatro temas de relevancia moral en la práctica de dar atención médica a un paciente a través de la interpretación de Máximas, que son opiniones significativas, proverbios, reglas o estándares de conducta de observancia obligatoria. (2, 3) Basados en la prudencia, intentan conocer las formas generales y particulares de cada caso o problema. Pueden existir diversas máximas que son de utilidad en base a cada caso, entre ellas se encuentran quitar el sufrimiento y el dolor, salvar la vida, no prolongar la agonía, y la antigua primero no dañar. En los pacientes que se encuentran en la fase terminal de la enfermedad ya no aplica salvar la vida, aplican el quitar el sufrimiento y no prolongar la agonía. Estas máximas son muy bien comprendidas por los padres y familiares.
La Casuística se basa en el análisis de casos similares que han sido paradigmáticos; para el casuista las pruebas claras del bien y el mal las encuentra en casos más que en teorías o principios, lo que ayuda a tomar soluciones razonables de problemas reales. Las cuatro dimensiones que plantea son:
Indicaciones médicas. Tiene que ver con todo lo relacionado a la enfermedad, a la situación clínica, el nivel de la enfermedad, si es curable o no, que intervenciones se pueden hacer. La fase en que se encuentra el padecimiento es el punto biomédico central en las determinaciones.
Calidad de vida. Es una cualidad o un conjunto de cualidades que nos permiten vivir como un todo. Evaluar la forma en que vive un individuo y de cómo se percibe en las diversas dimensiones del cosmos, de su funcionalidad integral como persona, de la forma en que disfruta su existencia es fundamental en la toma de decisiones. Es importante señalar que cada quien mide o valora su calidad de vida desde la perspectiva individual, que puede o no coincidir con la apreciación de otros. A la hora de optar por decisiones médicas complejas, no sólo debe considerarse el derecho a la vida y que hay que salvarla como sea, ya que el derecho a la vida no es absoluto; la calidad de vida, de cuño reciente es el otro aspecto sobresaliente en la toma de decisiones. Hay pacientes que se encuentran en tales situaciones de deterioro irreversible que hace necesario detener todas las medidas que puedan prolongar una agonía. Es necesario que los médicos cuenten con elementos e instrumentos para tratar de evaluar en lo posible la calidad de vida de sus pacientes y así poder proponer alternativas prudentes en casos muy complicados.
Preferencias del paciente. El respeto a la libertad de la persona es otro valor relevante, el más importante en las resoluciones médicas, pues se relaciona íntimamente con la dignidad. El paciente tiene el derecho a elegir lo que le parezca más conveniente, una vez que ha recibido información amplia y precisa por parte de sus médicos, aunque estos no estén de acuerdo con la decisión. El respeto a la autonomía es el pilar en las libertades democráticas de una sociedad y tendremos que considerar la opinión del niño o adolescente, que muchas veces tiene la madurez suficiente.
Contexto. Todo lo que se relaciona con el ambiente del niño, sea la escuela, el juego, sus amigos, la familia, los padres, el trabajo, su economía, el nivel de compromiso con su hijo, entre otros, tienen importancia en la toma de decisiones médicas.
Estas cuatro dimensiones que plantea la nueva casuística proponen que los llamados casos de "conciencia", sean analizados a través de casos similares, con máximas o estándares de comportamiento general, pero que también analiza las particularidades de cada uno, todos son diferentes, y facilita que un casuista experimentado tome decisiones razonables acerca de acciones particulares en problemas reales. Cada dimensión tiene una importancia diferente en base a cada caso, no hay uno prevalezca. No hay un algoritmo preestablecido, depende más de la habilidad del médico en el que la prudencia marca la pauta. Esta perspectiva de ética clínica no busca la verdad absoluta, está abierta a los cambios, tiene una aplicación práctica considerable y permite tomar soluciones en forma rápida y es muy bien entendida por los padres y familiares. (3, 4)
Principalísimo o Ética basada en Principios. En este modelo, propuesto por Tom L. Beauchamp y James F. Childress en 1978, sus cuatro principios tienen una jerarquía similar y no hay ninguno preponderante, sino cobran valor de en base a cada circunstancia. Son considerados prima facie, que en principio serían obligatorios, sin embargo, no son normas absolutas. Una de las críticas que se le han hecho a este modelo es cuando ocurre una confrontación de principios, por lo que suele complementarse con otros marcos teóricos y metodológicos. (5, 6)
Se presenta una breve descripción de cada principio:
Autonomía. Es la capacidad de autodeterminación de cada ser humano, de pensar, sentir y vivir como le parezca conveniente, siempre y cuando no lesione los intereses de otra persona. Es la cualidad más importante que tiene que ver con la libertad de elegir, el libre desarrollo de la personalidad y la dignidad humana y es la consecución más importante de las luchas democráticas, sin embargo, tiene sus límites, que son la libertad de otra persona o cuando se pueda ocasionar un daño a terceros. A pesar de la capacidad de elegir de los padres, deberá prevalecer el interés superior del niño, considerarlo como sujeto de derecho y no ser propiedad de alguien, como lo precisan las Declaraciones Universal de Derechos Humanos, la Convención Internacional de los Derechos del Niño y las leyes de este país. (7, 8, 9, 10)
Beneficencia. Es un principio rector de todas las actividades médicas, y tiene que ver con la obligación moral de actuar en beneficio de los demás. Sus principios son positivos y relacionados con "hacer el bien" pero no es obligación categórica, pues no estamos obligados a ser caritativos, por ejemplo, sin embargo, sí estamos obligados a proporcionar los mejores tratamientos a los pacientes. Todo tipo de acción que pretenda beneficiar a otras personas (bondad, misericordia, caridad, altruismo, amor, humanidad) son actos de beneficencia, pero este principio deberá ponderar los riesgos y los beneficios. La Beneficencia incluye también juicios sobre la calidad de vida (2) y es esencial en la toma de decisiones clínicas difíciles debe ajustarse a las circunstancias de cada persona. (11)
Justicia. Implica que todos los seres humanos tendrían las mismas oportunidades, y recibirían un trato equitativo, con base en sus necesidades. Tratar de respetar los derechos humanos y la dignidad de las personas otorgando un trato considerado y de calidad, aun con pocos recursos sería un amortiguador para garantizar justicia en alguna medida. Los recursos para salud son siempre escasos, por lo que este principio abarca desde la toma de decisiones sobre la asignación de recursos y establecimiento de prioridades en la política públicas hasta la prevención, curación y rehabilitación oportuna en el ámbito operativo; estrategias como las de cuidados paliativos, que son sustentables y destinadas a mejorar la calidad de vida de los enfermos pueden ser consideradas como un acto de justicia.
No Maleficencia. El no hacer daño en forma intencional es obligado para todo tipo de intervenciones médicas, se considera incluso como una obligación mayor que la de hacer el bien. Este principio tiene un papel importante en las discusiones de dilemas que tienen que ver con la etapa terminal y toma muy en cuenta los juicios de calidad de la vida y puede ser de gran ayuda en la atención de los enfermos. En el caso de no iniciar tratamientos en pacientes en fase terminal o en agonía, cada vez más frecuente en la práctica clínica, uno de los argumentos para esta omisión es hacer un bien evitando una agonía prolongada y el sufrimiento, por lo que la actitud será buena y no maleficente. Para un paciente en condiciones similares, pero con apoyo tecnológico, el retiro de los tratamientos, consensuado con paciente y familia, sí es posible y tiene las mismas bases médicas y éticas. No existen diferencias morales entre no iniciar y retirar tratamientos en estos pacientes. El sustento ético es el mismo; siempre que un tratamiento se pueda no iniciar, también se puede retirar y el retiro puede comenzar con él no iniciar, siempre es mejor no iniciar. En estas situaciones límite, deben valorarse siempre los riesgos y beneficios. Los tratamientos no son obligatorios cuando no suponen ningún beneficio para el paciente o son inútiles y sin sentido.(9, 10, 12) Por ejemplo, en las Reglas Baby Doe, que son parte de una ley federal en Estados Unidos enfocada en la protección del abuso infantil, y señalan que "un tratamiento no debe iniciarse o puede ser retirado en casos de pérdida irreversible de la conciencia o cuando el tratamiento es inútil e inhumano"; en México, está descrito en forma similar en los artículos 166 Bis 5, y 166 Bis 6, de la Ley General de Salud, en que precisa el no inicio o retiro de tratamientos cuando son inútiles e inhumanos. En contraparte, hay médicos que no están dispuestos al retiro o a no iniciar tratamientos, porque consideran que retirar una sonda de alimentación en un paciente en estado vegetativo o retirar el ventilador de un niño irrecuperable y avanzado va en contra de los cimientos de la medicina, que sus principios se resquebrajan, y les angustia "dejar morir de hambre o ahogados a sus enfermos", (12, 13) es la otra postura, tan respetable como la otra; el ser humano es un ser social y hay diversidad de opiniones, pero si se continúan estos tratamientos como el uso del ventilador mecánico en estos casos, se prolonga la agonía y el sufrimiento y se podría considerar obstinación terapéutica, proscrita por la ley en este país. La máxima de lo sagrado de la vida ya no ayuda en este caso y de continuar los tratamientos causamos mayor sufrimiento e incluso ahora podemos ser sujetos de responsabilidad legal.
8.4 ASPECTOS PARA CONSIDERAR DESDE LA PERSPECTIVA BIOÉTICA
Proporcionalidad Terapéutica. Si bien parte del concepto ético es respetar y promover la vida y la salud del niño, es evidente que nadie está obligado a utilizar todas las medidas médicas actualmente disponibles, sino únicamente aquellas que ofrezcan un beneficio razonable. Con el avance tecnológico, se ha abierto la posibilidad de mantener con vida a niños gravemente enfermos que antes fallecían irremediablemente, por lo que se debe distinguir el real beneficio terapéutico o la prolongación de un proceso que conduce inexorablemente a su fallecimiento y sufrimiento, para ello se deberá valorar la utilización de medidas ordinarias y extraordinarias.
Este concepto sostiene que la obligación moral versa en implementar sólo aquellas medidas terapéuticas que guarden una relación de debida proporción entre los medios empleados y el resultado previsible; aquellas intervenciones en las que esta relación de proporción no se cumpla se consideran "desproporcionadas" y no son moralmente obligatorias. Para efectuar en un caso particular el juicio de proporcionalidad deben puntualizarse algunos conceptos como: a) la utilidad o inutilidad de la medida; b) las alternativas de acción, con sus respectivos riesgos y beneficios; c) el pronóstico con y sin la implementación de la medida, y d) los costos (en sentido amplio): cargas físicas, psicológicas, morales, sociales, económicas. (14)
Prevención: Es parte de la responsabilidad médica para con el paciente pediátrico prever las posibles complicaciones o los síntomas que con mayor frecuencia se presentan en la evolución de una determinada condición clínica, así como implementar las medidas necesarias para prevenir estas complicaciones y aconsejar oportunamente a los familiares sobre los mejores cursos de acción a seguir en caso de que ellas se presenten. Este principio permite, por un lado, evitar sufrimientos innecesarios al paciente y, por otro, facilita el no involucrarse de manera precipitada en cursos de acción que conducirán a intervenciones desproporcionadas. (1)
No abandono: Es importante destacar que las decisiones deben centrarse en la autonomía del paciente sin olvidar el deber de cuidar el alivio del sufrimiento y respeto por los derechos y la voluntad de este, por lo que sería éticamente reprobable abandonar a un paciente que rechaza determinadas terapias, aun cuando los profesionales de la salud consideren que ese rechazo o petición sean inadecuados. Permanecer junto al paciente y establecer una comunicación muchas veces es la mejor forma de asistirlo. Ello pone a prueba la verdad de nuestro respeto por la dignidad de toda persona, aun en condiciones de extrema debilidad y dependencia. Abandono consiste en la falta de atención adecuada a las necesidades del enfermo y su familia. Entre sus motivos destacan la falsa idea de que "ya no hay nada que hacer". (15)
Veracidad. Abrir canales de comunicación efectivos y asertivos entre el paciente, personal de salud y familia constituye un beneficio que posibilita su participación en el proceso de toma de decisiones. Sin embargo, hay situaciones en las que el manejo de la información genera especial dificultad para los médicos, en particular cuando se comunican malas noticias, como el pronóstico de una muerte próxima inevitable. Caer en la conspiración del silencio, por un lado, representa una fuente de sufrimiento para el paciente y supone una injusticia, pues lo priva del derecho a ejercer su autonomía. Por otro lado, no revelar toda la verdad acerca del diagnóstico o pronóstico a un paciente determinado no siempre significa violar su autonomía, ya que la comunicación también depende de otros factores, como las prácticas culturales. La comunicación de la verdad médica debe ir precedida por una cuidadosa reflexión sobre qué, cómo, cuándo, cuánto, quién y a quién debe informarse.
Doble efecto. Este principio se basa en que un mismo acto puede tener un efecto bueno y uno malo. La condición moral del acto es: a) que la acción sea en sí misma buena o, al menos, indiferente; b) que el efecto malo previsible no sea directamente buscado, sino sólo tolerado; c) que el efecto bueno no sea causado inmediata y necesariamente por el malo, y d) que el bien buscado sea proporcional al daño eventual provocado.
Vulnerabilidad. El principio de la vulnerabilidad puede definirse como la capacidad disminuida de una persona o un grupo de personas para anticiparse, hacer frente y resistir a los efectos de un peligro natural o causado por la actividad humana, y para recuperarse de los mismos. La población pediátrica puede tener dificultades para expresarse, entender el proceso de la enfermedad y para participar en las decisiones respecto a su atención; en este sentido, pueden considerarse susceptibles de ser lastimados y heridos. La vulnerabilidad es condición humana inherente a su existencia en su finitud y fragilidad, de manera tal que no puede ser superada o eliminada. Los individuos y grupos en condición de vulnerabilidad específica deben ser protegidos y la integridad individual de cada uno debe ser respetada. (16)
8.5 PARTICIPACIÓN DE LOS COMITÉS HOSPITALARIOS DE BIOÉTICA.
Los Comités Hospitalarios de Bioética (CHB) tienen la atribución de emitir recomendaciones no vinculantes, a los involucrados en la relación médico-paciente respecto de casos clínicos difíciles que involucran problemas o Dilemas Bioéticos en Cuidados Paliativos en pacientes pediátricos.
Los CHB deliberarán los casos clínicos que les sean solicitados desde una perspectiva laica, y emitirán recomendaciones como apoyo a la toma de decisiones de los profesionales de la salud, a través del cumplimiento de sus atribuciones.
Los criterios para su integración y funcionamiento son emitidos por la Secretaría de Salud, a través de la Comisión Nacional de Bioética; se deberá tomar como referencia las Disposiciones para la Integración y Funcionamiento de Comités Hospitalarios de Bioética y su Guía.
8.6 INVESTIGACIÓN EN POBLACIÓN PEDIÁTRICA QUE RECIBE CUIDADOS PALIATIVOS.
La investigación contribuye a generar conocimiento -técnico, científico, médico, psicológico, etc.- que promoverá la mejora en el abordaje diagnóstico y terapéutico; sin embargo, cuando se trata de investigación en niños, los mecanismos regulatorios y las medidas de seguridad puede tener el efecto contrario al deseado, por lo que en ocasiones estos grupos de edad son excluidos de la investigación, lo que conlleva al uso de tratamientos o medidas terapéuticas no probadas y a extrapolar los resultados derivados de la investigación en adultos, trayendo consecuencias o resultados no óptimos en la población pediátrica. Para evitarlo, es necesario asegurar la representatividad de este sector de la población y establecer medidas de protección adecuadas a sus necesidades.
En este sentido, es importante que los niños tengan acceso a los beneficios derivados de avances científicos y tecnológicos, mediante el uso de intervenciones seguras y eficaces, en apego a los principios bioéticos antes mencionados.
Se deben generar protocolos inclusivos, vigilando la integridad ética y científica, el respeto a la dignidad de los participantes y a la protección de sus derechos. Toda investigación científica que pretenda incluir niños debe contar con rigor metodológico, con las fases previas ya superadas y con justificación de su aplicación.
Particularmente en la investigación en población pediátrica en cuidados paliativos, el equipo de investigación y seguimiento debe estar atento a detectar y atender oportunamente cualquier tipo de complicación, con el objetivo de no provocar mayor sufrimiento al participante. La investigación se debe desarrollar en un ambiente de transparencia y confianza.
En respeto al principio de autonomía, para quienes no cuenten con capacidad jurídica en los procesos de toma de decisiones, dependiendo la edad y capacidad cognoscitiva, se deberá considerar el asentimiento informado, sin que esto exima la firma del consentimiento informado por parte de los padres o los tutores. Este proceso conlleva el entendimiento de que todo acto médico o de investigación puede tener efectos indeseables e inesperados, y asume que se está corriendo un riesgo razonable con la expectativa de obtener un probable beneficio y que está en libertad de rechazar en cualquier momento el procedimiento o tratamiento
experimental y declinar su participación en la investigación.
Tanto el participante como sus familiares deben ser tratados con respeto, tienen derecho a estar informados, con veracidad, empatía, información suficiente, lenguaje claro e incluyente -adecuado al nivel de escolaridad y contexto cultural-, asegurando el correcto entendimiento y evitando tecnicismos incomprensibles para el usuario y su representante legal.
Aquí entra el papel de los Comités de Ética en Investigación, figura que tiene por función verificar el cumplimiento de los más altos estándares éticos que garanticen el respeto a los derechos humanos y que el protocolo implique el riesgo mínimo para el sujeto de investigación. (17)
8.7 PARTICIPACIÓN DE LOS COMITÉS DE ÉTICA EN INVESTIGACIÓN.
Los Comités de Ética en Investigación tienen la atribución de revisar protocolos de investigación en seres humanos y salvaguardar la dignidad, derechos y seguridad de los involucrados en el proceso, enfatizando su protección.
La inclusión de los aspectos éticos en los protocolos es un indicador de calidad, equiparable al rigor metodológico de una investigación científica y al tratarse pacientes pediátricos debe tener un beneficio directo en el menor o será el único tratamiento disponible para el tratamiento de su enfermedad.
También deberá asegurarse de que los resultados de la investigación que se pretende llevar a cabo en niños no podrían obtenerse con la participación de adultos.
Los criterios para su integración y funcionamiento son emitidos por la Secretaría de Salud, a través de la Comisión Nacional de Bioética; se deberá tomar como referencia las Disposiciones para la Integración y Funcionamiento de Comités de Ética en Investigación y su Guía.
BIBLIOGRAFÍA.
1. Tealdi JC. Diccionario latinoamericano de bioética [Internet]. Vol. 53, Red Latinoamericana y del Caribe de Bioética. Colombia; 2008. Available from: https://www.salud.gob.ec/wp-content/uploads/2016/12/8.-Diccionario-latinoamericano-de-Bioética-UNESCO.pdf
2. Jonsen AR. La toma de decisiones éticas en la medicina clínica, en La Casuística. Una metodología para la ética aplicada. Hall R, Arellano JS, editors. Santiago de Querétaro; 2012. 20-41 p.
3. Strong C. La Casuística en La Casuística: Una metodología para la ética aplicada. Hall R, Arellano JS, editors. Santiago de Querétaro; 2012. 42-49 p.
4. Jonsen AR. Razonamiento casuístico en la ética médica. Dilemata [Internet]. 2016 Jan 30 [cited 2021 Sep 10];8(20):1-14. Available from:
https://www.dilemata.net/revista/index.php/dilemata/article/view/419
5. Valdés E. Haciendo más práctico el principialismo: la importancia de la especificación en bioética. Rev Bioética y Derecho [Internet]. 2015 [cited 2021 Sep 10];(35):65-78. Available from: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S1886-58872015000300007&lng=es&nrm=iso&tlng=es
6. Quintana T. El "principialismo" y la bioética [Internet]. Bioética desde Asturias. 2012 [cited 2021 Sep 10]. Available from: https://www.bioeticadesdeasturias.com/el-principialismo-y-la-bioetica/
7. Pose C, Gracia D. 07 Procedimiento o método de toma de decisiones en Título de Expertos en Ética Médica. In: Título de Expertos en Ética Médica [Internet]. [cited 2021 Sep 15]. Available from: https://www.ffomc.org/CursosCampus/Experto_Etica_Medica/U7_Procedimiento o metodo de toma de decisiones.pdf
8. Beauchamp T, Childress J. No Maleficencia. In: Principios De Ética Biomédica. 1°. Barcelona, España: Masson; 2002. p. 179.
9. Casanueva L. Aplicación de los cuidados paliativos en la unidad de cuidados intensivos pediátricos. En: Gómez Sancho, Cuidados Paliativos: atención integral a enfermos terminales. 1998.
10. Casanueva L, López PR, Díaz JIS, Casado MVR. Cuidados al final de la vida en la unidad de cuidados intensivos pediátrica. Revisión de la bibliografía. 2005;63(2):152-9.
11. Fanaroff J, McIntosh N. Ética. La cesación o suspensión del tratamiento médico vital. In: Neonatología: Lo esencial en un Vistazo. 2014. p. 354.
12. Lantos JD, Meadow WL. Bioética neonatal: los desafíos morales de la innovación médica. 1st ed. SIBEN; 2006. 91 p.
13. Cámara De Diputados del H. Congreso De La, Unión. Ley General de Salud. Artículo 166 bis. México: Cámara De Diputados del H. Congreso De La Unión Secretaría General; Jun 1, 2021 p. 74-5.
14. Chuck-Sepulveda JA. Bioética y el paciente pediátrico oncológico. Rev Médico-Científica la Secr Salud Jalisco. 2019;6:131-4.
15. Bátiz Cantera J. Mientras Llega la Muerte (Reflexiones en torno al final de la vida). Fundación San Juan de Dios, editor. Madrid; 2021. 172-173 p.
16. Arruda De Morais TC, Sadi Monteiro P. Los conceptos de vulnerabilidad humana y la Integridad individual para la bioética. Rev bioét [Internet]. 2017 [cited 2021 Sep 15];25(2):311-20. Available from: http://dx.doi.org/10.1590/1983-80422017252191
17. Cámara de diputados del H. Congreso de la Unión. Reglamento de la Ley General de Salud en Materia de Investigación para la Salud [Internet]. Diario Oficial de la Federación. México; 2014. Available from: http://www.cofepris.gob.mx/MJ/Paginas/Reglamentos.aspx
Bibliografía adicional.
· Beauchamp LT, Childress FO. Principios de Ética Biomédica. 1ª. Ed, Masson, Barcelona 2002; pp 200-44
· Garduño EA, Véliz PRA. El interés superior de la infancia. Un derecho que marca un nuevo paradigma en la toma de decisiones en pediatría. Rev Mex Pediatr 2017; 84: 173
· Garduño EA, editor. Guía Práctica de Cuidados Paliativos en Pediatría. 1ª. Ed Corinter, México 2019.
· Hall TR, Arellano JS, coordinadores. La Casuística. Una metodología para la Ética Aplicada. unidadbioetica.com<libros 2012-2013
· Jonsen AR. La toma de decisiones éticas en la medicina clínica, en: Hall TR, Arellano JS. Coordinadores. La Casuística. Una metodología para la ética aplicada. unidadbioetica.com<libros, pp: 20, 2012-2013
· Strong C. La Casuística, en: Hall TR, Arellano JS, coordinadores. La Casuística. Una metodología para la ética aplicada. unidadbioetica.com<libros, pp: 43, 2012-2013
· Jonsen ARE. Razonamiento casuístico en la ética médica. Dilemata 2016; 8: 1-14
· Acuerdo por el que se emiten las Disposiciones Generales para la Integración y Funcionamiento de los Comités Hospitalarios de Bioética y se establecen las unidades hospitalarias que deben contar con ellos, de conformidad con los criterios establecidos por la Comisión Nacional de Bioética, publicado en el Diario oficial de la Federación el 31 de octubre de 2012.
· Acuerdo por el que se emiten las Disposiciones Generales para la Integración y Funcionamiento de los Comités de Ética en Investigación y se establecen las unidades hospitalarias que deben contar con ellos, de conformidad con los criterios establecidos por la Comisión Nacional de Bioética, publicado en el Diario Oficial de la Federación el 31 de octubre de 2012.
· Acuerdo por el que se reforma y adiciona el diverso por el que se emiten las Disposiciones Generales para la Integración y Funcionamiento de los Comités de Ética en Investigación y se establecen las unidades hospitalarias que deben contar con ellos, de conformidad con los criterios establecidos por la Comisión Nacional de Bioética, publicado el 31 de octubre de 2012, publicado en el Diario Oficial de la Federación el 11 de enero de 2016.
· Acuerdo por el que se modifica el diverso por el que se emiten las Disposiciones Generales para la Integración y Funcionamiento de los Comités de Ética en Investigación y se establecen las unidades hospitalarias que deben contar con ellos, de conformidad con los criterios establecidos por la Comisión Nacional de Bioética, publicado el 31 de octubre de 2012, publicado en el Diario Oficial de la Federación el 10 de diciembre de 2020.
CAPÍTULO 9
COMPETENCIAS PARA LA PROVISIÓN DE CUIDADOS PALIATIVOS PEDIÁTRICOS
9.1 ¿QUE SE NECESITA SABER PARA LA PROVISIÓN DE CUIDADOS PALIATIVOS PEDIÁTRICOS (CPP)?
Es fundamental entender que la filosofía paliativa y consideraciones éticas de la atención en adultos, no puede, ni debe, aplicarse textualmente a la atención pediátrica, ya que el contexto y necesidades para esta población son únicas y diferentes para cada periodo del desarrollo, que incluye desde la etapa prenatal hasta la adolescencia.
Apreciar y comprender el amplio espectro de las diferentes necesidades del cuerpo, mente y espíritu desde la gestación hasta la adolescencia (como periodo de transición a la vida adulta) es de suma importancia para poder proveer adecuados CPP.
En este contexto, se considera la atención de CPP desde la etapa prenatal, lactantes, preescolares, niños, hasta adolescentes y jóvenes adultos. (población AYA, (1) así como la definición de competencias al conjunto de "atributos personales y aptitud demostrada para aplicar conocimientos, habilidades y destrezas". Es decir, las competencias son la "capacidad de resolver problemas en un determinado contexto", (2) y se establece que, para proporcionar dichos cuidados, se requiere definir:
· ¿Qué significa la palabra paliativo?;
· ¿Quién tiene que otorgar los cuidados paliativos desde la etapa prenatal hasta la adolescencia y jóvenes adultos?;
· ¿Cuáles son las responsabilidades del proveedor que brinda los CPP?; y
· ¿Cuáles son las competencias nucleares, generales, específicas, y de especialidad que se requieren para proveer CPP de acuerdo con el nivel de complejidad del paciente?
Bajo este marco se integró el presente capítulo.
9.2 PROPÓSITOS
· Describir las competencias nucleares, generales, específicas y de especialidad de los profesionales de la salud para la provisión de atención paliativa, de conformidad al perfil profesional, nivel de atención y complejidad de la intervención educativa a realizar;
· Contribuir a la adquisición y fortalecimiento de las competencias individuales y colectivas para la atención paliativa en el neonato, niño y adolescente (NNA) a partir de la definición de intervenciones educativas específicas, y estándares e indicadores para su evaluación; y
· Contribuir al desarrollo de programas académicos, de acreditación y certificación en esta materia.
9.3 DIRIGIDO A:
Profesionales de la salud
· Personal médico general y especialista, que otorgue atención paliativa;
· Personal de enfermería técnico, general, especialista y postécnicos;
· Personal de salud mental psicología y psiquiatría con enfoque en atención pediátrica;
· Personal de nutrición y rehabilitación que atiendan pacientes con necesidades paliativas;
· Personal de trabajo social;
· Otras áreas médicas y equipos de salud que atienden ocasionalmente necesidades paliativas desde la etapa prenatal hasta la adolescencia y jóvenes adultos; y
· Terapeutas de medicina complementaria: acupuntura, arteterapia, musicoterapia, terapia ocupacional y áreas afines que atienden población con necesidades paliativas.
Otras personas involucradas en el CPP
· Padres y otros integrantes del núcleo familiar;
· Comunidad;
· Voluntariado; y
· Personal de soporte espiritual.
Organizaciones
· Gubernamentales (tomadores de decisiones, legisladores, gestores);
· Sanitarias: Individuales, de los equipos de Atención Primaria a la Salud, establecimientos de atención médica y unidades de cuidados paliativos en los tres niveles de atención;
· Organizaciones de la sociedad civil;
· Instituciones educativas;
· Organizaciones religiosas; y
· Todas aquellas instituciones u organizaciones que tengan que ver con la atención en CPP.
9.4 ESCENARIOS POSIBLES PARA LA ATENCION PALIATIVA
· Domicilio;
· Escuela;
· Espacios recreativos;
· Establecimiento de atención médica: Consulta externa, corta estancia, hospitalización, urgencias, cuidados intensivos;
· Casas hogar;
· Comunidad; y
· Cualquier sitio donde el niño, niña y adolescente se desarrolle.
9.5 NIVEL DE COMPLEJIDAD
Las competencias necesarias para brindar cuidados paliativos variarán de acuerdo con el grado de complejidad de las necesidades paliativas que se requiera atender, centrado en la persona (desde la etapa prenatal hasta los adolescentes y jóvenes adultos) tomando en cuenta el contexto individual de evolución de la condición que limita o amenaza la vida, y características de cada familia.
El abordaje del NNA, su familia y necesidades requiere estar centrado en la persona, considerando las múltiples y complejas dimensiones que constituyen al ser humano, en los planos físico, psicológico, social y espiritual.
A mayor grado de complejidad será necesario desarrollar un mayor número de competencias en cada uno de los miembros del equipo de salud para lograr satisfacer sus necesidades.
Las necesidades paliativas pediátricas deberán de ser evaluadas desde una visión multidimensional al incluir los aspectos físicos, emocionales, sociales y espirituales del niño, niña, adolescente y su familia. Si quienes proveen cuidados paliativos pediátricos no cuentan con las competencias necesarias para solventar dichas necesidades o el contexto particular del caso no lo permite, será responsabilidad del profesional y el sistema de salud referir a un nivel de atención de mayor especialización que cuente con las competencias necesarias para su óptima atención.
El nivel de complejidad se determinará de acuerdo con la dificultad para la atención clínica, control de variables psicosociales y espirituales, problema para toma de decisiones, incertidumbre en el resultado del tratamiento, el pronóstico o evolución natural de la enfermedad, recursos y redes de apoyo disponibles, interacción de otras determinantes de la salud y en el grado adecuado de intensidad del tratamiento a ofrecerse. (3, (Modificado de Codornuy-Tuca).
9.6 COMPETENCIAS
Una competencia es un constructo multidimensional que favorece la capacidad de un buen desempeño en contextos complejos y auténticos. Se basa en la integración y activación de conocimientos, habilidades, destrezas, actitudes y valores; incluye distintos niveles como saber (datos, conceptos, conocimientos), saber hacer (habilidades, destrezas, métodos de actuación), saber ser (actitudes y valores que guían el comportamiento) y saber estar (capacidades relacionadas con la comunicación interpersonal y el trabajo cooperativo).
De acuerdo con lo mencionado, la interacción entre competencia y complejidad de provisión de atención permite sistematizarlas en 4 áreas: Nucleares, Generales, Específicas y Especializadas.
Las competencias nucleares aplican para toda persona que brinde atención a población pediátrica con enfermedades o condiciones que limiten o amenacen su vida, así como atención a sus familiares. Se enfocan en los fundamentos de los cuidados paliativos para asegurar un abordaje básico de calidad con un enfoque integral. Estas estrategias y acciones pueden ser brindadas por familiares, voluntarios, comunidad y todos los equipos de salud. Forman parte del conocimiento básico de todos los proveedores de atención en salud
Las competencias generales serán determinadas de acuerdo con el perfil de quien brinda los cuidados paliativos pediátricos incluyendo profesionales de la salud (medicina, enfermería, rehabilitación, nutrición, psicología y trabajo social), organizaciones de la sociedad civil, voluntariado y terapeutas de medicina complementaria que colaboren sistemáticamente con equipos de atención pediátrica. Son competencias recomendables de atención para todo el personal de salud.
Las competencias específicas aplicaran a todo personal de salud (médicos, enfermeras, psicólogos, trabajadoras sociales, nutriólogos, rehabilitadores, entre otros) que brinden atención en áreas pediátricas y de cuidados paliativos tanto en contexto hospitalario como en atención domiciliaria y/o comunitaria. Estas estarán enfocadas en control de síntomas en las cuatro esferas de la atención a los niños, niñas, adolescentes: física, social, psicológica y espiritual promoviendo la incorporación del enfoque paliativo en cada una de sus prácticas profesionales en sus áreas de trabajo.
Las competencias especializadas están dirigidas a especialistas en cuidados paliativos pediátricos, que brinden cuidados de alta complejidad clínica, asistencial y/o social. Se trata de equipos de alto desempeño en atención paliativa pediátrica.
La adquisición y desarrollo de estas competencias será de manera progresiva, de tal manera que el proveedor de los CPP pueda brindar la mejor atención según las necesidades del niño, niña, adolescente y adulto joven, del nivel de atención y de la complejidad de las necesidades paliativas.
De manera general los elementos para cada uno de los grupos de competencias son: (5, 6, 7, 8, 9)
| COMPETENCIAS NUCLEARES | COMPETENCIAS GENERALES |
| Proveer atención centrada en la persona y su familia (Meta 2030); Identificar la necesidad de atención con un enfoque paliativo; Colaborar en equipos interprofesionales; Identificar necesidades de atención; Emplear la practica medica basada en evidencias; Aplicar la mejoría en la calidad; Interés es su formación profesional y capacitación continua; Conformar estructura operativa en el entorno local ; Integrar redes locales de atención; | Conocer las diferentes etapas de desarrollo del niño, niña y adolescente; Atención y orientación básica en control de síntomas; Mantener el enfoque de aliviar el sufrimiento y mejorar las condiciones de vida a lo largo del proceso de enfermedad desde el diagnostico, a lo largo de la evolución incluyendo la fase final de vida; Competencias para comunicación eficaz, manejo de conflicto, negociación, trabajo en equipo, liderazgo, toma de decisiones informadas; Comprender y facilitar el proceso de duelo. |
| COMPETENCIAS ESPECÍFICAS CUIDADOS PALIATIVOS | COMPETENCIAS ESPECIFICAS CUIDADOS PALIATIVOS PEDIÁTRICOS |
| Toma de decisiones informadas, basadas en la mejor evidencia disponible; Colocación y uso de dispositivo subcutáneo y su aspecto farmacológico; Orientación a la persona y al servicio; Desarrollo de talento humano; Distintas vías de administración de medicamentos (intravenosa, subcutánea, oral, sublingual, rectal y tópica); Prevención y cuidado de lesiones cutáneas y manejo de estomas; Soporte emocional y social inicial del niño, niña, adolescente y su familia; Apoyo inicial durante el duelo; | Identificación de necesidades de atención paliativa y medidas de atención; Atención Paliativa en Pediatría: Domiciliaria, ambulatoria y hospitalaria; Plan de cuidados paliativos pediátricos con estrategia multimodal; Adecuación de esfuerzo terapéutico y planificación avanzada; Práctica profesional y ética en los cuidados paliativos pediátricos; Control sintomático paliativo en pediatría; Manejo de opioides; Conocimiento básico de deontología médica y legislación pediátrica. |
| COMPETENCIAS DE ALTA ESPECIALIDAD | |
| Manejo analgésico avanzado y uso adecuado de opioides (rotación, destete); Control multimodal de síntomas; Manejo integral en casos con necesidades complejas; Contingencia, intervención en crisis, liderazgo y gestión; Atención a poblaciones N, N y A vulnerables; Cuidados al final de la vida; y Bioética, deontología médica y legislación vigente. | |
9.7 FORMADOR DE FORMADORES.
Una de las competencias clave desde el nivel nuclear hasta de alta especialidad es continuar educando sobre alivio del sufrimiento, mejorar condiciones de vida y cuidados paliativos pediátricos. Tanto la comunidad, los voluntarios como los profesionales de la salud reconocidos por sus pares como "educacionalmente influyentes" tienen un papel fundamental para que el conocimiento paliativo sensibilice, difunda, crezca y se fortalezca en la sociedad.
Es importante formar líderes de capacitación y promover agentes de cambio que puedan participar en los diferentes niveles de atención y escenarios donde se den los cuidados paliativos pediátricos. Es indispensable promover la docencia e investigación en todas las áreas desde la atención hasta la gestión de políticas en salud.
Un elemento que determina el avance o ralentización de la provisión de CP es la educación; es indispensable el apoyo de equipos pedagógicos que coordinen el diseño e implementación de la intervención educativa, a partir de la identificación de necesidades específicas para implementar, incorporar y fortalecer la formación de los equipos de salud.
9.8 METAS
1. Elaborar un Programa Educativo (Planeación);
2. Operacionalizar una Intervención Educativa (Ejecución);.
3. Desarrollar un instrumento para la evaluación del proceso educativo (Información y Control);
4. Preparar un programa de mantenimiento y desarrollo de contenidos; y
5. Seguimiento y medición de impacto de los programas aplicados.
9.9 ESTRATEGIA
1. Integrar un equipo de trabajo para desarrollar la intervención educativa:
· Identificación de necesidades de capacitación;
· Seleccionar escenarios a intervenir;
· Definir modalidad educativa;
· Identificar líderes de opinión;
· Seleccionar personal docente;
· Diseñar programa académico teórico-práctico;
· Integrar sistema de evaluación y seguimiento; y
· Elaborar material didáctico y contenidos específicos.
2. Diseñar intervenciones educativas esencialmente participativas que faciliten el aprendizaje significativo para lograr una práctica efectiva en el otorgamiento de cuidados paliativos pediátricos,
3. Implementar la intervención educativa de manera piloto, evaluar resultados de aprendizaje, ajustar-rediseñar-cambiar para ampliar cobertura de capacitación y
4. Establecer indicadores y plan de mejora continua.
9.10 FORMAS DE INTERVENCIÓN: INTERVENCIÓN EDUCATIVA SINÉRGICA
En las iniciativas de mejora en la atención médica, las intervenciones requieren ser individualizadas y vinculadas a la disposición al cambio del educando, para reducir la resistencia, el estrés, el tiempo para implementarlas y acelerar el movimiento hacia la etapa de acción.
Asociado al proceso educativo y de capacitación establecido se recomienda integrar otras intervenciones que faciliten el cambio de paradigma de atención tradicional a un enfoque centrado en las necesidades del paciente.
Entre estas iniciativas se recomiendan:
Visita personalizada: Apoyo de un experto, entrenado en cuidados paliativos, y comunicación educativa, al personal de salud en su propio ambiente de trabajo.
Discusión en pequeños grupos: es un método efectivo para introducir nuevos temas, facilita una experiencia intelectual y social que estimula el pensamiento reflexivo y la solución participativa de problemas en un ambiente amigable. Una discusión exitosa motiva a los participantes a buscar información adicional sobre ideas no consideradas que pueden tener impacto en su práctica.
Aprendizaje basado en problemas: es un método que genera un contexto donde los participantes adquieren las habilidades para identificar el problema y encontrar una solución con fundamento en la mejor evidencia disponible. Favorece el desarrollo para el trabajo en equipo, analiza y sintetiza la información, diagnóstica las necesidades propias de aprendizaje y facilita el compromiso con el aprendizaje auto dirigido.
Auditoria y retroalimentación: cualquier resumen de desempeño en la atención otorgada en un periodo específico. El resumen puede incluir recomendaciones para la mejora de la atención o de las intervenciones.
BIBLIOGRAFÍA
1. Adolescentes y adultos jóvenes con cáncer (AYA): una población huérfana. White PH, Cooley WC. Supporting the Health Care Transition From Adolescence to Adulthood in the Medical Home FROM THE AMERICAN ACADEMY OF PEDIATRICS Guidance for the Clinician in Rendering Pediatric Care [Internet]. Vol. 142, PEDIATRICS. 2018. Disponible en: www.aappublications.org/news
2. Informe UNE 66173 IN, Octubre 2003 "Los recursos humanos en un sistema de gestión de calidad. Gestión de las competencias. Documento Internet, 22 pp. Disponible en :
https://qualitasbiblo.files.wordpress.com/2013/01/une-66173-2003-gestic3b3n-de-las-competencias.pdf
3. Complejidad asistencial en la atención al final de la vida: criterios y niveles de intervención en atención comunitaria de salud Med Paliat. 2015;22(2):69-80
https://www.elsevier.es/es-revista-medicina-paliativa-337-pdf-S1134248X13000852
4. Codorniu N, Tuca A. Complexity levels of interventions in a hospital support team: descriptive study about prevalence, clinical characteristics and team organization for each level. 3rd European Association for Palliative Care Research Congress - Stresa, Italy, June 2004. EAPC Abstracts. Palliat Med. 2004;18:309-93.
5. Chirino-Barceló Yazmín Amelia, Gamboa-Marrufo José Domingo. Cuidados paliativos en pediatría. Bol. Med. Hosp. Infant. Mex. [revista en la Internet]. 2010 Jun [citado 2021 Oct 13] ; 67( 3 ): 270-280. Disponible en:
http://www.scielo.org.mx/scielo.php?script=sci_arttext&pid=S1665-11462010000300010&lng=es.
6. Competencias en Cuidados Paliativos: Nivel básico" (2008) Documento en Internet 75 pp. Disponible en:
http://www.ffis.es/ups/Manual%20Competencias%20en%20Cuidados%20Paliativos.pdf
7. Competencias en Medicina Paliativa Pediátrica. Documento Internet, 27 pp. Disponible en :
https://www.sap.org.ar/docs/profesionales/CEP/COMPETENCIAS%20EN%20MEDICINA%20PALIATIVA%20PEDIATRICA.pdf
8. G. Benavides Fernando, Moya Carmela, Segura Andreu, Puente M. Lluïsa de la, Porta Miquel, Amela Carmen. Las competencias profesionales en Salud Pública. Gac Sanit [Internet]. 2006 Jun [citado 2021 Oct 13] ; 20( 3 ): 239-243. Disponible en: http://scielo.isciii.es/scielo.php?script=sci_arttext&pid=S0213-91112006000300011&lng=es.
9. Perfil y competencias en salud. Perspectiva de los profesionales , un aporte al cuidado de la salud, las personas, familias y comunidades. MINSALUD, Colombia (2016). Academia Nacional de Medicina. Documento en internet 337 pp. Disponible en :
https://www.observatoriorh.org/sites/default/files/perfiles_profesionales_salud.pdf
10. Real Academia Española. Diccionario. Página Web disponible en: https://dle.rae.es/actitud
11. Agentes de cambio. Sitio Web "Acercando el IMSS al ciudadano". Página Web. Disponible en:
https://www.imss.gob.mx/SERIMSS/agente-cambio
12. Tipo de conocimientos. Centro Europeo de posgrado (CEUPE) México. Página Web. Disponible en :
https://www.ceupe.mx/blog/tipos-de-conocimientos.html
13. Eliot Levine & Susan Patrick. What is Competency-Based-Education. An updated definition. Aurora Institute. Documento en internet 14 pp. Disponible en:
https://aurora-institute.org/wp-content/uploads/what-is-competency-based-education-an-updated-definition-web.pdf
14. Real Academia Española. Diccionario. Página Web disponible en : https://dle.rae.es/comprensi%C3%B3n
15. Real Academia Española. Diccionario. Página Web disponible en: https://dle.rae.es/habilidad
16. Real Academia Española. Diccionario. Página Web disponible en : https://dle.rae.es/gu%C3%ADa
17. DeConceptos.com Página Web https://deconceptos.com/ciencias-sociales/recomendacion
GLOSARIO
Actitud: Disposición a realizar una acción o comportamiento, forma de reaccionar y resolver problemas.
Agente de cambio: Persona proactiva capaz de desarrollar acciones, actitudes y procesos para fortalecer los aspectos internos y externos de una organización.
Autorregulación: Se entiende por autorregulación al control que una persona ejerce sobre sus emociones, sus acciones y sus pensamientos. Este proceso contribuye a que el individuo pueda cumplir con sus objetivos.
Intervención educativa: Programa o grupo de pasos específicos para ayudar a desarrollar áreas necesarias en un proyecto.
Bioética: Rama de la ética aplicada que reflexiona, delibera y hace planteamientos normativos y de políticas públicas, para regular y resolver conflictos en la vida social, especialmente en las ciencias de la vida, así como en la práctica y en la investigación médica, que afecten la vida en el planeta, tanto en la actualidad como en futuras generaciones.
Clínica del dolor y Cuidados Paliativos: Institución organizada con espacio y personal dedicado a valorar y tratar la interacción de los aspectos físicos, emocionales, espirituales y sociales de pacientes con enfermedades potencialmente mortales.
Comités Hospitalarios de Bioética: Son espacios de reflexión, análisis, orientación y educación acerca de los dilemas que surgen en la atención médica. Se conforman como órganos interdisciplinarios y plurales, que en ningún caso pueden sustituir la responsabilidad de los médicos hacia los pacientes ni imponerse a sus decisiones, sino que su carácter es únicamente consultivo.
Comité de Ética en Investigación: Órganos colegiados, autónomos, institucionales, multidisciplinarios, plurales y de carácter consultivo, cuya finalidad principal es la de proteger los derechos, dignidad y bienestar de los sujetos que participen en investigaciones en salud, a través de la evaluación, dictaminación y seguimiento a las investigaciones puestas a su consideración.
Conocimiento: Es un concepto complejo. Se refiere al proceso mediante el cual la realidad es reflejada y reproducida en el pensamiento humano. Es producto de distinto tipo de experiencias, razonamientos y aprendizajes.
Contención emocional: Es un conjunto de procedimientos básicos que tienen como objetivo tranquilizar y estimular la confianza de una persona que se encuentra afectada por una fuerte crisis emocional.
Competencia: Conjunto de comportamientos socioafectivos, habilidades, destrezas y aptitudes cognoscitivas, psicológicas, sensoriales y motoras que permiten llevar a cabo adecuadamente un desempeño, una función, una actividad o una tarea.
Competencia clave: Enunciado que define aquello que la ocupación o área bajo análisis permite alcanzar o lograr para que el desempeño laboral resulte altamente efectivo y responda a lineamientos técnicos y normativos que garanticen un nivel mínimo aceptable de calidad y eficiencia.
Comprensión: Facultad, capacidad o perspicacia para entender las cosas, por medio de la razón de la naturaleza, cualidades y relaciones de las cosas.
Comunicación. Herramienta terapéutica esencial que da acceso al principio de autonomía, al consentimiento informado, a la confianza mutua, a la seguridad y a la información que el paciente necesita para ser ayudado y ayudarse a sí mismo. También permite la imprescindible coordinación entre el equipo cuidador, la familia y el paciente.
Comunicación colaborativa. La comunicación colaborativa se refiere tanto al intercambio de información como a la naturaleza de la relación de colaboración entre las personas que se comunican, enfatizando las relaciones entre las personas, viendo la comunicación interpersonal y las relaciones como inexorablemente entrelazadas. (4)
Comunicación eficaz. La comunicación es eficaz cuando el mensaje deseado se transmite, se recibe y se entiende de la misma manera por todas las partes implicadas y es un proceso bidireccional entre dos o más personas mediante el cual se comparten información y sentimientos a través de un intercambio de mensajes verbales y no verbales.
Comunicación no verbal. La transmisión de mensajes sin el uso de palabras (por ejemplo, mediante gestos, el uso del espacio). Uno de los dos principales sistemas de códigos de comunicación; a veces se define como todo lo que no es el lenguaje; se comunica a través de canales distintos de las palabras. Cualquier información que se expresa sin palabras.
Comunicación verbal. Uno de los dos principales sistemas de códigos de comunicación; asociado a nuestro lenguaje hablado y escrito; típicamente etiquetado como "lenguaje". (La transmisión de mensajes mediante palabras, ya sean escritas o habladas).
Conspiración del silencio. Acuerdo implícito o explícito por parte de los familiares, amigos y/o profesionales, de alterar la información que se le da al paciente con el fin de ocultarle el diagnóstico y/o pronóstico y/o gravedad de la situación.
Couselling: Conjunto de habilidades terapéuticas que facilitan la relación de ayuda puntual hacia el enfermo o familiar, y que define lo que llamamos «apoyo emocional.
Cuidados Paliativos Pediátricos: La definición de cuidados paliativos de la OMS (adaptada para pediatría) dice que éstos constituyen "un enfoque que mejora la calidad de vida de los pacientes y familias que afrontan una enfermedad que amenaza la vida de un niño, a través de la prevención y alivio del sufrimiento". Para ello se requiere de "la identificación temprana, la evaluación precisa, y el tratamiento adecuado del dolor y otros problemas físicos, psicosociales, y espirituales".
Criterio de desempeño: Es un resultado y enunciado evaluativo, con base en un aspecto crítico o relevante de la función, que demuestra el desempeño del profesional y por lo tanto su competencia.
Elementos de competencia: Componente de la unidad de competencia. Lo que la persona debe ser capaz de hacer.
Equipo Interdisciplinario: Grupo de profesionales que trabaja en un área común de forma independiente y que interactúan entre sí de manera formal, intercambiando información sistemáticamente, comparten una metodología de trabajo y tienen objetivos comunes al desarrollar una planificación centrada en el paciente.
Escucha activa. Proceso de análisis y evaluación de lo que dice otra persona en un esfuerzo por comprender los sentimientos del hablante o el verdadero significado del mensaje.
Espiritualidad: Es una aspiración y una actitud profundamente arraigadas en el ser humano, y profundamente íntimas: pertenece al dominio interior, a la conciencia o percepción de uno mismo en el universo y su relación con los demás, así como a su desarrollo en el camino de la existencia.
Guía: Tratado o documento que contiene preceptos o indicaciones para encaminar o dirigir un tema específico. (16)
Habilidad: Capacidad de ejecutar acciones en forma adecuada con destreza. (15)
Mala noticia. Una mala noticia es toda aquella que afecta de forma drástica, negativa y grave a la visión que un individuo tiene de su futuro. Toda mala noticia, por tanto, tiene graves consecuencias adversas para los pacientes y sus familias; el impacto es proporcional a su efecto en el cambio de las expectativas del paciente.
Es importante definir el elemento central de las malas noticias: es decir, tratar de identificar qué es lo que las hace tan malas para el paciente. En la mayoría de los casos esto es obvio, como el diagnóstico de una enfermedad grave que limita la vida y, en consecuencia, tener que enfrentarse a una vida limitada y/o a la pérdida de funciones y/o de calidad de vida.
Niveles de Atención Médica: Es una forma ordenada y estratificada de organizar los recursos para satisfacer las necesidades de la población. (26)
País de bajo ingreso: El banco mundial clasifica las economías del mundo en 4 grupos de ingreso; alto, mediano alto, mediano bajo y bajo, esta clasificación se basa en el ingreso nacional bruto per cápita en USD corrientes calculado usando el método de Atlas.
Pensamientos concretos: es un proceso cognitivo que se caracteriza por la descripción de los hechos y los objetos tangibles. Es el tipo de pensamiento que se encuentra ligado a los fenómenos del mundo real, es decir, a los objetos materiales. El pensamiento concreto nos permite generar conceptos generales sobre fenómenos particulares y categorizarlas de una manera lógica.
Preguntas existenciales: Las preguntas existenciales surgen de aquellas dudas nos hacemos en la búsqueda de nuestra conciencia y esencia. Son preguntas que muchas veces requieren un profundo trabajo de autorreflexión, y otras veces son preguntas que, como su nombre indica, tratan sobre nuestra existencia y los porqués de la vida.
Primer nivel de atención: Es el nivel más cercano a la población, o sea, el nivel del primer contacto, permite resolver las necesidades de atención básicas y más frecuentes, que puede ser resueltas por actividades de promoción a la salud, prevención de la enfermedad y por procedimientos de recuperación y rehabilitación; y actualmente paliación.
Recomendación: Sugerencia de una acción ventajosa o benéfica que mejora la calidad o aprecio.
Religión: La religión se refiere a un sistema de creencias estructuradas que tratan aspectos espirituales a menudo con un código de comportamiento ético y una filosofía. Como aspecto central a la mayoría de las religiones se encuentra la creencia en -y la vinculación con- un dios o ser supremo, así como la esperanza en una salvación.
Regulación emocional: La regulación emocional es el proceso a través del cual los individuos modulan sus emociones y modifican su comportamiento para alcanzar metas, adaptarse al contexto o promover el bienestar tanto individual como social.
Servicios básicos de salud: Son aquellas prestaciones que brindan asistencia sanitaria; puede decirse que la articulación de estos servicios constituye un sistema de atención orientado al mantenimiento, la restauración y la promoción de la salud de las personas.
Segundo nivel de atención: Se ubican los hospitales y establecimientos donde se prestan servicios relacionados a la atención en medicina interna, pediatría, gineco-obstetricia, cirugía general y psiquiatría. (27)
Tercer nivel de atención: Se reserva para la atención de problemas poco prevalentes, se refiere a la atención de patologías complejas que requieren procedimientos especializados y de alta tecnología. (27)
Trascendencia: La trascendencia es, pues, la capacidad de expandir el ser, traspasando la percepción limitada de la realidad que nos ofrecen nuestros sentidos y teniendo una perspectiva más profunda y amplia de nuestro yo y nuestras circunstancias presentes, incluidas el sufrimiento y la muerte, capacidad que se deriva del sentimiento de la presencia del Ser Superior o de pertenencia a un Todo que nos supera y abarca.
Unidad de competencia: Es un aspecto o un elemento discreto, entre varios, que puede ser descrito y desagregado en los elementos de competencia, que puede ser reconocido y certificado.
ANEXO
ENFOQUE DE COMPETENCIAS
Un profesional es competente cuando dispone de los conocimientos, habilidades y actitudes necesarias para ejercer la propia actividad laboral, resolviendo colaborativamente los diversos problemas que se presentan a fin de conseguir los objetivos que se plantean. (1)
En este sentido, el profesional de la salud y los equipos interdisciplinarios que ofrecen cuidados paliativos pediátricos requieren "saber actuar" para mejorar la calidad de vida y aliviar el sufrimiento asociado a la salud de las personas en edad pediátrica con condiciones limitantes o amenazantes para la vida y sus familias. Esto implica dinamizar las competencias personales y de grupo para aplicarlos en la acción práctica que el contexto específico le plantea con la finalidad mencionada. (2)
Una competencia es por tanto el conjunto de "atributos personales y (la) aptitud demostrada para aplicar conocimientos y habilidades", traduciéndose en la "capacidad de resolver problemas en un determinado contexto". (3)
De manera descriptiva, una competencia consta de:
· Los atributos personales son características que pertenecen al sujeto y pueden ser rasgos que se poseen desde el nacimiento o que fueron adquiridos por formación. Estos incluyen: talento, motivación, comunicación, capacidades cognitivas, valores, inteligencia emocional, conocimientos (saber) y habilidades (saber hacer);
· Las aptitudes demostradas son las conductas observables dentro de un entorno real y se dividen en destrezas y habilidades aplicadas;
· La capacidad para resolver problemas en cualquier contexto. Esto incluye la capacidad de atender situaciones inesperadas y anticipar futuras complicaciones o incertidumbres haciendo uso de las competencias requeridas, disponibles y potenciales.
Por tanto, adquirir, fomentar y/o desarrollar competencias profesionales implica en que atentos a las necesidades cambiantes del contexto (en este caso la provisión de CPP) se gestione el aprendizaje para no solo sumar saberes sino articularlos e integrarlos para la acción. Es necesario que la acción educativa se centre no en la enseñanza y la transmisión de información sino en que el profesional sea agente de su propio aprendizaje.
Figura 1 Ser cuidador en CPP requiere:
Fuente: Diseño propio Beatriz Elena Dorsey Rivera, octubre 2021
En el Cuidado Paliativo Pediátrico es importante considerar el desarrollo de competencias universales, ya que además del personal de salud, participan en esta provisión de cuidados, entre otros, personas voluntarias, padres y familiares del paciente, personas de la comunidad, por lo que se hace necesario considerar lo que se requiere y muestra en la Figura 1
Estrategias para el desarrollo de competencias
En las tablas 1 y 2, se describen los ejes para la integración de competencias y las etapas para la gestión de su implementación.
| Tabla 1 Ejes para la integración de un modelo basado en competencias | ||
| EJE | ACCIONES A REALIZAR | RESULTADO ESPERADO |
| Diseño de modelos educativos basado en competencias Reorientación de actividades y posicionamiento de las estructuras de educación medica Implementación de mecanismos de reconversión funcional y selección de educandos Diseño del modelo académico administrativo para la gestión por competencias Diseño del modelo académico administrativo para la gestión por competencias | DISEÑO DE MODELOS EDUCATIVOS BASADOS EN COMPETENCIA A. Definir el perfil basados en competencias B. Elaborar un catálogo de competencias por categorías de personal: a. nucleares b. generales c. específicas d. de especialidad C. Implantar los modelos educativos basados en competencia en: a. Formación b. Capacitación c. Educación Continua | A. Modelo para definir competencias del personal que otorga los cuidados paliativos pediátricos B. Catálogo para cada categoría de personal de salud, entre otros: médicos/enfermeras generales, especialistas, paliativistas, psicólogos, trabajadores sociales... C. Programas educativos para la formación, capacitación y educación continua basados en competencia |
| GESTION DE RECURSOS HUMANOS POR COMPETENCIA A. Diseño de procesos y procedimientos para el aprendizaje institucional B. Diseño de procesos y procedimientos para elevar el grado de competencia individual C. Desarrollo de indicadores para valorar el desempeño organizacional y el rendimiento individual D. Sistema para la selección, capacitación, evaluación del desempeño e incentivos E. Sistema de evaluación de competencias | A. Desarrollo de intervenciones educativas participativas B. Sistema de evaluación de la intervención educativa y C. Sistema de evaluación por competencias | |
| ESTRUCTURA DE LA EDUCACION CONTINUA A. Revisión de normatividad vigente B. Diseños de normas, lineamientos y procedimientos C. Definición de funciones y posición de los responsables de los cuidados paliativos pediátricos D. Establecer convenios interinstitucionales, intrasectoriales e intersectoriales E. Asignación de Recursos a. Personal b. Tecnológicos c. Financieros d. Materiales | A. Adecuación de las normas B. Posicionamiento del personal que otorga cuidados paliativos pediátricos C. Convenios institucionales para orientar la formación, la capacitación y la educación continua basada en competencias D. Gestión de recursos para la intervención educativa | |
| Tabla 2 Etapas para la gestión e implementación de un modelo basado en competencias | |||
| ETAPA | DIRIGIDA A : | ACTIVIDAD | PRÓPOSITO |
| GESTIÓN | Secretarios de Salud o Directores de los Servicios de Salud | 1. Comunicado oficial del proyecto 2. Envío de una carpeta con los siguientes documentos: >Proyecto >Estrategia Educativa 3. Reunión ejecutiva | >Comunicar intencionalidad y beneficios de la intervención >Solicitar apoyo a las actividades educativas |
| INDUCCIÓN A NIVEL ESTATAL | · Responsables de enseñanza, calidad, programas de formación, capacitación y educación permanente · Responsables de los cuidados paliativos | 1. Comunicado oficial del proyecto 2. Envío de una carpeta con los siguientes documentos: >Proyecto >Estrategia Educativa >herramientas educativas: boletines, guías, recomendaciones 3. Taller | >Desarrollar capacidades para emplear intervenciones educativas que promuevan el pensamiento crítico y la solución de problemas >Implantar y evaluar las estrategias educativas |
| INSTITUCIONALIZACIÓN INSTITUCIONALIZACIÓN | · Responsables de los cuidados paliativos · Responsables de servicios clínicos, paraclínicos y otros | 1. Comunicado oficial del proyecto de colaboración 2. Envío de una carpeta con los siguientes documentos: >Proyecto >Estrategia Educativa >herramientas educativas: boletines, guías, recomendaciones 3. Taller | >Desarrollar capacidades para emplear intervenciones educativas que promuevan el pensamiento crítico y la solución de problemas >Incorporar contenidos en programas operativos |
| · Personal de Salud que provee CPP · Personal en formación · Personal de equipos inter-profesionales | 1. Comunicado oficial del proyecto de colaboración 2. Envío de una carpeta con los siguientes documentos: >Proyecto >Estrategia Educativa >herramientas educativas: boletines, guías, recomendaciones 3. Taller | >Fortalecer las capacidades para mejorar el otorgamiento de cuidados paliativos en pediatría. | |
En la figura 2 se muestra un mapa, que presenta los elementos conceptuales para el desarrollo de competencias
Figura 2 Mapa conceptual: desarrollo de competencias
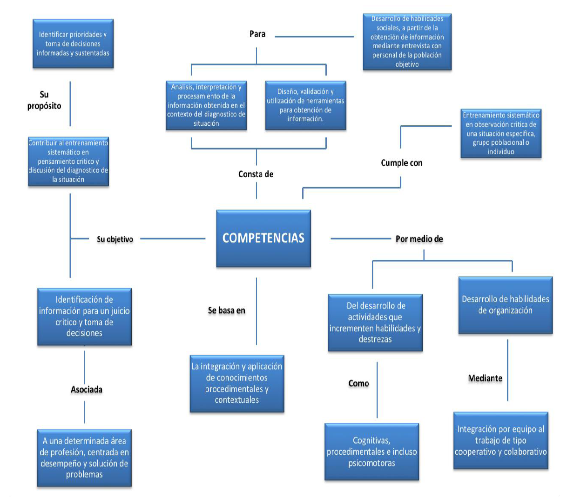
Fuente: Diseño propio Dávalos, M.L; Dorsey, B.E; Llamas, N; Osio, M; Ramos, J.A, Zúñiga, G. Octubre 2021
Al integrar estrategias para el desarrollo de competencias para la provisión del Cuidado Paliativo Pediátrico, RECORDAR:
| Los cuidados paliativos pediátricos son una forma de atención especializada, ofrecida por múltiples profesionales, para aquellos niños y sus familias que afrontan enfermedades graves y crónicas que amenazan seriamente la vida. Consisten en la asistencia activa y total del cuerpo, la mente y el espíritu del niño. Se centran en la prevención y el alivio de los síntomas, el dolor y el estrés, así como en el apoyo a los aspectos psicológicos, espirituales y sociales del paciente y su familia. Los cuidados paliativos pediátricos garantizan el respeto a su dignidad y el derecho a su autonomía, mediante una atención continuada e individualizada. Los objetivos son poder satisfacer las necesidades físicas y emocionales del niño y mantener el «funcionamiento» familiar con la mayor normalidad posible, incluyendo servicios de apoyo a los hermanos y soporte (tiempos de descanso) a la familia. (4) Los niños tienen que seguir siendo niños, aun en su enfermedad y requieren ellos y su familia estar acompañados por su "familia paliativa" para contribuir en mejorar su atención, su satisfacción y su experiencia. A lidiar con el estrés y la incertidumbre de las enfermedades agudas y crónicas, las lesiones, los traumas, las discapacidades, las pérdidas y el duelo. Proporcionan intervenciones basadas en la evidencia, apropiadas desde el punto de vista del desarrollo y psicológico, incluido el juego terapéutico, la preparación para los procedimientos y la educación para reducir el miedo, la ansiedad y el dolor. (5) |
1. Bunk, G. P. (1994). La transmisión de las competencias en la formación y perfeccionamiento de profesionales de la RFA. Revista Europea de Formación Profesional, 1 (8-14).; Echeverría, B. (2002). Gestión de la Competencia de Acción Profesional. Revista de Educación Educativa; 20 (1): 7- 43.
2. Martínez-Clares, P., Martínez-Juárez, M y Muñoz-Cantero, J.M. (2008). Formación basada en competencias en educación sanitaria: aproximaciones a enfoques y modelos de competencia. RELIEVE, v. 14, n. 2, p. 1-23. http://www.uv.es/RELIEVE/v14n2/RELIEVEv14n2_1.htm
3. Informe UNE 66173 IN, Octubre 2003 "Los recursos humanos en un sistema de gestión de calidad. Gestión de las competencias. Documento Internet, 22 pp. Dispnible en: https://qualitasbiblo.files.wordpress.com/2013/01/une-66173-2003-gestic3b3n-de-las-competencias.pdf
4. ¿Qué son los Cuidados Paliativos Pediátricos?. Sociedad Española de Cuidados Paliativos Pediátricos (PEDPAL) Página Web. Disponible en: https://www.pedpal.es/site/quienes-somos/que-son-los-cuidados-paliativos-pediatricos/
5. ¿Qué es un especialista certificado en vida infantil? Association of child Life Professionals. Página Web. Disponible en: https://www.childlife.org/the-child-life-profession
_________________________________